Cellule souche
Dans les Organismes multicellulaires , les cellules souches sont des cellules indifférenciées ou partiellement différenciées qui peuvent se différencier en différents Types de cellules et proliférer indéfiniment pour produire davantage de la même cellule souche. Ils sont le type de cellule le plus ancien d’une lignée cellulaire . [1] On les trouve à la fois dans les organismes embryonnaires et adultes, mais ils ont des propriétés légèrement différentes dans chacun. Elles se distinguent généralement des Cellules progénitrices , qui ne peuvent pas se diviser indéfiniment, et des cellules précurseurs .ou les cellules blastiques, qui sont généralement engagées à se différencier en un type de cellule.
| Cellule souche | |
|---|---|
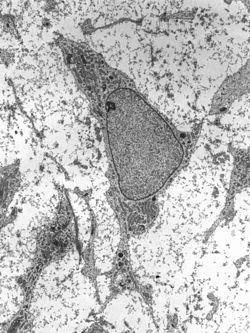 Micrographie électronique à transmission d’une cellule souche mésenchymateuse présentant des caractéristiques ultrastructurales typiques Micrographie électronique à transmission d’une cellule souche mésenchymateuse présentant des caractéristiques ultrastructurales typiques |
|
| Des détails | |
| Identifiants | |
| Latin | Cellula precursoria |
| Engrener | D013234 |
| E | H1.00.01.0.00028, H2.00.01.0.00001 |
| FMA | 63368 |
| Terminologie anatomique [ modifier sur Wikidata ] |
Chez les Mammifères , environ 50 à 150 cellules constituent la masse cellulaire interne au stade blastocyste du développement embryonnaire, vers les jours 5 à 14. Ceux-ci ont une capacité de cellules souches. In vivo , elles finissent par se différencier en tous les Types de cellules de l’organisme (ce qui les rend pluripotentes ). Ce processus commence par la différenciation en trois couches germinales – l’ ectoderme , le mésoderme et l’ endoderme – au stade de la gastrulation . Cependant, lorsqu’ils sont isolés et cultivés in vitro , ils peuvent être conservés au stade de cellule souche et sont connus sous le nom decellules souches embryonnaires (CSE).
Les cellules souches adultes se trouvent dans quelques endroits sélectionnés du corps, appelés niches , telles que celles de la moelle osseuse ou des gonades . Ils existent pour reconstituer les Types de cellules rapidement perdus et sont multipotents ou unipotents, ce qui signifie qu’ils ne se différencient qu’en quelques Types de cellules ou en un seul type de cellule. Chez les Mammifères, elles comprennent, entre autres, les cellules souches hématopoïétiques , qui reconstituent les cellules sanguines et immunitaires, les cellules basales , qui maintiennent l’ épithélium cutané , et les cellules souches mésenchymateuses , qui maintiennent les os, le cartilage, musculaires et adipeuses. Les cellules souches adultes sont une petite minorité de cellules ; ils sont largement dépassés en nombre par les Cellules progénitrices et les cellules différenciées en phase terminale dans lesquelles ils se différencient. [1]
La recherche sur les cellules souches est née des découvertes des biologistes canadiens Ernest McCulloch , James Till et Andrew J. Becker de l’ Université de Toronto et de l’Ontario Cancer Institute dans les années 1960. [2] [3] Depuis 2016 [mettre à jour], la seule thérapie médicale établie utilisant des cellules souches est la greffe de cellules souches hématopoïétiques , [4] réalisée pour la première fois en 1958 par l’oncologue français Georges Mathé . Depuis 1998 cependant, il est possible de cultiver et de différencier des cellules souches embryonnaires humaines (dans des lignées de cellules souches ). Le processus d’isolement de ces cellules a été controversé, car cela entraîne généralement la destruction de l’embryon. Les sources d’isolement des CSE ont été restreintes dans certains pays européens et au Canada, mais d’autres comme le Royaume-Uni et la Chine ont promu la recherche. [5] Le transfert nucléaire de cellules somatiques est une méthode de clonage qui peut être utilisée pour créer un embryon cloné pour l’utilisation de ses cellules souches embryonnaires dans la thérapie par cellules souches. [6] En 2006, une équipe japonaise dirigée par Shinya Yamanaka a découvert une méthode pour reconvertir les cellules matures du corps en cellules souches. Celles-ci ont été appelées cellules souches pluripotentes induites (iPSC). [7]
Histoire
Le terme cellule souche a été inventé par Theodor Boveri et Valentin Haecker à la fin du 19e siècle. [8] Des travaux pionniers sur la théorie des cellules souches sanguines ont été menés au début du XXe siècle par Artur Pappenheim , Alexander Maximow , Franz Ernst Christian Neumann . [8]
Les principales propriétés d’une cellule souche ont été définies pour la première fois par Ernest McCulloch et James Till de l’Université de Toronto et de l’Ontario Cancer Institute au début des années 1960. Ils ont découvert la cellule souche hématopoïétique, la cellule souche hématopoïétique (CSH), grâce à leur travail de pionnier chez la souris. McCulloch et Till ont commencé une série d’expériences dans lesquelles des cellules de moelle osseuse ont été injectées à des souris irradiées. Ils ont observé des grumeaux dans la rate des souris qui étaient linéairement proportionnels au nombre de cellules de moelle osseuse injectées. Ils ont émis l’hypothèse que chaque masse (colonie) était un clone provenant d’une seule cellule de moelle (cellule souche). Dans les travaux ultérieurs, McCulloch et Till, rejoints par l’étudiant diplômé Andrew John Becker et le scientifique principal Louis Siminovitch, a confirmé que chaque masse provenait en fait d’une seule cellule. Leurs résultats ont été publiés dans Nature en 1963. La même année, Siminovitch était l’un des principaux chercheurs d’études qui ont révélé que les cellules formant des colonies étaient capables de s’auto-renouveler, ce qui est une propriété clé des cellules souches que Till et McCulloch avaient théorisée. [9]
La première thérapie utilisant des cellules souches fut une greffe de moelle osseuse réalisée par l’oncologue français Georges Mathé en 1958 sur cinq travailleurs de l’ Institut nucléaire de Vinča en Yougoslavie qui avaient été touchés par un accident de criticité . Les ouvriers ont tous survécu. [dix]
En 1981, des cellules souches embryonnaires (ES) ont d’abord été isolées et cultivées avec succès à l’aide de blastocystes de souris par les biologistes britanniques Martin Evans et Matthew Kaufman . Cela a permis la formation de modèles génétiques murins, un système dans lequel les gènes de souris sont supprimés ou modifiés afin d’étudier leur fonction en pathologie. En 1998, des cellules souches embryonnaires ont été isolées pour la première fois par le biologiste américain James Thomson , ce qui a permis de disposer de nouvelles méthodes de transplantation ou de différents types cellulaires pour tester de nouveaux traitements. En 2006, Shinya YamanakaL’équipe de Kyoto, au Japon, a converti des fibroblastes en cellules souches pluripotentes en modifiant l’expression de seulement quatre gènes. L’exploit représente l’origine des cellules souches pluripotentes induites, appelées cellules iPS. [7]
En 2011, une louve à crinière femelle , renversée par un camion, a subi un traitement par cellules souches au zoo de Brasilia , ce qui est le premier cas enregistré d’utilisation de cellules souches pour soigner des blessures chez un animal sauvage. [11] [12]
Propriétés
La définition classique d’une cellule souche exige qu’elle possède deux propriétés :
- Auto-renouvellement : la capacité de passer par de nombreux cycles de croissance cellulaire et de division cellulaire , connus sous le nom de prolifération cellulaire , tout en maintenant l’état indifférencié.
- Puissance : capacité à se différencier en types cellulaires spécialisés. Au sens le plus strict, cela nécessite que les cellules souches soient totipotentes ou pluripotentes – pour pouvoir donner naissance à n’importe quel type de cellule mature, bien que les Cellules progénitrices multipotentes ou unipotentes soient parfois appelées cellules souches. En dehors de cela, on dit que la fonction des cellules souches est régulée par un mécanisme de rétroaction.
Auto-renouvellement
Deux mécanismes garantissent le maintien d’une population de cellules souches (ne diminue pas en taille) :
1. Division cellulaire asymétrique : une cellule souche se divise en une cellule mère, identique à la cellule souche d’origine, et une autre cellule fille, qui est différenciée.
Lorsqu’une cellule souche s’auto-renouvelle, elle se divise et ne perturbe pas l’état indifférencié. Cet auto-renouvellement exige le contrôle du cycle cellulaire ainsi que le maintien de la multipotence ou de la pluripotence, qui dépendent toutes de la cellule souche. [13]
2. Différenciation stochastique : lorsqu’une cellule souche se développe et se divise en deux cellules filles différenciées, une autre cellule souche subit une mitose et produit deux cellules souches identiques à l’originale.
Les cellules souches utilisent la télomérase , une protéine qui restaure les télomères , pour protéger leur ADN et étendre leur limite de division cellulaire (la limite de Hayflick ). [14]
Signification de la puissance
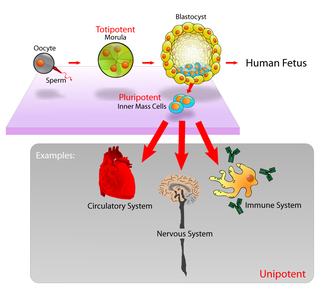
 Les cellules souches embryonnaires pluripotentes proviennent de cellules de la masse cellulaire interne (ICM) dans un blastocyste. Ces cellules souches peuvent devenir n’importe quel tissu du corps, à l’exception du placenta. Seules les cellules d’un stade antérieur de l’embryon, connues sous le nom de morula , sont totipotentes, capables de devenir tous les tissus du corps et le placenta extra-embryonnaire.
Les cellules souches embryonnaires pluripotentes proviennent de cellules de la masse cellulaire interne (ICM) dans un blastocyste. Ces cellules souches peuvent devenir n’importe quel tissu du corps, à l’exception du placenta. Seules les cellules d’un stade antérieur de l’embryon, connues sous le nom de morula , sont totipotentes, capables de devenir tous les tissus du corps et le placenta extra-embryonnaire. 
 Cellules souches embryonnaires humaines
Cellules souches embryonnaires humaines
A : Colonies de cellules souches non encore différenciées.
B : Cellules nerveuses , un exemple de type cellulaire après différenciation.
La puissance spécifie le potentiel de différenciation (le potentiel de se différencier en différents Types de cellules) de la cellule souche. [15]
- Les cellules souches totipotentes (également appelées omnipotentes) peuvent se différencier en Types de cellules embryonnaires et extra-embryonnaires. De telles cellules peuvent construire un organisme complet et viable. [15] Ces cellules sont produites à partir de la fusion d’un ovule et d’un spermatozoïde. Les cellules produites par les premières divisions de l’œuf fécondé sont également totipotentes. [16]
- Les cellules souches pluripotentes sont les descendantes des cellules totipotentes et peuvent se différencier en presque toutes les cellules, [15] c’est-à-dire des cellules dérivées de l’une des trois couches germinales . [17]
- Les cellules souches multipotentes peuvent se différencier en un certain nombre de Types de cellules, mais uniquement celles d’une famille de cellules étroitement apparentées. [15]
- Les cellules souches oligopotentes peuvent se différencier en quelques Types de cellules seulement, comme les cellules souches lymphoïdes ou myéloïdes. [15]
- Les cellules unipotentes ne peuvent produire qu’un seul type de cellule, la leur, [15] mais ont la propriété d’auto-renouvellement, ce qui les distingue des cellules non souches
Identification
En pratique, les cellules souches sont identifiées selon leur capacité à régénérer les tissus. Par exemple, le test déterminant pour la moelle osseuse ou les cellules souches hématopoïétiques (CSH) est la capacité de transplanter les cellules et de sauver un individu sans CSH. Cela démontre que les cellules peuvent produire de nouvelles cellules sanguines à long terme. Il devrait également être possible d’isoler des cellules souches de l’individu greffé, qui peuvent elles-mêmes être transplantées dans un autre individu sans CSH, démontrant que la cellule souche était capable de s’auto-renouveler.
Les propriétés des cellules souches peuvent être illustrées in vitro , à l’aide de méthodes telles que les tests clonogéniques , dans lesquels des cellules individuelles sont évaluées pour leur capacité à se différencier et à s’auto-renouveler. [18] [19] Les cellules souches peuvent également être isolées par leur possession d’un ensemble distinctif de marqueurs de surface cellulaire. Cependant, les conditions de culture in vitro peuvent modifier le comportement des cellules, ce qui rend difficile de savoir si les cellules doivent se comporter de manière similaire in vivo . Il y a un débat considérable quant à savoir si certaines populations de cellules adultes proposées sont vraiment des cellules souches. [20]
Embryonnaire
Les cellules souches embryonnaires (CSE) sont les cellules de la masse cellulaire interne d’un blastocyste , formées avant l’ implantation dans l’utérus. [21] Dans le développement embryonnaire humain, le stade de blastocyste est atteint 4 à 5 jours après la fécondation , moment auquel il se compose de 50 à 150 cellules. Les CSE sont pluripotentes et donnent naissance au cours du développement à tous les dérivés des trois couches germinales : ectoderme , endoderme et mésoderme . En d’autres termes, ils peuvent se développer dans chacun des plus de 200 Types de cellules du corps adultelorsqu’il reçoit une stimulation suffisante et nécessaire pour un type de cellule spécifique. Ils ne contribuent ni aux membranes extra -embryonnaires ni au placenta .
Au cours du développement embryonnaire, les cellules de la masse cellulaire interne se divisent continuellement et se spécialisent. Par exemple, une partie de l’ectoderme de la partie dorsale de l’embryon se spécialise en « neurectoderme », qui deviendra le futur système nerveux central . [22] Plus tard dans le développement, la neurulation amène le neurectoderme à former le tube neural . Au stade du tube neural, la partie antérieure subit une encéphalisation pour générer ou « modeler » la forme de base du cerveau. À ce stade de développement, le principal type cellulaire du SNC est considéré comme une cellule souche neurale .
Les cellules souches neurales s’auto-renouvellent et, à un moment donné, se transforment en Cellules progénitrices gliales radiales (RGP). Les RGP formés tôt s’auto-renouvellent par division symétrique pour former un groupe réservoir de Cellules progénitrices . Ces cellules passent à un état neurogène et commencent à se diviser de manière asymétrique pour produire une grande diversité de nombreux types de neurones différents, chacun avec une expression génique, des caractéristiques morphologiques et fonctionnelles uniques. Le processus de génération de neurones à partir de cellules gliales radiales est appelé neurogenèse . La cellule gliale radiale a une morphologie bipolaire distinctive avec des processus très allongés couvrant l’épaisseur de la paroi du tube neural. Il partage quelques glialescaractéristiques, notamment l’expression de la protéine acide fibrillaire gliale (GFAP). [23] [24] La cellule gliale radiale est la cellule souche neurale primaire du SNC des vertébrés en développement , et son corps cellulaire réside dans la zone ventriculaire , adjacente au système ventriculaire en développement . Les cellules souches neurales sont engagées dans les lignées neuronales ( neurones , astrocytes et oligodendrocytes ), et leur puissance est donc limitée. [22]
Presque toutes les recherches à ce jour ont utilisé des cellules souches embryonnaires de souris (mES) ou des cellules souches embryonnaires humaines (hES) dérivées de la masse cellulaire interne précoce. Les deux ont les caractéristiques essentielles des cellules souches, mais elles nécessitent des environnements très différents afin de maintenir un état indifférencié. Les cellules ES de souris sont cultivées sur une couche de gélatine en tant que matrice extracellulaire (pour le support) et nécessitent la présence de facteur inhibiteur de la leucémie (LIF) dans le milieu sérique. Un cocktail de médicaments contenant des inhibiteurs de GSK3B et de la voie MAPK/ERK , appelé 2i, s’est également avéré maintenir la pluripotence dans la culture de cellules souches. [25] Les CSE humaines sont cultivées sur une couche nourricière d’embryons de sourisfibroblastes et nécessitent la présence de facteur de croissance basique des fibroblastes (bFGF ou FGF-2). [26] Sans conditions de culture optimales ni manipulation génétique, [27] les cellules souches embryonnaires se différencieront rapidement.
Une cellule souche embryonnaire humaine est également définie par l’expression de plusieurs facteurs de transcription et protéines de surface cellulaire. Les facteurs de transcription Oct-4 , Nanog et Sox2 forment le réseau de régulation de base qui assure la suppression des gènes qui conduisent à la différenciation et au maintien de la pluripotence. [28] Les antigènes de surface cellulaire les plus couramment utilisés pour identifier les cellules hES sont les antigènes embryonnaires spécifiques au stade des glycolipides 3 et 4, et les antigènes de sulfate de kératan Tra-1-60 et Tra-1-81. La définition moléculaire d’une cellule souche comprend beaucoup plus de protéines et continue d’être un sujet de recherche. [29]
En utilisant des cellules souches embryonnaires humaines pour produire des cellules spécialisées telles que des cellules nerveuses ou des cellules cardiaques en laboratoire, les scientifiques peuvent accéder à des cellules humaines adultes sans prélever de tissus sur des patients. Ils peuvent ensuite étudier en détail ces cellules adultes spécialisées pour tenter de discerner les complications des maladies ou pour étudier les réactions cellulaires aux nouveaux médicaments proposés.
En raison de leurs capacités combinées d’expansion illimitée et de pluripotence, les cellules souches embryonnaires restent théoriquement une source potentielle pour la médecine régénérative et le remplacement des tissus après une blessure ou une maladie. [30] Cependant, il n’existe actuellement aucun traitement approuvé utilisant des cellules ES. Le premier essai sur l’homme a été approuvé par la Food and Drug Administration des États-Unis en janvier 2009. [31] Cependant, l’essai sur l’homme n’a été lancé que le 13 octobre 2010 à Atlanta pour la recherche sur les lésions de la moelle épinière . Le 14 novembre 2011, la société menant l’essai ( Geron Corporation ) a annoncé qu’elle interromprait le développement de ses programmes de cellules souches. [32]Différencier les cellules ES en cellules utilisables tout en évitant le rejet de greffe ne sont que quelques-uns des obstacles auxquels les chercheurs sur les cellules souches embryonnaires sont encore confrontés. [33] Les cellules souches embryonnaires, étant pluripotentes, nécessitent des signaux spécifiques pour une différenciation correcte – si elles sont injectées directement dans un autre corps, les cellules ES se différencieront en de nombreux Types de cellules différents, provoquant un tératome . Les considérations éthiques concernant l’utilisation de tissus humains à naître sont une autre raison du manque de traitements approuvés utilisant des cellules souches embryonnaires. De nombreux pays ont actuellement des moratoires ou des limitations sur la recherche sur les cellules ES humaines ou sur la production de nouvelles lignées de cellules ES humaines.
-
![]()
![]()
Cellules souches embryonnaires de souris avec marqueur fluorescent
-
![]()
![]()
Colonie de cellules souches embryonnaires humaines sur couche nourricière de fibroblastes embryonnaires de souris
Les cellules souches mésenchymateuses
Les cellules souches mésenchymateuses (MSC) sont connues pour être multipotentes, que l’on peut trouver dans les tissus adultes, par exemple, dans le muscle, le foie, la moelle osseuse. Les cellules souches mésenchymateuses fonctionnent généralement comme support structurel dans divers organes, comme mentionné ci-dessus, et contrôlent le mouvement des substances. Les MSC peuvent se différencier en de nombreuses catégories de cellules comme par exemple les adipocytes, les ostéocytes et les chondrocytes, dérivés de la couche mésodermique. [34]Où la couche de mésoderme fournit une augmentation des éléments squelettiques du corps, tels que ceux liés au cartilage ou à l’os. Le terme « méso » signifie milieu, infusion originaire du grec, signifiant que les cellules mésenchymateuses sont capables de se déplacer et de se déplacer au début de la croissance embryonnaire entre les couches ectodermiques et endodermiques. Ce mécanisme aide à remplir l’espace, ce qui est essentiel pour réparer les plaies des organismes adultes qui ont à voir avec les cellules mésenchymateuses du derme (peau), des os ou des muscles. [35]
Les cellules souches mésenchymateuses sont connues pour être essentielles à la médecine régénérative. Ils sont largement étudiés dans les essais cliniques. Puisqu’ils sont facilement isolés et obtiennent un rendement élevé, une plasticité élevée, ce qui permet de faciliter l’inflammation et d’encourager la croissance cellulaire, la différenciation cellulaire et la restauration des tissus dérivés de l’immunomodulation et de l’immunosuppression. Les MSC proviennent de la moelle osseuse, ce qui nécessite une procédure agressive pour isoler la quantité et la qualité de la cellule isolée, et cela varie en fonction de l’âge du donneur. Lorsque l’on compare les taux de MSC dans les aspirations de moelle osseuse et le stroma de moelle osseuse, les aspirations ont tendance à avoir des taux de MSC inférieurs à ceux du stroma. Les MSC sont connues pour être hétérogènes et expriment un niveau élevé de marqueurs pluripotents par rapport à d’autres Types de cellules souches, telles que les cellules souches embryonnaires. [34]
Contrôle du cycle cellulaire
Les cellules souches embryonnaires (CSE) ont la capacité de se diviser indéfiniment tout en conservant leur pluripotence , ce qui est rendu possible grâce à des mécanismes spécialisés de contrôle du cycle cellulaire . [36] Par rapport aux cellules somatiques proliférantes , les ESC ont des caractéristiques uniques du cycle cellulaire, telles qu’une division cellulaire rapide causée par une phase G1 raccourcie, une phase G0 absente et des modifications des points de contrôle du cycle cellulaire, ce qui laisse les cellules principalement en phase S à tout moment . . [36] [37]La division rapide des ESC est démontrée par leur court temps de doublement, qui varie de 8 à 10 heures, alors que les cellules somatiques ont un temps de doublement d’environ 20 heures ou plus. [38] Au fur et à mesure que les cellules se différencient, ces propriétés changent : les phases G1 et G2 s’allongent, entraînant des cycles de division cellulaire plus longs. Cela suggère qu’une structure spécifique du cycle cellulaire peut contribuer à l’établissement de la pluripotence. [36]
En particulier parce que la phase G1 est la phase dans laquelle les cellules ont une sensibilité accrue à la différenciation, le G1 raccourci est l’une des caractéristiques clés des ESC et joue un rôle important dans le maintien du phénotype indifférencié . Bien que le mécanisme moléculaire exact ne soit que partiellement compris, plusieurs études ont montré comment les ESC progressent à travers G1 – et potentiellement d’autres phases – si rapidement. [37]
Le cycle cellulaire est régulé par un réseau complexe de cyclines , de kinases dépendantes des cyclines (Cdk), d’inhibiteurs de kinases dépendantes des cyclines (Cdkn), de protéines de poche de la famille des rétinoblastomes (Rb) et d’autres facteurs accessoires. [38] Un aperçu fondamental de la régulation distinctive du cycle cellulaire des ESC a été obtenu par des études sur les ESC de souris (mESC). [37] Les mESC ont montré un cycle cellulaire avec une phase G1 très abrégée, ce qui a permis aux cellules d’alterner rapidement entre la phase M et la phase S. Dans un cycle cellulaire somatique, l’activité oscillatoire des complexes Cycline-Cdk est observée en action séquentielle, qui contrôle des régulateurs cruciaux du cycle cellulaire pour induire des transitions unidirectionnelles entre les phases : Cycline Det Cdk4/6 sont actifs dans la phase G1, tandis que la cycline E et Cdk2 sont actives pendant la phase G1 tardive et la phase S ; et la cycline A et Cdk2 sont actives en phase S et G2, tandis que la cycline B et Cdk1 sont actives en phase G2 et M. [38] Cependant, dans les mESC, cette activité typiquement ordonnée et oscillatoire des complexes Cycline-Cdk est absente. Au contraire, le complexe Cycline E/Cdk2 est constitutivement actif tout au long du cycle, maintenant la protéine du rétinoblastome (pRb) hyperphosphorylée et donc inactive. Cela permet une transition directe de la phase M à la phase G1 tardive, conduisant à l’absence de cyclines de type D et donc à une phase G1 raccourcie.[37] L’activité de Cdk2 est cruciale à la fois pour la régulation du cycle cellulaire et les décisions relatives au destin cellulaire dans les mESC ; la régulation à la baisse de l’activité de Cdk2 prolonge la progression de la phase G1, établit un cycle cellulaire de type cellule somatique et induit l’expression de marqueurs de différenciation. [39]
Dans les CSE humaines (CSEh), la durée de G1 est considérablement raccourcie. Cela a été attribué à des niveaux élevés d’ARNm des gènes Cycline D2 et Cdk4 liés à G1 et à de faibles niveaux de protéines régulatrices du cycle cellulaire qui inhibent la progression du cycle cellulaire à G1, telles que p21 CipP1 , p27 Kip1 et p57 Kip2 . [36] [40]De plus, les régulateurs de l’activité Cdk4 et Cdk6, tels que les membres de la famille des inhibiteurs Ink (p15, p16, p18 et p19), sont exprimés à des niveaux faibles ou pas du tout. Ainsi, à l’instar des mESC, les hESC présentent une activité Cdk élevée, Cdk2 présentant l’activité kinase la plus élevée. Également similaires aux mESC, les hESC démontrent l’importance de Cdk2 dans la régulation de la phase G1 en montrant que la transition de G1 à S est retardée lorsque l’activité de Cdk2 est inhibée et que G1 s’arrête lorsque Cdk2 est renversé. [36] Cependant, contrairement aux mESC, les hESC ont une phase G1 fonctionnelle. Les CSEh montrent que les activités des complexes Cycline E/Cdk2 et Cycline A/Cdk2 dépendent du cycle cellulaire et que le point de contrôle Rb dans G1 est fonctionnel. [38]
Les ESC sont également caractérisées par la non-fonctionnalité du point de contrôle G1, même si le point de contrôle G1 est crucial pour le maintien de la stabilité génomique. En réponse aux dommages à l’ADN , les ESC ne s’arrêtent pas en G1 pour réparer les dommages à l’ADN, mais dépendent plutôt des points de contrôle S et G2/M ou subissent une apoptose. L’absence de point de contrôle G1 dans les ESC permet d’éliminer les cellules dont l’ADN est endommagé, évitant ainsi les mutations potentielles dues à une réparation inexacte de l’ADN. [36] Conformément à cette idée, les ESC sont hypersensibles aux dommages à l’ADN afin de minimiser les mutations transmises à la génération suivante. [38]
Fœtal
Les cellules souches primitives situées dans les organes des fœtus sont appelées cellules souches fœtales. [41]
Il existe deux Types de cellules souches fœtales :
- Les cellules souches fœtales propres proviennent des tissus du fœtus proprement dit et sont généralement obtenues après un avortement . Ces cellules souches ne sont pas immortelles mais ont un haut niveau de division et sont multipotentes.
- Les cellules souches fœtales extra-embryonnaires proviennent de membranes extra-embryonnaires et ne se distinguent généralement pas des cellules souches adultes. Ces cellules souches sont acquises après la naissance, elles ne sont pas immortelles mais ont un haut niveau de division cellulaire, et sont pluripotentes. [42]
Adulte
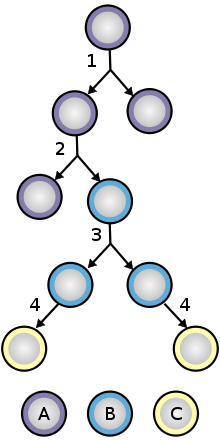
 Division et différenciation des cellules souches A : cellule souche ; B : cellule progénitrice ; C : cellule différenciée ; 1 : division symétrique des cellules souches ; 2 : division asymétrique des cellules souches ; 3 : division progénitrice ; 4 : différenciation terminale
Division et différenciation des cellules souches A : cellule souche ; B : cellule progénitrice ; C : cellule différenciée ; 1 : division symétrique des cellules souches ; 2 : division asymétrique des cellules souches ; 3 : division progénitrice ; 4 : différenciation terminale
Les cellules souches adultes, également appelées cellules souches somatiques (du grec σωματικóς, « du corps »), sont des cellules souches qui entretiennent et réparent les tissus dans lesquels elles se trouvent. [43] Ils peuvent être trouvés chez les enfants, ainsi que les adultes. [44]
Il existe trois sources accessibles connues de cellules souches adultes autologues chez l’homme :
- Moelle osseuse , qui nécessite une extraction par prélèvement , généralement à partir des os du bassin par chirurgie. [45]
- Tissu adipeux (cellules graisseuses), qui nécessite une extraction par liposuccion. [46]
- Sang, qui nécessite une extraction par aphérèse , dans laquelle le sang est prélevé sur le donneur (similaire à un don de sang) et passé dans une machine qui extrait les cellules souches et renvoie d’autres parties du sang au donneur. [ citation nécessaire ]
Les cellules souches peuvent également être prélevées dans le sang du cordon ombilical juste après la naissance. De tous les Types de cellules souches, la récolte autologue comporte le moins de risques. Par définition, les cellules autologues sont obtenues à partir de son propre corps, tout comme on peut conserver son propre sang pour des interventions chirurgicales électives. [ citation nécessaire ]
Les cellules souches adultes pluripotentes sont rares et généralement peu nombreuses, mais elles peuvent être trouvées dans le sang du cordon ombilical et d’autres tissus. [47] La moelle osseuse est une riche source de cellules souches adultes, [48] qui ont été utilisées dans le traitement de plusieurs affections, notamment la cirrhose du foie, [49] l’ischémie chronique des membres [50] et l’insuffisance cardiaque terminale. [51] La quantité de cellules souches de la moelle osseuse diminue avec l’âge et est plus élevée chez les hommes que chez les femmes pendant les années de reproduction. [52] À ce jour, de nombreuses recherches sur les cellules souches adultes ont visé à caractériser leur puissance et leurs capacités d’auto-renouvellement. [53]Les dommages à l’ADN s’accumulent avec l’âge dans les cellules souches et les cellules qui composent l’environnement des cellules souches. Cette accumulation est considérée comme responsable, au moins en partie, de l’augmentation du dysfonctionnement des cellules souches avec le vieillissement (voir la théorie des dommages à l’ADN du vieillissement ). [54]
La plupart des cellules souches adultes sont à lignée restreinte ( multipotentes ) et sont généralement désignées par leur origine tissulaire ( cellule souche mésenchymateuse, cellule souche d’origine adipeuse, cellule souche endothéliale, cellule souche de la pulpe dentaire , etc.). [55] [56] Les cellules Muse (cellules endurantes au stress multi-lignées différenciées) sont un type de cellules souches pluripotentes récemment découvert que l’on trouve dans plusieurs tissus adultes, y compris les fibroblastes adipeux, dermiques et la moelle osseuse. Bien que rares, les cellules muses sont identifiables par leur expression de SSEA-3 , un marqueur pour les cellules souches indifférenciées, et des marqueurs généraux de cellules souches mésenchymateuses tels que CD105. Lorsqu’elles sont soumises à une culture en suspension monocellulaire, les cellules génèrent des grappes similaires aux corps embryoïdes en morphologie ainsi qu’en expression génique, y compris les marqueurs canoniques de pluripotence Oct4 , Sox2 et Nanog . [57]
Les traitements à base de cellules souches adultes sont utilisés avec succès depuis de nombreuses années pour traiter la leucémie et les cancers des os et du sang associés grâce à des greffes de moelle osseuse. [58] Les cellules souches adultes sont également utilisées en médecine vétérinaire pour traiter les lésions tendineuses et ligamentaires chez les chevaux. [59]
L’utilisation de cellules souches adultes dans la recherche et la thérapie n’est pas aussi controversée que l’utilisation de cellules souches embryonnaires , car la production de cellules souches adultes ne nécessite pas la destruction d’un embryon . De plus, dans les cas où des cellules souches adultes sont obtenues du receveur prévu (une autogreffe ), le risque de rejet est pratiquement inexistant. Par conséquent, davantage de financements du gouvernement américain sont accordés à la recherche sur les cellules souches adultes. [60]
Avec la demande croissante de cellules souches adultes humaines à des fins de recherche et cliniques (généralement 1 à 5 millions de cellules par kg de poids corporel sont nécessaires par traitement), il devient de la plus haute importance de combler le fossé entre la nécessité d’étendre les cellules in vitro et la capacité d’exploiter les facteurs sous-jacents à la sénescence réplicative. Les cellules souches adultes sont connues pour avoir une durée de vie limitée in vitro et pour entrer en sénescence réplicative de manière presque indétectable lors du démarrage de la culture in vitro. [61]
Amniotique
Aussi appelées cellules souches périnatales, ces cellules souches multipotentes se trouvent dans le liquide amniotique et le sang du cordon ombilical. Ces cellules souches sont très actives, se développent largement sans alimentation et ne sont pas tumorigènes. Les cellules souches amniotiques sont multipotentes et peuvent se différencier en cellules de lignées adipogéniques, ostéogéniques, myogéniques, endothéliales, hépatiques mais aussi neuronales. [62] Les cellules souches amniotiques sont un sujet de recherche active.
L’utilisation de cellules souches du liquide amniotique surmonte les objections éthiques à l’utilisation d’embryons humains comme source de cellules. L’enseignement catholique romain interdit l’utilisation de cellules souches embryonnaires dans l’expérimentation ; en conséquence, le journal vatican « Osservatore Romano » a qualifié les cellules souches amniotiques « d’avenir de la médecine ». [63]
Il est possible de prélever des cellules souches amniotiques pour des donneurs ou pour un usage autologue : la première banque américaine de cellules souches amniotiques [64] [65] a été ouverte en 2009 à Medford, MA, par Biocell Center Corporation [66] [67] [68] et collabore avec divers hôpitaux et universités du monde entier. [69]
Pluripotent induit
Les cellules souches adultes ont des limites quant à leur puissance ; contrairement aux cellules souches embryonnaires (CSE), elles ne sont pas capables de se différencier en cellules des trois couches germinales . A ce titre, ils sont réputés multipotents .
Cependant, la reprogrammation permet la création de cellules pluripotentes, cellules souches pluripotentes induites (iPSC), à partir de cellules adultes. Il ne s’agit pas de cellules souches adultes, mais de cellules somatiques (par exemple des cellules épithéliales) reprogrammées pour donner naissance à des cellules aux capacités pluripotentes. En utilisant la reprogrammation génétique avec des facteurs de transcription protéique , des cellules souches pluripotentes avec des capacités de type ESC ont été dérivées. [70] [71] [72] La première démonstration de cellules souches pluripotentes induites a été menée par Shinya Yamanaka et ses collègues de l’Université de Kyoto . [73] Ils ont utilisé les facteurs de transcription Oct3/4 , Sox2, c-Myc et Klf4 pour reprogrammer les fibroblastes de souris en cellules pluripotentes. [70] [74] Des travaux ultérieurs ont utilisé ces facteurs pour induire la pluripotence dans les cellules fibroblastiques humaines. [75] Junying Yu , James Thomson et leurs collègues de l’ Université du Wisconsin-Madison ont utilisé un ensemble différent de facteurs, Oct4, Sox2, Nanog et Lin28, et ont mené leurs expériences en utilisant des cellules de prépuce humain . [70] [76] Cependant, ils ont pu répliquer la découverte de Yamanaka selon laquelle l’induction de la pluripotence dans les cellules humaines était possible.
Les cellules souches pluripotentes induites diffèrent des cellules souches embryonnaires. Ils partagent de nombreuses propriétés similaires, telles que la pluripotence et le potentiel de différenciation, l’expression de gènes de pluripotence , les schémas épigénétiques , la formation de corps embryoïdes et de tératomes et la formation de chimères viables , [73] [74] mais il existe de nombreuses différences au sein de ces propriétés. La chromatine des iPSC semble être plus “fermée” ou méthylée que celle des ESC. [73] [74] De même, le modèle d’expression génique entre les ESC et les iPSC, ou même les iPSC provenant d’origines différentes. [73]On s’interroge ainsi sur la « complétude » de la reprogrammation et la mémoire somatique des cellules souches pluripotentes induites. Malgré cela, induire des cellules somatiques à être pluripotentes semble être viable.
Suite au succès de ces expériences, Ian Wilmut , qui a aidé à créer le premier animal cloné Dolly la brebis , a annoncé qu’il abandonnerait le transfert nucléaire de cellules somatiques comme voie de recherche. [77]
Les IPSC ont considérablement aidé le domaine de la médecine en trouvant de nombreuses façons de guérir les maladies. Depuis, l’IPSCc humain a donné l’avantage de créer des modèles in vitro pour étudier les toxines et la pathogenèse. [78]
De plus, les cellules souches pluripotentes induites offrent plusieurs avantages thérapeutiques. Comme les CES, ils sont pluripotents . Ils ont donc un grand potentiel de différenciation ; théoriquement, ils pourraient produire n’importe quelle cellule du corps humain (si la reprogrammation en pluripotence était “complète”). [73] De plus, contrairement aux ESC, ils pourraient potentiellement permettre aux médecins de créer une lignée de cellules souches pluripotentes pour chaque patient. [79] Les échantillons de sang congelés peuvent être utilisés comme source précieuse de cellules souches pluripotentes induites. [80] Les cellules souches spécifiques au patient permettent le dépistage des effets secondaires avant le traitement médicamenteux, ainsi que le risque réduit de rejet de greffe. [79]Malgré leur utilisation thérapeutique limitée actuelle, les CSPi recèlent un grand potentiel pour une utilisation future dans le traitement médical et la recherche.
Contrôle du cycle cellulaire
Les facteurs clés contrôlant le cycle cellulaire régulent également la pluripotence . Ainsi, la manipulation de gènes pertinents peut maintenir la pluripotence et reprogrammer les cellules somatiques dans un état Pluripotent induit. [38] Cependant, la reprogrammation des cellules somatiques est souvent peu efficace et considérée comme stochastique . [81]
Avec l’idée qu’un cycle cellulaire plus rapide est un élément clé de la pluripotence, l’efficacité de la reprogrammation peut être améliorée. Les méthodes d’amélioration de la pluripotence par la manipulation des régulateurs du cycle cellulaire comprennent : la surexpression de la cycline D/Cdk4, la phosphorylation de Sox2 à S39 et S253, la surexpression de la cycline A et de la cycline E, l’inactivation de Rb et l’inactivation des membres de la famille Cip/Kip ou la famille Encre. [38] De plus, l’efficacité de la reprogrammation est corrélée au nombre de divisions cellulaires survenues pendant la phase stochastique, ce qui est suggéré par l’inefficacité croissante de la reprogrammation des cellules de plongée plus anciennes ou lentes. [82]
Lignée
La lignée est une procédure importante pour analyser les embryons en développement. Puisque les lignées cellulaires montrent la relation entre les cellules à chaque division. Cela aide à analyser les lignées de cellules souches en cours de route, ce qui aide à reconnaître l’efficacité, la durée de vie et d’autres facteurs des cellules souches. Avec la technique de la lignée cellulaire, les gènes mutants peuvent être analysés dans des clones de cellules souches qui peuvent aider dans les voies génétiques. Ces voies peuvent réguler le fonctionnement de la cellule souche. [83]
Pour assurer leur auto-renouvellement, les cellules souches subissent deux types de division cellulaire (voir le schéma Division et différenciation des cellules souches ). La division symétrique donne naissance à deux cellules filles identiques, toutes deux dotées de propriétés de cellules souches. La division asymétrique, en revanche, ne produit qu’une seule cellule souche et une cellule progénitrice avec un potentiel d’auto-renouvellement limité. Les progéniteurs peuvent passer par plusieurs cycles de division cellulaire avant de se différencier en phase terminale en une cellule mature. Il est possible que la distinction moléculaire entre les divisions symétriques et asymétriques réside dans la ségrégation différentielle des protéines de la membrane cellulaire (telles que les récepteurs ) entre les cellules filles. [84]
Une théorie alternative est que les cellules souches restent indifférenciées en raison de signaux environnementaux dans leur niche particulière . Les cellules souches se différencient lorsqu’elles quittent cette niche ou ne reçoivent plus ces signaux. Des études sur le germarium de Drosophila ont identifié les signaux des jonctions décapentaplégiques et adhérentes qui empêchent les cellules souches du germarium de se différencier. [85] [86]
Thérapies
La thérapie par cellules souches est l’utilisation de cellules souches pour traiter ou prévenir une maladie ou un état. La greffe de moelle osseuse est une forme de thérapie par cellules souches qui est utilisée depuis de nombreuses années car elle s’est avérée efficace dans les essais cliniques. [87] [88]
L’implantation de cellules souches peut aider à renforcer le ventricule gauche du cœur, ainsi qu’à conserver le tissu cardiaque chez les patients qui ont souffert de crises cardiaques dans le passé. [89]
Avantages
Les traitements à base de cellules souches peuvent atténuer les symptômes de la maladie ou de l’affection traitée. La diminution des symptômes peut permettre aux patients de réduire la prise de médicaments de la maladie ou de l’affection. Le traitement des cellules souches peut également fournir des connaissances à la société pour approfondir la compréhension des cellules souches et les futurs traitements. [90] Le credo des médecins serait de ne pas blesser, et les cellules souches rendent cela plus simple que jamais. Les processus chirurgicaux par leur caractère sont nocifs. Les tissus doivent être abandonnés pour obtenir un résultat positif. On peut prévenir les dangers des interventions chirurgicales utilisant des cellules souches. De plus, il existe un risque de maladie et, si la procédure échoue, une nouvelle intervention chirurgicale peut être nécessaire. Les risques associés à l’anesthésie peuvent également être éliminés grâce aux cellules souches. [91]En plus de cela, des cellules souches ont été prélevées sur le corps du patient et redéployées là où elles sont recherchées. Puisqu’ils proviennent du propre corps du patient, on parle de traitement autologue. Les remèdes autologues sont considérés comme les plus sûrs car il n’y a probablement aucune probabilité de rejet de la substance du donneur.
Désavantages
Les traitements à base de cellules souches peuvent nécessiter une immunosuppression en raison d’un besoin de radiothérapie avant la greffe pour éliminer les cellules précédentes de la personne, ou parce que le système immunitaire du patient peut cibler les cellules souches. Une approche pour éviter la deuxième possibilité consiste à utiliser des cellules souches du même patient qui est traité.
La pluripotence de certaines cellules souches pourrait également rendre difficile l’obtention d’un type cellulaire spécifique. Il est également difficile d’obtenir le type cellulaire exact nécessaire, car toutes les cellules d’une population ne se différencient pas uniformément. Les cellules indifférenciées peuvent créer des tissus autres que les types souhaités. [92]
Certaines cellules souches forment des tumeurs après la transplantation ; [93] la pluripotence est liée à la formation de tumeurs, en particulier dans les cellules souches embryonnaires, les cellules souches propres au fœtus, les cellules souches pluripotentes induites. Les cellules souches propres au fœtus forment des tumeurs malgré la multipotence. [94]
Des préoccupations éthiques sont également soulevées quant à la pratique consistant à utiliser ou à rechercher des cellules souches embryonnaires. La récolte des cellules du blastocyste entraîne la mort du blastocyste. La question est de savoir si le blastocyste doit être considéré ou non comme une vie humaine. [95] Le débat sur cette question est essentiellement philosophique et non scientifique.
Tourisme de cellules souches
Le tourisme des cellules souches est l’industrie dans laquelle les patients (et parfois leurs familles) se rendent dans une autre juridiction pour obtenir des procédures de cellules souches qui ne sont pas approuvées mais qui sont annoncées sur Internet comme des remèdes éprouvés. [96]
Les États-Unis, ces dernières années [ quand ? ] , a eu une explosion de “cliniques de cellules souches”. [97] Les procédures de cellules souches sont très rentables pour les cliniques. La publicité fait autorité, mais l’efficacité et la sécurité des procédures ne sont pas prouvées. Les patients éprouvent parfois des complications, telles que des tumeurs de la colonne vertébrale [98] et la mort. Les dépenses élevées peuvent également conduire à la ruine financière. [98] Selon les chercheurs, il est nécessaire d’éduquer le public, les patients et les médecins sur cette question. [99]
Selon la Société internationale pour la recherche sur les cellules souches , la plus grande organisation universitaire qui défend la recherche sur les cellules souches, les thérapies à base de cellules souches sont en cours de développement et ne peuvent pas encore être considérées comme prouvées. [100] [101] Les médecins doivent informer les patients que les essais cliniques continuent d’étudier si ces thérapies sont sûres et efficaces, mais que les cliniques contraires à l’éthique les présentent comme prouvées. [102]
Rechercher
Certains des brevets fondamentaux couvrant les cellules souches embryonnaires humaines appartiennent à la Wisconsin Alumni Research Foundation (WARF) – il s’agit des brevets 5 843 780, 6 200 806 et 7 029 913 inventés par James A. Thomson . WARF n’applique pas ces brevets contre les scientifiques universitaires, mais les applique contre les entreprises. [103]
En 2006, une requête auprès de l’ Office américain des brevets et des marques (USPTO) pour réexaminer les trois brevets a été déposée par la Public Patent Foundation au nom de son client, le groupe à but non lucratif de surveillance des brevets Consumer Watchdog (anciennement la Foundation for Droits du contribuable et du consommateur). [103] Dans le processus de réexamen, qui implique plusieurs séries de discussions entre l’USPTO et les parties, l’USPTO a initialement accepté Consumer Watchdog et a rejeté toutes les revendications des trois brevets, [104]cependant, en réponse, WARF a modifié les revendications des trois brevets pour les rendre plus étroites et, en 2008, l’USPTO a conclu que les revendications modifiées des trois brevets étaient brevetables. La décision sur l’un des brevets (7 029 913) était susceptible d’appel, tandis que les décisions sur les deux autres ne l’étaient pas. [105] [106] Consumer Watchdog a fait appel de l’octroi du brevet ‘913 auprès de la Commission des appels et des interférences en matière de brevets (BPAI) de l’USPTO, qui a accordé l’appel, et en 2010, la BPAI a décidé que les revendications modifiées du brevet ‘913 n’étaient pas brevetable. [107] Cependant, WARF a pu rouvrir la poursuite de l’affaire et l’a fait, modifiant à nouveau les revendications du brevet ‘913 pour les rendre plus étroites, et en janvier 2013, les revendications modifiées ont été autorisées. [108]
En juillet 2013, Consumer Watchdog a annoncé qu’il ferait appel de la décision d’autoriser les revendications du brevet ‘913 devant la Cour d’appel des États-Unis pour le circuit fédéral (CAFC), la cour d’appel fédérale qui entend les affaires de brevets. [109] Lors d’une audience en décembre 2013, le CAFC a soulevé la question de savoir si Consumer Watchdog avait qualité pour interjeter appel; l’affaire ne pouvait pas continuer tant que ce problème n’était pas résolu. [110]
Enquêtes

 Maladies et affections pour lesquelles un traitement par cellules souches est à l’étude.
Maladies et affections pour lesquelles un traitement par cellules souches est à l’étude.
Les maladies et affections pour lesquelles un traitement par cellules souches est à l’étude comprennent :
- Diabète [111]
- Alopécie androgénique et perte de cheveux [112] [113]
- Polyarthrite rhumatoïde [111]
- Maladie de Parkinson [111]
- Maladie d’Alzheimer [111]
- Arthrose [111]
- Réparation d’AVC et de lésions cérébrales traumatiques [114]
- Trouble d’ apprentissage dû à une maladie congénitale [115]
- Réparation des lésions de la moelle épinière [116]
- Infarctus cardiaque [117]
- Traitements anticancéreux [ 114 ]
- Inversion de la calvitie [ 118 ]
- Remplacer les dents manquantes [119]
- Audience de réparation [120]
- Rétablir la vision [121] et réparer les dommages à la cornée [122]
- Sclérose latérale amyotrophique [123]
- Maladie de Crohn [124]
- Cicatrisation [125]
- Infertilité masculine due à l’absence de cellules souches spermatogoniales. [126] Dans des études récentes, des scientifiques ont trouvé un moyen de résoudre ce problème en reprogrammant une cellule et en la transformant en spermatozoïde. D’autres études ont prouvé la restauration de la spermatogenèse en introduisant des cellules iPSC humaines dans des testicules de souris. Cela pourrait signifier la fin de l’ azoospermie . [127]
- Infertilité féminine : ovocytes fabriqués à partir de cellules souches embryonnaires. Les scientifiques ont découvert les cellules souches ovariennes, un type rare de cellules (0,014%) trouvées dans l’ovaire. Ils pourraient être utilisés comme traitement non seulement de l’infertilité, mais aussi de l’insuffisance ovarienne prématurée. [128]
Des recherches sont en cours pour développer diverses sources de cellules souches et pour appliquer des traitements à base de cellules souches aux maladies et affections neurodégénératives , au diabète , aux maladies cardiaques et à d’autres affections. [129] Des recherches sont également en cours pour générer des organoïdes à l’aide de cellules souches, ce qui permettrait de mieux comprendre le développement humain, l’ organogenèse et la modélisation des maladies humaines. [130]
Ces dernières années, avec la capacité des scientifiques à isoler et à cultiver des cellules souches embryonnaires , et avec la capacité croissante des scientifiques à créer des cellules souches en utilisant le transfert nucléaire de cellules somatiques et des techniques pour créer des cellules souches pluripotentes induites , la controverse s’est glissée, toutes deux liées à la politique de l’avortement et le clonage humain . [ citation nécessaire ]
L’hépatotoxicité et les lésions hépatiques d’origine médicamenteuse sont à l’origine d’un nombre important d’échecs de nouveaux médicaments en cours de développement et de retrait du marché, ce qui souligne la nécessité de tests de dépistage tels que les cellules de type hépatocyte dérivées de cellules souches, capables de détecter la toxicité tôt dans le médicament processus de développement . [131]
Des études notables
En août 2021, des chercheurs du Princess Margaret Cancer Center du University Health Network ont publié leur découverte d’un mécanisme de dormance dans les cellules souches clés qui pourrait aider à développer des traitements contre le cancer à l’avenir. [132]
Voir également
- Banque de cellules
- Génome humain
- Méristème
- Cellule souche mésenchymateuse
- Clonage partiel
- Cellule souche végétale
- Controverse sur les cellules souches
- Marqueur de cellules souches
Références
- ^ un b Atala A, Lanza R (2012). Manuel des cellules souches . Presse académique. p. 452. ISBN 978-0-12-385943-3.
- ^ Becker AJ, McCulloch EA, Jusqu’à JE (février 1963). “Démonstration cytologique de la nature clonale des colonies de rate dérivées de cellules de moelle de souris transplantées”. Nature . 197 (4866): 452–454. Bibcode : 1963Natur.197..452B . doi : 10.1038/197452a0 . manche : 1807/2779 . PMID 13970094 . S2CID 11106827 .
- ^ Siminovitch L, McCulloch EA, Jusqu’à JE (décembre 1963). “La distribution des cellules formant des colonies parmi les colonies de rate”. Journal de physiologie cellulaire et comparée . 62 (3): 327–336. doi : 10.1002/jcp.1030620313 . manche : 1807/2778 . PMID 14086156 . S2CID 43875977 .
- ^ Müller AM, Huppertz S, Henschler R (juillet 2016). « Cellules souches hématopoïétiques en médecine régénérative : égarées ou sur la bonne voie ? » . Médecine transfusionnelle et hémothérapie . 43 (4): 247–254. doi : 10.1159/000447748 . PMC 5040947 . PMID 27721700 .
- ^ Ralston, Michelle (17 juillet 2008). “Recherche sur les cellules souches dans le monde” . Projet sur la religion et la vie publique du Pew Research Center .
- ^ Tuch, BE (septembre 2006). « Cellules souches : une mise à jour clinique » . Médecin de famille australien . 35 (9): 719–721. PMID 16969445 . ProQuest 216301343 .
- ^ un b Ferreira L (2014-01-03). “Cellules souches : bref historique et perspectives” . Cellules souches : bref historique et perspectives – La science dans l’actualité . WordPress . Récupéré le 3 décembre 2019 .
- ^ un b Ramalho-Santos, Miguel; Willenbring, Holger (juin 2007). “Sur l’origine du terme ‘cellule souche’ “. Cell Stem Cell . 1 (1): 35–38. doi : 10.1016/j.stem.2007.05.013 . PMID 18371332 .
- ^ MacPherson C. “La découverte accidentelle de cellules souches” . USask Nouvelles . Université de la Saskatchewan . Récupéré le 3 décembre 2019 .
- ^ Accident du réacteur Vinca, 1958 Archivé le 27 janvier 2011 à la Wayback Machine , compilé par Wm. Robert Johnson
- ^ Boyle, Rebecca. Le loup brésilien blessé est le premier animal sauvage traité avec des cellules souches . Popular Science , 15 janvier 2011. Récupéré le 07/08/2021.
- ^ Tratamento . Conselho Federal de Medicina Veterinária, 2011-11-01, (portugais). Récupéré le 07/08/2021.
- ^ Shenghui, HE, Nakada, D., & Morrison, SJ (2009). Mécanismes d’auto-renouvellement des cellules souches. Revue annuelle de la cellule et du développement, 25, 377–406.
- ^ Cong YS, Wright WE, Shay JW (septembre 2002). « La télomérase humaine et sa régulation » . Examens de microbiologie et de biologie moléculaire . 66 (3) : 407-425, table des matières. doi : 10.1128/MMBR.66.3.407-425.2002 . PMC 120798 . PMID 12208997 .
- ^ un bcdef Schöler HR ( 2007 ). “Le potentiel des cellules souches : un inventaire”. Dans Nikolaus Knoepffler, Dagmar Schipanski, Stefan Lorenz Sorgner (dir.). La biotechnologie humaine comme défi social . Éditions Ashgate. p. 28. ISBN 978-0-7546-5755-2.
- ^ Mitalipov S, Loup D (2009). “Totipotence, pluripotence et reprogrammation nucléaire”. Ingénierie des cellules souches . Avancées en génie biochimique / biotechnologie. Vol. 114. pp. 185–199. Bibcode : 2009esc..book..185M . doi : 10.1007/10_2008_45 . ISBN 978-3-540-88805-5. PMC 2752493 . PMID 19343304 .
- ^ Ulloa-Montoya F, Verfaillie CM, Hu WS (juillet 2005). “Systèmes de culture de cellules souches pluripotentes” . Journal des biosciences et de la bioingénierie . 100 (1): 12–27. doi : 10.1263/jbb.100.12 . PMID 16233846 .
- ^ Friedenstein AJ, Deriglasova UF, Kulagina NN, Panasuk AF, Rudakowa SF, Luriá EA, Ruadkow IA (1974). “Précurseurs de fibroblastes dans différentes populations de cellules hématopoïétiques détectées par la méthode de dosage in vitro des colonies”. Hématologie expérimentale . 2 (2): 83–92. PMID 4455512 . INIST : PASCAL7536501060 NAID 10025700209 .
- ^ Friedenstein AJ, Gorskaja JF, Kulagina NN (septembre 1976). “Précurseurs de fibroblastes dans les organes hématopoïétiques de souris normaux et irradiés”. Hématologie expérimentale . 4 (5): 267-274. PMID 976387 .
- ^ Sekhar L, Bisht N (2006-09-01). “Thérapie par cellules souches”. Médecine d’Apollon . 3 (3): 271–276. doi : 10.1016/S0976-0016(11)60209-3 .
- ^ Thomson JA, Itskovitz-Eldor J, Shapiro SS, Waknitz MA, Swiergiel JJ, Marshall VS, Jones JM (novembre 1998). “Lignées de cellules souches embryonnaires dérivées de blastocystes humains” . Sciences . 282 (5391): 1145–1147. Bibcode : 1998Sci…282.1145T . doi : 10.1126/science.282.5391.1145 . PMID 9804556 .
- ^ un b Gilbert, Scott F. (2014). Biologie du développement . Associés Sinauer. ISBN 978-0-87893-978-7.[ page nécessaire ]
- ^ Rakic P (octobre 2009). « Évolution du néocortex : une perspective de la biologie du développement » . Revues naturelles. Neurosciences . 10 (10): 724–735. doi : 10.1038/nrn2719 . PMC 2913577 . PMID 19763105 .
- ^ Noctor SC, Flint AC, Weissman TA, Dammerman RS, Kriegstein AR (février 2001). “Les neurones dérivés des cellules gliales radiales établissent des unités radiales dans le néocortex”. Nature . 409 (6821): 714–720. Bibcode : 2001Natur.409..714N . doi : 10.1038/35055553 . PMID 11217860 . S2CID 3041502 .
- ^ Ying QL, Wray J, Nichols J, Batlle-Morera L, Doble B, Woodgett J, Cohen P, Smith A (mai 2008). “L’état fondamental de l’auto-renouvellement des cellules souches embryonnaires” . Nature . 453 (7194): 519-523. Bibcode : 2008Natur.453..519Y . doi : 10.1038/nature06968 . PMC 5328678 . PMID 18497825 .
- ^ “Culture de cellules souches embryonnaires humaines (hESC)” . Instituts nationaux de la santé. Archivé de l’original le 2010-01-06 . Récupéré le 07/03/2010 .
- ^ Chambers I, Colby D, Robertson M, Nichols J, Lee S, Tweedie S, Smith A (mai 2003). “Clonage d’expression fonctionnelle de Nanog, un facteur de maintien de la pluripotence dans les cellules souches embryonnaires”. Cellule . 113 (5): 643–655. doi : 10.1016/S0092-8674(03)00392-1 . manche : 1842/843 . PMID 12787505 . S2CID 2236779 .
- ^ Boyer LA, Lee TI, Cole MF, Johnstone SE, Levine SS, Zucker JP, Guenther MG, Kumar RM, Murray HL, Jenner RG, Gifford DK, Melton DA, Jaenisch R, Young RA (septembre 2005). “Circuits de régulation de la transcription de base dans les cellules souches embryonnaires humaines” . Cellule . 122 (6): 947–956. doi : 10.1016/j.cell.2005.08.020 . PMC 3006442 . PMID 16153702 .
- ^ Adewumi O, Aflatoonian B, Ahrlund-Richter L, Amit M, Andrews PW, Beighton G, et al. (L’Initiative internationale sur les cellules souches) (juillet 2007). “Caractérisation des lignées de cellules souches embryonnaires humaines par l’Initiative internationale sur les cellules souches”. Biotechnologie naturelle . 25 (7): 803–816. doi : 10.1038/nbt1318 . PMID 17572666 . S2CID 13780999 .
- ^ Mahla RS (2016). “Applications des cellules souches dans la médecine régénérative et la thérapeutique des maladies” . Journal international de biologie cellulaire . 2016 (7) : 1–24. doi : 10.1155/2016/6940283 . PMC 4969512 . PMID 27516776 .
- ^ Winslow R, Mundy A (23 janvier 2009). “Le premier essai de cellules souches embryonnaires obtient l’approbation de la FDA” . Le Wall StreetJournal .
- ^ “La thérapie par cellules souches embryonnaires à risque? Geron termine l’essai clinique” . ScienceDebate.com . Récupéré le 11/12/2011 .
- ^ Wu DC, Boyd AS, Wood KJ (mai 2007). “Transplantation de cellules souches embryonnaires : applicabilité potentielle dans la thérapie de remplacement cellulaire et la médecine régénérative”. Frontières en biosciences . 12 (8–12): 4525–35. doi : 10.2741/2407 . PMID 17485394 . S2CID 6355307 .
- ^ un b Zomer HD, Vidane AS, Gonçalves NN, Ambrósio CE (2015-09-28). “Cellules souches mésenchymateuses et pluripotentes induites : aperçus généraux et perspectives cliniques” . Cellules souches et clonage : avancées et applications . 8 : 125–134. doi : 10.2147/SCCAA.S88036 . PMC 4592031 . PMID 26451119 .
- ^ Caplan AI (septembre 1991). “Les cellules souches mésenchymateuses”. Journal de recherche orthopédique . 9 (5): 641–650. doi : 10.1002/jor.1100090504 . PMID 1870029 . S2CID 22606668 .
- ^ un bcdef Koledova Z, Krämer A, Kafkova LR, Divoky V (novembre 2010). “Régulation du cycle cellulaire dans les cellules souches embryonnaires: décisions centrosomales sur l’auto-renouvellement”. Cellules souches et développement . 19 (11): 1663-1678. doi : 10.1089/scd.2010.0136 . PMID 20594031 .
- ^ un bcd Barta T, Dolezalova D , Holubcova Z, Hampl A (mars 2013). “Régulation du cycle cellulaire dans les cellules souches embryonnaires humaines: liens avec l’adaptation à la culture cellulaire”. Biologie expérimentale et médecine . 238 (3): 271–275. doi : 10.1177/1535370213480711 . PMID 23598972 . S2CID 2028793 .
- ^ un bcdefg Zaveri L , Dhawan J ( 2018 ). “Faire du vélo pour rencontrer le destin: connecter la pluripotence au cycle cellulaire” . Frontières en biologie cellulaire et développementale . 6 : 57. doi : 10.3389/fcell.2018.00057 . PMC 6020794 . PMID 29974052 .
- ^ Koledova Z, Kafkova LR, Calabkova L, Krystof V, Dolezel P, Divoky V (février 2010). “L’inhibition de Cdk2 prolonge la progression de la phase G1 dans les cellules souches embryonnaires de souris”. Cellules souches et développement . 19 (2): 181–194. doi : 10.1089/scd.2009.0065 . PMID 19737069 .
- ^ Becker KA, Ghule PN, Therrien JA, Lian JB, Stein JL, van Wijnen AJ, Stein GS (décembre 2006). “L’auto-renouvellement des cellules souches embryonnaires humaines est soutenu par une phase de cycle cellulaire G1 raccourcie”. Tourillon de physiologie cellulaire . 209 (3): 883–893. doi : 10.1002/jcp.20776 . PMID 16972248 . S2CID 24908771 .
- ^ Ariff Bongso; Eng Hin Lee, éd. (2005). « Cellules souches : leur définition, leur classification et leurs sources ». Cellules souches : de la paillasse au chevet . Scientifique mondial. p. 5 . ISBN 978-981-256-126-8. OCLC 443407924 .
- ^ Moore, Keith L.; Persaud, TVN; Torchia, Mark G. (2013). Avant notre naissance : éléments essentiels de l’embryologie et des malformations congénitales . Saunders/Elsevier. ISBN 978-1-4377-2001-3.[ page nécessaire ]
- ^ “Qu’est-ce qu’une cellule souche” . anthonynolan.org . Antoine Nolan . Récupéré le 17 février 2022 .
- ^ Jiang Y, Jahagirdar BN, Reinhardt RL, Schwartz RE, Keene CD, Ortiz-Gonzalez XR, Reyes M, Lenvik T, Lund T, Blackstad M, Du J, Aldrich S, Lisberg A, Low WC, Largaespada DA, Verfaillie CM (juillet 2002). « Pluripotence des cellules souches mésenchymateuses dérivées de la moelle adulte » . Nature . 418 (6893): 41–49. Bibcode : 2002Natur.418…41J . doi : 10.1038/nature00870 . PMID 12077603 . S2CID 47162269 .
- ^ “Don de moelle osseuse (cellules souches): Encyclopédie médicale MedlinePlus” . medlineplus.gov . Récupéré le 17/10/2021 .
- ^ Coughlin RP, Oldweiler A, Mickelson DT, Moorman CT (octobre 2017). “Technique de greffe de cellules souches dérivées du tissu adipeux pour les maladies articulaires dégénératives” . Techniques d’arthroscopie . 6 (5) : e1761–e1766. doi : 10.1016/j.eats.2017.06.048 . PMC 5795060 . PMID 29399463 .
- ^ Ratajczak MZ, Machalinski B, Wojakowski W, Ratajczak J, Kucia M (mai 2007). “Une hypothèse pour une origine embryonnaire des cellules souches pluripotentes Oct-4(+) dans la moelle osseuse adulte et d’autres tissus” . Leucémie . 21 (5): 860–867. doi : 10.1038/sj.leu.2404630 . PMID 17344915 .
- ^ Narasipura SD, Wojciechowski JC, Charles N, Liesveld JL, King MR (janvier 2008). “Microtube revêtu de P-sélectine pour l’enrichissement des cellules souches et progénitrices hématopoïétiques CD34 + de la moelle osseuse humaine” . Chimie clinique . 54 (1): 77–85. doi : 10.1373/clinchem.2007.089896 . PMID 18024531 .
- ^ Terai S, Ishikawa T, Omori K, Aoyama K, Marumoto Y, Urata Y, Yokoyama Y, Uchida K, Yamasaki T, Fujii Y, Okita K, Sakaida I (octobre 2006). “Fonction hépatique améliorée chez les patients atteints de cirrhose du foie après une thérapie par perfusion de cellules de moelle osseuse autologue”. Cellules souches . 24 (10): 2292–2298. doi : 10.1634/stemcells.2005-0542 . PMID 16778155 . S2CID 5649484 .
- ^ Subrammaniyan R, Amalorpavanathan J, Shankar R, Rajkumar M, Baskar S, Manjunath SR, Senthilkumar R, Murugan P, Srinivasan VR, Abraham S (septembre 2011). “Application de cellules mononucléaires de moelle osseuse autologues chez six patients atteints d’ischémie critique chronique avancée des membres à la suite d’un diabète : notre expérience”. Cytothérapie . 13 (8): 993–999. doi : 10.3109/14653249.2011.579961 . PMID 21671823 . S2CID 27251276 .
- ^ Madhusankar N (2007). “Utilisation de cellules souches dérivées de la moelle osseuse chez les patients atteints de troubles cardiovasculaires” . Journal des cellules souches et médecine régénérative . 3 (1) : 28-29. PMC 3908115 . PMID 24693021 .
- ^ Dedeepiya VD, Rao YY, Jayakrishnan GA, Parthiban JK, Baskar S, Manjunath SR, Senthilkumar R, Abraham SJ (2012). “Indice des cellules CD34 + et des cellules mononucléaires dans la moelle osseuse des patients atteints de lésions de la moelle épinière de différents groupes d’âge : une analyse comparative” . Recherche sur la moelle osseuse . 2012 : 1–8. doi : 10.1155/2012/787414 . PMC 3398573 . PMID 22830032 .
- ^ Gardner RL (mars 2002). « Cellules souches : puissance, plasticité et perception du public » . Revue d’Anatomie . 200 (Partie 3): 277–282. doi : 10.1046/j.1469-7580.2002.00029.x . PMC 1570679 . PMID 12033732 .
- ^ Behrens A, van Deursen JM, Rudolph KL, Schumacher B (mars 2014). “Impact des dommages génomiques et du vieillissement sur la fonction des cellules souches” . Biologie Cellulaire Nature . 16 (3): 201–207. doi : 10.1038/ncb2928 . PMC 4214082 . PMID 24576896 .
- ^ Barrilleaux B, Phinney DG, Prockop DJ, O’Connor KC (novembre 2006). « Bilan : ingénierie ex vivo de tissus vivants avec des cellules souches adultes ». Ingénierie tissulaire . 12 (11): 3007–3019. CiteSeerX 10.1.1.328.2873 . doi : 10.1089/ten.2006.12.3007 . PMID 17518617 .
- ^ Gimble JM, Katz AJ, Bunnell BA (mai 2007). “Cellules souches adipeuses pour la médecine régénérative” . Recherche sur la diffusion . 100 (9) : 1249-1260. doi : 10.1161/01.RES.0000265074.83288.09 . PMC 5679280 . PMID 17495232 .
- ^ Kuroda Y, Kitada M, Wakao S, Nishikawa K, Tanimura Y, Makinoshima H, Goda M, Akashi H, Inutsuka A, Niwa A, Shigemoto T, Nabeshima Y, Nakahata T, Nabeshima Y, Fujiyoshi Y, Dezawa M (mai 2010). “Cellules multipotentes uniques dans les populations de cellules mésenchymateuses humaines adultes” . Actes de l’Académie nationale des sciences des États-Unis d’Amérique . 107 (19): 8639–8643. Bibcode : 2010PNAS..107.8639K . doi : 10.1073/pnas.0911647107 . PMC 2889306 . PMID 20421459 .
- ^ “Greffe de moelle osseuse” . ucsfchildrenshospital.org .
- ^ Kane, Ed (2008-05-01). “La thérapie par cellules souches est prometteuse pour les blessures des tissus mous du cheval, la maladie” . DVM Newsmagazine . Récupéré le 12/06/2008 .
- ^ “FAQ sur les cellules souches” . Département américain de la santé et des services sociaux. 2004-07-14. Archivé de l’original le 09/01/2009.
- ^ Oliveira PH, da Silva CL, Cabral JM (2014). “Instabilité génomique dans les cellules souches humaines : situation actuelle et défis futurs”. Cellules souches . 32 (11): 2824–2832. doi : 10.1002/stem.1796 . PMID 25078438 . S2CID 41335566 .
- ^ De Coppi P, Bartsch G, Siddiqui MM, Xu T, Santos CC, Perin L, Mostoslavsky G, Serre AC, Snyder EY, Yoo JJ, Furth ME, Soker S, Atala A (janvier 2007). “Isolement des lignées de cellules souches amniotiques avec un potentiel de thérapie”. Biotechnologie naturelle . 25 (1): 100–106. doi : 10.1038/nbt1274 . PMID 17206138 . S2CID 6676167 .
- ^ “Le journal du Vatican appelle la nouvelle source de cellules souches” l’avenir de la médecine ” ” . Agence de presse catholique . 3 février 2010.
- ^ “European Biotech Company Biocell Center ouvre la première installation américaine pour la préservation des cellules souches amniotiques à Medford, Massachusetts” . Reuters . 2009-10-22. Archivé de l’original le 2009-10-30 . Récupéré le 14/03/2010 .
- ^ “Le Centre Biocell d’Europe ouvre le bureau de Medford – Mise à jour quotidienne des affaires” . Le BostonGlobe . 2009-10-22 . Récupéré le 14/03/2010 .
- ^ “Le téléscripteur” . BostonHerald.com. 2009-10-22 . Récupéré le 14/03/2010 .
- ^ “Biocell Center ouvre une banque de cellules souches amniotiques à Medford” . Nouvelles d’affaires de masse de haute technologie . 2009-10-23. Archivé de l’original le 14/10/2012 . Récupéré le 26/08/2012 .
- ^ “La première banque de cellules souches amniotiques au monde s’ouvre à Medford” . wbur.org . Récupéré le 14/03/2010 .
- ^ “Biocell Center Corporation s’associe au plus grand réseau hospitalier communautaire de la Nouvelle-Angleterre pour offrir un unique …” Medford, Mass.: Prnewswire.com . Récupéré le 14/03/2010 .
- ^ un bc ” Fabriquer des cellules souches embryonnaires humaines” . L’Économiste . 2007-11-22.
- ^ Marque M, Palca J, Cohen A (2007-11-20). “Les cellules de la peau peuvent devenir des cellules souches embryonnaires” . Radio Publique Nationale .
- ^ “Breakthrough Set pour changer radicalement le débat sur les cellules souches” . L’heure de l’actualité avec Jim Lehrer . 2007-11-20.
- ^ un bcde Kimbrel EA , Lanza R (décembre 2016). “Cellules souches pluripotentes : les 10 dernières années” . Médecine régénérative . 11 (8): 831–847. doi : 10.2217/rme-2016-0117 . PMID 27908220 .
- ^ un bc Takahashi K, Yamanaka S (août 2006). “Induction de cellules souches pluripotentes à partir de cultures de fibroblastes embryonnaires et adultes de souris par des facteurs définis”. Cellule . 126 (4): 663–676. doi : 10.1016/j.cell.2006.07.024 . hdl : 2433/159777 . PMID 16904174 . S2CID 1565219 .
- ^ Takahashi K, Tanabe K, Ohnuki M, Narita M, Ichisaka T, Tomoda K, Yamanaka S (novembre 2007). “Induction de cellules souches pluripotentes à partir de fibroblastes humains adultes par des facteurs définis”. Cellule . 131 (5): 861–872. doi : 10.1016/j.cell.2007.11.019 . hdl : 2433/49782 . PMID 18035408 . S2CID 8531539 .
- ^ Yu J, Vodyanik MA, Smuga-Otto K, Antosiewicz-Bourget J, Frane JL, Tian S, Nie J, Jonsdottir GA, Ruotti V, Stewart R, Slukvin II, Thomson JA (décembre 2007). “Lignées de cellules souches pluripotentes induites dérivées de cellules somatiques humaines”. Sciences . 318 (5858): 1917–1920. Bibcode : 2007Sci…318.1917Y . doi : 10.1126/science.1151526 . PMID 18029452 . S2CID 86129154 .
- ^ “Son inspiration vient de la recherche du professeur Shinya Yamanaka à l’Université de Kyoto , qui suggère un moyen de créer des cellules souches embryonnaires humaines sans avoir besoin d’ovules humains, qui sont extrêmement rares, et sans avoir besoin de créer et de détruire des clones humains embryons, auquel s’oppose farouchement le mouvement pro-vie.” Highfield R (2007-11-16). “Le créateur de Dolly, le professeur Ian Wilmut, évite le clonage” . Le Télégraphe . Londres. Archivé de l’original le 2009-07-30.
- ^ Maldonado M, Luu RJ, Ico G, Ospina A, Myung D, Shih HP, Nam J (septembre 2017). “Mécanomodulation spécifique à la lignée et au stade de développement de la différenciation induite des cellules souches pluripotentes” . Recherche et thérapie sur les cellules souches . 8 (1): 216. doi : 10.1186/s13287-017-0667-2 . PMC 5622562 . PMID 28962663 .
- ^ un b Robinton DA, Daley GQ (janvier 2012). “La promesse des cellules souches pluripotentes induites dans la recherche et la thérapie” . Nature . 481 (7381): 295–305. Bibcode : 2012Natur.481..295R . doi : 10.1038/nature10761 . PMC 3652331 . PMID 22258608 .
- ^ Staerk J, Dawlaty MM, Gao Q, Maetzel D, Hanna J, Sommer CA, Mostoslavsky G, Jaenisch R (juillet 2010). “Reprogrammation des cellules sanguines périphériques humaines en cellules souches pluripotentes induites” . Cellule Cellule Souches . 7 (1): 20–24. doi : 10.1016/j.stem.2010.06.002 . PMC 2917234 . PMID 20621045 . Résumé profane – ScienceDaily . {{cite journal}}: Cite utilise un paramètre obsolète |lay-url=( aide )
- ^ Chen X, Hartman A, Guo S (2015-09-01). “Choisir le destin cellulaire à travers un cycle cellulaire dynamique” . Rapports actuels sur les cellules souches . 1 (3): 129–138. doi : 10.1007/s40778-015-0018-0 . PMC 5487535 . PMID 28725536 .
- ^ Hindley C, Philpott A (avril 2013). “Le cycle cellulaire et la pluripotence” . Le Journal biochimique . 451 (2): 135–143. doi : 10.1042/BJ20121627 . PMC 3631102 . PMID 23535166 .
- ^ Renard, DT; Morris, LX; Nystul, T.; Spradling, AC (2008). « Analyse de la lignée des cellules souches » . StemBook . doi : 10.3824/stembook.1.33.1 . PMID 20614627 .
- ^ Beckmann, Julia; Scheitza, Sébastien; Wernet, Pierre; Fischer, Johannes C.; Giebel, Bernd (15 juin 2007). “Division cellulaire asymétrique dans le compartiment des cellules souches et progénitrices hématopoïétiques humaines : identification des protéines à ségrégation asymétrique” . Sang . 109 (12): 5494–5501. doi : 10.1182/blood-2006-11-055921 . PMID 17332245 .
- ^ Xie, Ting; Spradling, Allan C (juillet 1998). “Le décapentaplégique est essentiel pour le maintien et la division des cellules souches germinales dans l’ovaire de drosophile” . Cellule . 94 (2): 251–260. doi : 10.1016/s0092-8674(00)81424-5 . PMID 9695953 . S2CID 11347213 .
- ^ Chanson, X.; Zhu, CH; Doan, C; Xie, T (7 juin 2002). “Cellules souches germinales ancrées par des jonctions adhérentes dans les niches ovariennes de la drosophile”. Sciences . 296 (5574): 1855–1857. Bib code : 2002Sci …296.1855S . doi : 10.1126/science.1069871 . PMID 12052957 . S2CID 25830121 .
- ^ Ian Murnaghan pour Explorer les cellules souches. Mise à jour : 16 décembre 2013 Pourquoi effectuer une greffe de cellules souches ?
- ^ Greffe de moelle osseuse et greffe de cellules souches du sang périphérique sur le site Web de la fiche d’information de l’Institut national du cancer. Bethesda, MD : National Institutes of Health, US Department of Health and Human Services, 2010. Cité le 24 août 2010
- ^ Stamm C, Westphal B, Kleine HD, Petzsch M, Kittner C, Klinge H, et al. (janvier 2003). “Transplantation autologue de cellules souches de moelle osseuse pour la régénération myocardique”. Lancette . 361 (9351): 45–46. doi : 10.1016/S0140-6736(03)12110-1 . PMID 12517467 . S2CID 23858666 .
- ^ Maître Z, McLeod M, Mendez I (mars 2007). “Avantages, risques et considérations éthiques dans la traduction de la recherche sur les cellules souches en applications cliniques dans la maladie de Parkinson” . Journal d’éthique médicale . 33 (3): 169-173. doi : 10.1136/jme.2005.013169 . JSTOR 27719821 . PMC 2598267 . PMID 17329391 .
- ^ “Cours de formation complet sur les cellules souches” . Formation médicale R3 . Récupéré le 15/05/2021 .
- ^ Moore KL, Persaud TV, Torchia MG (2013). Avant notre naissance : éléments essentiels de l’embryologie et des malformations congénitales . Philadelphie, Pennsylvanie : Saunders, Elsevier.
- ^ Bernadine Healy, MD. “Pourquoi les cellules souches embryonnaires sont obsolètes” US News et rapport mondial . Consulté le 17 août 2015.
- ^ “Les cellules souches fœtales provoquent une tumeur chez un adolescent” .
- ^ Lo, Bernard; Parham, Lindsay (mai 2009). “Problèmes éthiques dans la recherche sur les cellules souches” . Examens endocriniens . NIH. 30 (3): 204-213. doi : 10.1210/er.2008-0031 . PMC 2726839 . PMID 19366754 .
- ^ Bauer, G; Elsallab, M; Abou-El-Enein, M (septembre 2018). “Examen concis : une analyse complète des événements indésirables signalés chez les patients recevant des interventions à base de cellules souches non prouvées” . Médecine translationnelle des cellules souches . 7 (9): 676–685. doi : 10.1002/sctm.17-0282 . PMC 6127222 . PMID 30063299 .
- ^ Blackwell, Tom (2016-07-13). “Une étude révèle une explosion de traitements non prouvés à base de cellules souches aux États-Unis – et de nombreux Canadiens les recherchent” . Poste nationale . Récupéré le 22/03/2022 .
- ^ un b Berkowitz, Aaron L.; Miller, Michael B.; Mir, Saad A.; Cagney, Daniel; Chavakula, Vamsidhar ; Guléria, Indira; Aizer, Ayal ; Ligon, Keith L.; Chi, John H. (14 juillet 2016). « Lésion glioproliférative de la moelle épinière comme complication du « tourisme des cellules souches » “. New England Journal of Medicine . 375 (2): 196–198. doi : 10.1056/NEJMc1600188 . PMID 27331440 .
- ^ Bowman, Michelle; Racke, Michael; Kissel, John; Imitola, Jaime (1er novembre 2015). “Responsabilités des professionnels de la santé dans le conseil et l’éducation des patients atteints de maladies neurologiques incurables concernant le” tourisme des cellules souches “: Caveat Emptor”. JAMA Neurologie . 72 (11): 1342–1345. doi : 10.1001/jamaneurol.2015.1891 . PMID 26322563 .
- ^ “Communication sur les traitements de cellules souches non prouvés au public” .
- ^ Tsou, Amy (février 2015). “Considérations éthiques lors du conseil aux patients sur le tourisme des cellules souches”. Continuum : Apprentissage continu en neurologie . 21 (1 Troubles de la moelle épinière) : 201–205. doi : 10.1212/01.CON.0000461094.76563.be . PMID 25651226 .
- ^ Du, Li; Rachul, Christen ; Guo, Zhaochen ; Caulfield, Timothy (9 mars 2016). “Le “traitement miraculeux” de Gordie Howe : étude de cas sur les réactions des utilisateurs de Twitter au traitement des cellules souches d’une célébrité sportive” . Santé publique et surveillance du JMIR . 2 (1) : e8. doi : 10.2196/publichealth.5264 . PMC 4869214 . PMID 27227162 .
- ^ un Regalado b , Antonio, David P. Hamilton (juillet 2006). “Comment les brevets d’une université peuvent limiter le chercheur sur les cellules souches.” Le Wall StreetJournal . Consulté le 24 juillet 2006.
- ^ Stephen Jenei pour Patent Baristas, 3 avril 2007 Les brevets sur les cellules souches WARF ont été renversés au premier tour
- ^ Stephen Jenei pour Patent Baristas, 3 mars 2008 Ding! WARF remporte le Round 2 alors que le brevet sur les cellules souches est confirmé
- ^ Constance Holden pour Science Now. 12 mars 2008 WARF va 3 pour 3 sur les brevets
- ^ Stephen G. Kunin pour les brevets après la subvention. 10 mai 2010 BPAI rejette les demandes de brevet WARF sur les cellules souches dans le cadre d’un appel de réexamen inter partes
- ^ Bureau des brevets et des marques des États-Unis. Commission des recours et des ingérences en matière de brevets. La Fondation pour les droits des contribuables et des consommateurs, demandeur et appelant V. Patent Of Wisconsin Alumni Research Foundation, propriétaire du brevet et intimé. Appel 2012-011693, contrôle de réexamen 95/000,154. Brevet 7 029 913 Décision en appel Archivée le 20/02/2013 à la Wayback Machine
- ^ Personnel de GenomeWeb, 03 juillet 2013 Consumer Watchdog, PPF Seek Invalidation of Stem Cell Patent de WARF
- ^ Antoinette Konski pour le Bulletin de médecine personnalisée. 3 février 2014 Le gouvernement américain et l’USPTO exhortent le circuit fédéral à rejeter l’appel sur les cellules souches
- ^ a bcd Bases sur les cellules souches : quelles sont les utilisations potentielles des cellules souches humaines et les obstacles qui doivent être surmontés avant que ces utilisations potentielles ne soient réalisées ? . Dans le site Web d’information sur les cellules souches. Bethesda, MD : National Institutes of Health, US Department of Health and Human Services, 2009. cité le dimanche 26 avril 2009
- ^ “Traitement de la perte de cheveux avec la thérapie par cellules souches et PRP” . Cellules souches LA . 2019-02-20 . Récupéré le 30/05/2020 .
- ^ Gentil, Pietro; Garcovich, Simone; Bielli, Alessandra; Scioli, Maria Giovanna; Orlandi, Augusto; Cervelli, Valerio (novembre 2015). “L’effet du plasma riche en plaquettes sur la repousse des cheveux : un essai randomisé contrôlé par placebo” . Médecine translationnelle des cellules souches . 4 (11): 1317–1323. doi : 10.5966/sctm.2015-0107 . ISSN 2157-6564 . PMC 4622412 . PMID 26400925 .
- ^ un b Steinberg, Douglas (le 26 novembre 2000). “Cellules souches exploitées pour reconstituer les organes” . Le Magazine Scientifique .
- ^ ISRAEL21c: Des scientifiques israéliens inversent les anomalies congénitales du cerveau à l’aide de cellules souches, 25 décembre 2008. (Chercheurs de l’Université hébraïque de Jérusalem-Hadassah Medical dirigés par le professeur Joseph Yanai )
- ^ Kang KS, Kim SW, Oh YH, Yu JW, Kim KY, Park HK, Song CH, Han H (2005). “Une patiente de 37 ans blessée à la moelle épinière, transplantée de cellules souches multipotentes à partir de sang humain UC, avec une perception sensorielle et une mobilité améliorées, à la fois fonctionnellement et morphologiquement : une étude de cas”. Cytothérapie . 7 (4): 368–373. doi : 10.1080/14653240500238160 . PMID 16162459 . S2CID 33471639 .
- ^ Strauer BE, Schannwell CM, Brehm M (avril 2009). “Potentiels thérapeutiques des cellules souches dans les maladies cardiaques”. Minerva Cardioangiologica . 57 (2): 249–267. PMID 19274033 .
- ^ DeNoon, Daniel J. (4 novembre 2004). “Le clonage des cheveux se rapproche de la réalité en tant que remède contre la calvitie” . WebMD .
- ^ Yen AH, Sharpe PT (janvier 2008). “Cellules souches et ingénierie des tissus dentaires”. Recherche sur les cellules et les tissus . 331 (1): 359–372. doi : 10.1007/s00441-007-0467-6 . PMID 17938970 . S2CID 23765276 .
- ^ “La thérapie génique est le premier ‘remède’ contre la surdité ” . New Scientist . 14 février 2005.
- ^ “Cellules souches utilisées pour restaurer la vision” . Nouvelles de la BBC . 2005-04-28.
- ^ Hanson C, Hardarson T, Ellerström C, Nordberg M, Caisander G, Rao M, Hyllner J, Stenevi U (mars 2013). “Transplantation de cellules souches embryonnaires humaines sur une cornée humaine partiellement blessée in vitro” . Acta Ophthalmologica . 91 (2): 127–130. doi : 10.1111/j.1755-3768.2011.02358.x . PMC 3660785 . PMID 22280565 .
- ^ Vastag B (avril 2001). “Les cellules souches se rapprochent de la clinique : paralysie partiellement inversée chez les rats atteints d’une maladie semblable à la SLA”. JAMA . 285 (13): 1691–1693. doi : 10.1001/jama.285.13.1691 . PMID 11277806 .
- ^ Anderson, Querida (15 juin 2008). « Osiris trompe son produit de cellules souches adultes » . Nouvelles du génie génétique et de la biotechnologie . 28 (12).
- ^ Gurtner, Geoffrey C.; Callaghan, Matthew J.; Longaker, Michael T. (février 2007). “Progrès et potentiel pour la médecine régénérative”. Revue annuelle de médecine . 58 (1): 299–312. doi : 10.1146/annurev.med.58.082405.095329 . PMID 17076602 .
- ^ Hanna V, Gassei K, Orwig KE (2015). “Thérapies par cellules souches pour l’infertilité masculine : où en sommes-nous maintenant et où allons-nous ?”. Dans Carrell D, Schlegel P, Racowsky C, Gianaroli L (eds.). Revue biennale de l’infertilité . p. 17–39. doi : 10.1007/978-3-319-17849-3_3 . ISBN 978-3-319-17849-3.La greffe de moelle osseuse est, depuis 2009, la seule utilisation établie des cellules souches.
- ^ Valli H, Phillips BT, Shetty G, Byrne JA, Clark AT, Meistrich ML, Orwig KE (janvier 2014). « Cellules souches germinales : vers la régénération de la spermatogenèse » . Fertilité et stérilité . 101 (1): 3–13. doi : 10.1016/j.fertnstert.2013.10.052 . PMC 3880407 . PMID 24314923 .
- ^ White YA, Woods DC, Takai Y, Ishihara O, Seki H, Tilly JL (février 2012). “Formation d’ovocytes par des cellules germinales mitotiquement actives purifiées à partir d’ovaires de femmes en âge de procréer” . Médecine naturelle . 18 (3): 413–421. doi : 10.1038/nm.2669 . PMC 3296965 . PMID 22366948 .
- ^ Bubela T , Li MD, Hafez M, Bieber M, Atkins H (novembre 2012). « La croyance est-elle plus grande que la réalité : attentes, optimisme et réalité pour la recherche translationnelle sur les cellules souches » . Médecine BMC . 10 : 133. doi : 10.1186/1741-7015-10-133 . PMC 3520764 . PMID 23131007 .
- ^ Ader M, Tanaka EM (décembre 2014). “Modélisation du développement humain dans la culture 3D”. Opinion actuelle en biologie cellulaire . 31 : 23–28. doi : 10.1016/j.ceb.2014.06.013 . PMID 25033469 .
- ^ Greenhough, Sébastien; Hay, David C. (avril 2012). “Criblage de toxicité basé sur les cellules souches : avancées récentes dans la génération d’hépatocytes”. Médecine pharmaceutique . 26 (2): 85–89. doi : 10.1007/BF03256896 . S2CID 15893493 .
- ^ García-Prat, Laura; Kaufmann, Kerstin B.; Schneiter, Florin; Voisin, Véronique; Murison, Alex; Chen, Jocelyne; Chan-Seng-Yue, Michelle ; Gan, Olga I.; McLeod, Jessica L.; Smith, Sabrina A.; Shoong, Michelle C.; Parris, Darrien; Pan, Kristele ; Zeng, Andy GX ; Krivdova, Gabriela; Gupta, Kinam ; Takayanagi, Shin-Ichiro; Wagenblast, Elvin; Wang, Weijia ; Lupien, Mathieu; Schroeder, Timm; Xie, Stéphanie Z.; Dick, John E. (août 2021). “L’activité endolysosomale médiée par le TFEB contrôle le destin des cellules souches hématopoïétiques humaines”. Cellule Cellule Souches . 28 (10): 1838–1850.e10. doi : 10.1016/j.stem.2021.07.003 . PMID 34343492 . S2CID 236915618 .
Lectures complémentaires
- Manzo, Carlo; Torreno-Pina, Juan A.; Massignan, Pietro; Lapeyre, Gérald J.; Lewenstein, Maciej; Garcia Parajo, Maria F. (25 février 2015). “Rupture d’ergodicité faible du mouvement des récepteurs dans les cellules vivantes provenant de la diffusivité aléatoire”. Examen physique X . 5 (1) : 011021. arXiv : 1407.2552 . Bibcode : 2015PhRvX…5a1021M . doi : 10.1103/PhysRevX.5.011021 . S2CID 73582473 .
Liens externes
| Wikimedia Commons a des médias liés aux cellules souches . |
- Instituts nationaux de la santé : informations sur les cellules souches
- Nature.com : Cellules souches