Cancer colorectal
Le cancer colorectal ( CCR ), également connu sous le nom de cancer de l’intestin , cancer du côlon ou cancer du rectum , est le développement d’ un cancer du côlon ou du rectum (parties du gros intestin ). [6] Les signes et symptômes peuvent inclure du sang dans les selles , une modification des selles , une perte de poids et de la fatigue. [1]
| Cancer colorectal | |
|---|---|
| Autres noms | Cancer du côlon, cancer du rectum, cancer de l’intestin |
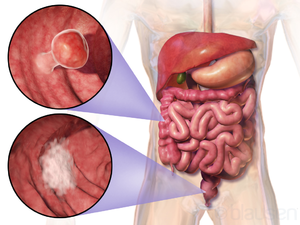 |
|
| Localisation et apparence de deux exemples de tumeurs colorectales | |
| Spécialité | Gastro- entérologie Chirurgie générale Oncologie |
| Les symptômes | Vomissements de sang , sang dans les selles , modification des selles, perte de poids , fatigue [1] |
| causes | Vieillesse, facteurs liés au mode de vie et maladies génétiques [2] [3] |
| Facteurs de risque | Alimentation, obésité , tabagisme, manque d’ activité physique , consommation d’alcool [2] [4] |
| Méthode diagnostique | Biopsie tissulaire lors d’une sigmoïdoscopie ou d’ une coloscopie [1] |
| La prévention | Dépistage de 50 à 75 ans [5] |
| Traitement | Chirurgie, radiothérapie , chimiothérapie , thérapie ciblée [6] |
| Pronostic | Taux de survie à cinq ans 65 % (États-Unis) [7] |
| La fréquence | 9,4 millions (2015) [8] |
| Décès | 551 000 (2018) [9] |
La plupart des cancers colorectaux sont dus à des facteurs liés à l’âge et au mode de vie, avec seulement un petit nombre de cas dus à des troubles génétiques sous-jacents. [2] [3] Les facteurs de risque comprennent l’alimentation, l’obésité , le tabagisme et le manque d’ activité physique . [2] Les facteurs alimentaires qui augmentent le risque comprennent la viande rouge , la viande transformée et l’alcool. [2] [4] Un autre facteur de risque est la maladie intestinale inflammatoire , qui comprend la maladie de Crohn et la colite ulcéreuse . [2] Certaines des maladies génétiques héréditaires pouvant causer le cancer colorectal comprennentpolypose adénomateuse familiale et cancer du côlon héréditaire sans polypose ; cependant, ceux-ci représentent moins de 5 % des cas. [2] [3] Cela commence généralement par une tumeur bénigne , souvent sous la forme d’un polype , qui au fil du temps devient cancéreuse . [2]
Le cancer de l’intestin peut être diagnostiqué en obtenant un échantillon du côlon au cours d’une sigmoïdoscopie ou d’ une coloscopie . [1] Ceci est ensuite suivi d’ une imagerie médicale pour déterminer si la maladie s’est propagée. [6] Le dépistage est efficace pour prévenir et diminuer les décès dus au cancer colorectal. [5] Le dépistage, par l’une des nombreuses méthodes, est recommandé à partir de l’âge de 50 à 75 ans. [5] Au cours de la coloscopie, de petits polypes peuvent être retirés s’ils sont trouvés. [2] Si un gros polype ou une tumeur est découvert, une biopsie peut être effectuée pour vérifier s’il est cancéreux. Aspirine et autreles anti-inflammatoires non stéroïdiens diminuent le risque. [2] [10] Leur utilisation générale n’est cependant pas recommandée à cette fin, en raison d’effets secondaires. [11]
Les traitements utilisés pour le cancer colorectal peuvent inclure une combinaison de chirurgie, de radiothérapie , de chimiothérapie et de thérapie ciblée . [6] Les cancers qui sont confinés dans la paroi du côlon peuvent être guéris par chirurgie, tandis que les cancers qui se sont largement propagés ne sont généralement pas guérissables, la prise en charge étant orientée vers l’amélioration de la qualité de vie et des symptômes. [6] Le taux de survie à cinq ans aux États-Unis est d’environ 65 %. [7] La probabilité individuelle de survie dépend de l’état d’avancement du cancer, du fait que tout le cancer peut ou non être enlevé par chirurgie et de l’état de santé général de la personne. [1]À l’échelle mondiale, le cancer colorectal est le troisième type de cancer le plus courant, représentant environ 10 % de tous les cas. [12] En 2018, il y a eu 1,09 million de nouveaux cas et 551 000 décès dus à la maladie. [9] Elle est plus fréquente dans les pays développés , où l’on retrouve plus de 65 % des cas. [2] Il est moins fréquent chez les femmes que chez les hommes. [2]
Signes et symptômes
Les signes et les symptômes du cancer colorectal dépendent de l’emplacement de la tumeur dans l’ intestin et de sa propagation ailleurs dans le corps ( métastase ). Les signes avant-coureurs classiques incluent : aggravation de la constipation , présence de sang dans les selles, diminution du calibre (épaisseur) des selles, perte d’appétit, perte de poids et nausées ou vomissements chez une personne de plus de 50 ans. [13] Environ 50 % des personnes atteintes d’un cancer colorectal ne signalent aucun symptôme. [14]
Les saignements rectaux ou l’anémie sont des symptômes à haut risque chez les personnes de plus de 50 ans. [15] La perte de poids et les changements dans les habitudes intestinales d’une personne ne sont généralement préoccupants que s’ils sont associés à des saignements rectaux. [15] [16]
Cause
75 à 95 % des cas de cancer colorectal surviennent chez des personnes présentant peu ou pas de risque génétique. [17] [18] Les facteurs de risque comprennent l’âge avancé, le sexe masculin, [18] une consommation élevée de graisses, de sucre , d’alcool , de viande rouge , de viandes transformées , d’ obésité , de tabagisme et d’un manque d’ exercice physique . [17] [19] Environ 10 % des cas sont liés à une activité insuffisante. [20] Le risque lié à l’alcool semble augmenter à plus d’un verre par jour. [21]Boire 5 verres d’eau par jour est lié à une diminution du risque de cancer colorectal et de polypes adénomateux. [22] Streptococcus gallolyticus est associé au cancer colorectal. [23] Certaines souches du complexe Streptococcus bovis/Streptococcus equinus sont consommées quotidiennement par des millions de personnes et peuvent donc être sans danger. [24] 25 à 80 % des personnes atteintes de bactériémie à Streptococcus bovis/gallolyticus ont des tumeurs colorectales concomitantes. [25] La séroprévalence de Streptococcus bovis/gallolyticus est considérée comme un marqueur pratique candidat pour la prédiction précoce d’une lésion intestinale sous-jacente dans une population à haut risque. [25]Il a été suggéré que la présence d’anticorps dirigés contre les antigènes de Streptococcus bovis/gallolyticus ou les antigènes eux-mêmes dans la circulation sanguine peuvent agir comme marqueurs de la carcinogenèse dans le côlon. [25]
L’ Escherichia coli pathogène peut augmenter le risque de cancer colorectal en produisant le métabolite génotoxique , la colibactine . [26]
Maladie inflammatoire de l’intestin
Les personnes atteintes d’ une maladie intestinale inflammatoire ( colite ulcéreuse et maladie de Crohn ) courent un risque accru de cancer du côlon. [27] [28] Le risque augmente plus une personne a la maladie longtemps et plus la sévérité de l’inflammation est grave. [29] Dans ces groupes à haut risque, la prévention avec de l’aspirine et des coloscopies régulières sont recommandées. [30] La surveillance endoscopique dans cette population à haut risque peut réduire le développement du cancer colorectal grâce à un diagnostic précoce et peut également réduire les risques de mourir du cancer du côlon. [30]Les personnes atteintes de maladies inflammatoires de l’intestin représentent moins de 2 % des cas de cancer du côlon chaque année. [29] Chez les personnes atteintes de la maladie de Crohn, 2 % ont un cancer colorectal après 10 ans, 8 % après 20 ans et 18 % après 30 ans. [29] Chez les personnes atteintes de colite ulcéreuse, environ 16 % développent soit un précurseur du cancer , soit un cancer du côlon sur 30 ans. [29]
La génétique
Ceux qui ont des antécédents familiaux dans deux ou plusieurs parents au premier degré (comme un parent ou un frère ou une sœur) ont un risque de maladie deux à trois fois plus élevé et ce groupe représente environ 20 % de tous les cas. Un certain nombre de syndromes génétiques sont également associés à des taux plus élevés de cancer colorectal. Le plus courant d’entre eux est le cancer colorectal héréditaire sans polypose (HNPCC ou syndrome de Lynch) qui est présent chez environ 3 % des personnes atteintes d’un cancer colorectal. [18] D’autres syndromes fortement associés au cancer colorectal comprennent le syndrome de Gardner et la polypose adénomateuse familiale (PAF). [31] Pour les personnes atteintes de ces syndromes, le cancer survient presque toujours et représente 1 % des cas de cancer.[32] Une proctocolectomie totale peut être recommandée pour les personnes atteintes de PAF à titre préventif en raison du risque élevé de malignité. La colectomie, l’ablation du côlon, peut ne pas suffire comme mesure préventive en raison du risque élevé de cancer du rectum si le rectum reste. [33] Le syndrome de polypose le plus courant affectant le côlon est le syndrome de polypose dentelée , [34] qui est associé à un risque de 25 à 40 % de CCR. [35]
Des mutations dans la paire de gènes ( POLE et POLD1 ) ont été associées au cancer du côlon familial. [36]
La plupart des décès dus au cancer du côlon sont associés à une maladie métastatique. Un gène qui semble contribuer au potentiel de maladie métastatique, la métastase associée au cancer du côlon 1 ( MACC1 ), a été isolé. [37] C’est un facteur de transcription qui influence l’expression du facteur de croissance des hépatocytes . Ce gène est associé à la prolifération, à l’invasion et à la dispersion des cellules cancéreuses du côlon en culture cellulaire, ainsi qu’à la croissance tumorale et aux métastases chez la souris. MACC1 peut être une cible potentielle pour une intervention contre le cancer, mais cette possibilité doit être confirmée par des études cliniques. [38]
Des facteurs épigénétiques, tels qu’une méthylation anormale de l’ADN des promoteurs suppresseurs de tumeurs, jouent un rôle dans le développement du cancer colorectal. [39]
Les juifs ashkénazes ont un risque 6% plus élevé de contracter des adénomes, puis un cancer du côlon, car les mutations du gène APC sont plus fréquentes. [40]
Pathogénèse
Le cancer colorectal est une maladie provenant des cellules épithéliales tapissant le côlon ou le rectum du tractus gastro-intestinal , le plus souvent à la suite de mutations de la voie de signalisation Wnt qui augmentent l’activité de signalisation. Les mutations peuvent être héréditaires ou acquises et surviennent très probablement dans la cellule souche de la crypte intestinale . [41] [42] [43] Le gène le plus souvent muté dans tous les cancers colorectaux est le gène APC , qui produit la protéine APC. La protéine APC empêche l’accumulation de β-caténineprotéine. Sans APC, la β-caténine s’accumule à des niveaux élevés et transloque (se déplace) dans le noyau, se lie à l’ADN et active la transcription des proto- oncogènes . Ces gènes sont normalement importants pour le renouvellement et la différenciation des cellules souches, mais lorsqu’ils sont exprimés de manière inappropriée à des niveaux élevés, ils peuvent provoquer le cancer. Alors que l’APC est muté dans la plupart des cancers du côlon, certains cancers ont augmenté la β-caténine en raison de mutations de la β-caténine (CTNNB1) qui bloquent sa propre dégradation, ou ont des mutations dans d’autres gènes ayant une fonction similaire à APC tels que AXIN1 , AXIN2 , TCF7L2 , ou NKD1 . [44]
Au-delà des défauts de la voie de signalisation Wnt , d’autres mutations doivent se produire pour que la cellule devienne cancéreuse. La protéine p53 , produite par le gène TP53 , surveille normalement la division cellulaire et induit leur mort programmée si elles présentent des défauts de la voie Wnt. Finalement, une lignée cellulaire acquiert une mutation dans le gène TP53 et transforme le tissu d’une tumeur épithéliale bénigne en un cancer invasif des cellules épithéliales . Parfois, le gène codant pour p53 n’est pas muté, mais une autre protéine protectrice nommée BAX est mutée à la place. [44]
Les autres protéines responsables de la mort cellulaire programmée qui sont couramment désactivées dans les cancers colorectaux sont le TGF-β et le DCC ( Deleted in Colorectal Cancer ). Le TGF-β possède une mutation désactivante dans au moins la moitié des cancers colorectaux. Parfois, le TGF-β n’est pas désactivé, mais une protéine en aval nommée SMAD est désactivée. [44] DCC a généralement un segment supprimé d’un chromosome dans le cancer colorectal. [45]
Environ 70 % de tous les gènes humains sont exprimés dans le cancer colorectal, dont un peu plus de 1 % ont une expression accrue dans le cancer colorectal par rapport aux autres formes de cancer. [46] Certains gènes sont des oncogènes : ils sont surexprimés dans le cancer colorectal. Par exemple, les gènes codant pour les protéines KRAS , RAF et PI3K , qui stimulent normalement la cellule à se diviser en réponse aux facteurs de croissance, peuvent acquérir des mutations qui entraînent une suractivation de la prolifération cellulaire. L’ordre chronologique des mutations est parfois important. Si une mutation APC antérieure s’est produite, une mutation primaire de KRAS évolue souvent vers un cancer plutôt que vers une lésion hyperplasique ou limite autolimitée.[47] PTEN , un suppresseur de tumeur, inhibe normalement PI3K, mais peut parfois devenir muté et désactivé. [44]
Une analyse complète à l’échelle du génome a révélé que les carcinomes colorectaux peuvent être classés en types de tumeurs hypermutées et non hypermutées. [48] En plus des mutations oncogènes et inactivatrices décrites pour les gènes ci-dessus, les échantillons non hypermutés contiennent également des mutations CTNNB1 , FAM123B , SOX9 , ATM et ARID1A . Progressant à travers un ensemble distinct d’événements génétiques, les tumeurs hypermutées présentent des formes mutées de ACVR2A , TGFBR2 , MSH3 , MSH6 , SLC9A9, TCF7L2 et BRAF. Le thème commun à ces gènes, dans les deux types de tumeurs, est leur implication dans les voies de signalisation Wnt et TGF-β, ce qui entraîne une activité accrue de MYC , un acteur central du cancer colorectal. [48]
Les tumeurs déficientes en réparation des mésappariements (MMR) sont caractérisées par une quantité relativement élevée de répétitions en tandem de polynucléotides. [49] Ceci est causé par une carence en protéines MMR – qui sont généralement causées par un silençage épigénétique et/ou des mutations héréditaires (par exemple , le syndrome de Lynch ). [50] 15 à 18 % des tumeurs cancéreuses colorectales présentent des déficiences en ROR, dont 3 % se développent en raison du syndrome de Lynch. [51] Le rôle du système de réparation des mésappariements est de protéger l’intégrité du matériel génétique dans les cellules (c’est-à-dire : détecter et corriger les erreurs). [50]Par conséquent, une déficience en protéines MMR peut entraîner une incapacité à détecter et à réparer les dommages génétiques, permettant à d’autres mutations cancérigènes de se produire et au cancer colorectal de progresser. [50]
La séquence de progression du polype au cancer est le modèle classique de la pathogenèse du cancer colorectal. [52] La séquence polype-cancer décrit les phases de transition des tumeurs bénignes au cancer colorectal sur de nombreuses années. [52] Les mutations géniques, les altérations épigénétiques et les changements inflammatoires locaux sont au cœur de la séquence polype-CRC. [52] La séquence polype à CRC peut être utilisée comme cadre sous-jacent pour illustrer comment des changements moléculaires spécifiques conduisent à divers sous-types de cancer. [52]
Défauts de terrain

 Segment de côlon fraîchement réséqué ouvert longitudinalement montrant un cancer et quatre polypes. Plus un diagramme schématique indiquant un défaut de champ probable (une région de tissu qui précède et prédispose au développement du cancer) dans ce segment du côlon. Le diagramme indique les sous-clones et les sous-sous-clones précurseurs des tumeurs.
Segment de côlon fraîchement réséqué ouvert longitudinalement montrant un cancer et quatre polypes. Plus un diagramme schématique indiquant un défaut de champ probable (une région de tissu qui précède et prédispose au développement du cancer) dans ce segment du côlon. Le diagramme indique les sous-clones et les sous-sous-clones précurseurs des tumeurs.
Le terme “cancerisation de champ” a été utilisé pour la première fois en 1953 pour décrire une zone ou “champ” d’épithélium qui a été préconditionné (par des processus largement inconnus à l’époque) pour le prédisposer au développement du cancer. [53] Depuis lors, les termes « cancérisation de terrain », « cancérogenèse de terrain », « défaut de terrain » et « effet de terrain » ont été utilisés pour décrire les tissus pré-malignes ou pré-néoplasiques dans lesquels de nouveaux cancers sont susceptibles de survenir. [54]
Les anomalies du champ sont importantes dans la progression vers le cancer du côlon. [55] [56]
Cependant, comme l’a souligné Rubin, “La grande majorité des études dans la recherche sur le cancer ont été réalisées sur des tumeurs bien définies in vivo , ou sur des foyers néoplasiques discrets in vitro . Pourtant, il existe des preuves que plus de 80% des mutations somatiques trouvées dans le phénotype mutateur, les tumeurs colorectales humaines surviennent avant le début de l’expansion clonale terminale.” [57] [58] De même, Vogelstein et al. [59] ont souligné que plus de la moitié des mutations somatiques identifiées dans les tumeurs se produisaient dans une phase pré-néoplasique (dans un défaut du champ), lors de la croissance de cellules apparemment normales. De même, des altérations épigénétiques présentes dans les tumeurs peuvent s’être produites dans des défauts de champ pré-néoplasiques. [60]
Une vision élargie de l’effet de champ a été appelée « effet de champ étiologique », qui englobe non seulement les changements moléculaires et pathologiques dans les cellules pré-néoplasiques, mais également les influences des facteurs environnementaux exogènes et des changements moléculaires dans le microenvironnement local sur l’évolution néoplasique de l’initiation de la tumeur à la mort . . [61]
Épigénétique
Les altérations épigénétiques sont beaucoup plus fréquentes dans le cancer du côlon que les altérations génétiques (mutationnelles). Comme décrit par Vogelstein et al. [59] , un cancer moyen du côlon n’a que 1 ou 2 mutations oncogènes et 1 à 5 mutations suppresseurs de tumeurs (ensemble appelées « mutations motrices »), avec environ 60 autres mutations « passagères ». Les oncogènes et les gènes suppresseurs de tumeurs sont bien étudiés et sont décrits ci-dessus sous Pathogenèse . [62] [63]
En plus de l’altération épigénétique de l’expression des miARN, d’autres types courants d’altérations épigénétiques dans les cancers qui modifient les niveaux d’expression des gènes comprennent l’hyperméthylation ou l’hypométhylation directe des îlots CpG des gènes codant pour les protéines et les altérations des histones et de l’architecture chromosomique qui influencent l’expression des gènes. [64] À titre d’exemple, 147 hyperméthylations et 27 hypométhylations de gènes codant pour des protéines étaient fréquemment associées à des cancers colorectaux. Parmi les gènes hyperméthylés, 10 étaient hyperméthylés dans 100 % des cancers du côlon, et de nombreux autres étaient hyperméthylés dans plus de 50 % des cancers du côlon. [65] De plus, 11 hyperméthylations et 96 hypométhylations de miARN ont également été associées à des cancers colorectaux. [65] Anormal (aberrant)la méthylation est une conséquence normale du vieillissement normal et le risque de cancer colorectal augmente à mesure qu’une personne vieillit. [66] La source et le déclencheur de cette méthylation liée à l’âge sont inconnus. [66] [67] Environ la moitié des gènes qui montrent des changements de méthylation liés à l’âge sont les mêmes gènes qui ont été identifiés comme étant impliqués dans le développement du cancer colorectal. [66] Ces résultats peuvent suggérer une raison pour laquelle l’âge est associé au risque accru de développer un cancer colorectal. [66]
Les réductions épigénétiques de l’expression des enzymes de réparation de l’ADN peuvent probablement conduire à l’instabilité génomique et épigénomique caractéristique du cancer. [68] [69] [70] Comme résumé dans les articles Carcinogenesis and Neoplasm , pour les cancers sporadiques en général, un déficit de réparation de l’ADN est parfois dû à une mutation dans un gène de réparation de l’ADN, mais est beaucoup plus fréquemment dû à des altérations épigénétiques qui réduisent ou font taire l’expression des gènes de réparation de l’ADN. [71]
Les altérations épigénétiques impliquées dans le développement du cancer colorectal peuvent affecter la réponse d’une personne à la chimiothérapie. [72]
Génomique | Épigénomique
La classification des sous-types moléculaires consensuels (CMS) du cancer colorectal a été introduite pour la première fois en 2015. Jusqu’à présent, la classification CMS a été considérée comme le système de classification le plus robuste disponible pour le CCR qui a une interprétabilité biologique claire et la base de la future stratification clinique et des interventions ciblées basées sur les sous-types . [73]
Une nouvelle classification basée sur l’épigénome (EpiC) du cancer colorectal a été proposée en 2021, introduisant 4 sous-types d’amplificateurs chez les personnes atteintes de CCR. Les états de la chromatine utilisant 6 marques d’histone sont caractérisés pour identifier les sous-types EpiC. Une approche thérapeutique combinatoire basée sur les sous-types moléculaires consensus (CMS) et les EpiC introduits précédemment pourrait améliorer considérablement les stratégies de traitement actuelles. [74]
Diagnostic
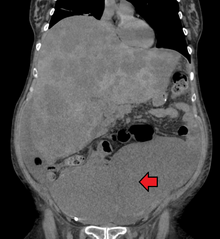
 Cancer du côlon avec métastases étendues au foie
Cancer du côlon avec métastases étendues au foie
Le diagnostic du cancer colorectal est réalisé en prélevant des échantillons de zones du côlon suspectes d’un éventuel développement tumoral, généralement au cours d’une coloscopie ou d’une sigmoïdoscopie, selon la localisation de la lésion. [18] Il est confirmé par l’examen microscopique d’un échantillon de tissu. [ citation nécessaire ]
L’imagerie médicale
Un cancer colorectal est parfois initialement découvert au scanner . [75]
La présence de métastases est déterminée par un scanner du thorax, de l’abdomen et du bassin. [18] D’autres tests d’imagerie potentiels tels que la TEP et l’ IRM peuvent être utilisés dans certains cas. [18] Ce dernier est souvent utilisé pour les lésions rectales afin de déterminer son stade local et de faciliter la planification préopératoire. [75]
Histopathologie

 Incidence relative de divers types histopathologiques de cancer colorectal. La grande majorité des cancers colorectaux sont des adénocarcinomes . [76]
Incidence relative de divers types histopathologiques de cancer colorectal. La grande majorité des cancers colorectaux sont des adénocarcinomes . [76] 
 Micrographie d’un adénocarcinome colorectal montrant une “sale nécrose”.
Micrographie d’un adénocarcinome colorectal montrant une “sale nécrose”.
Les caractéristiques histopathologiques de la tumeur sont rapportées à partir de l’analyse de tissus prélevés lors d’une biopsie ou d’une intervention chirurgicale. Un rapport de pathologie contient une description des caractéristiques microscopiques du tissu tumoral, y compris à la fois les cellules tumorales et la façon dont la tumeur envahit les tissus sains et enfin si la tumeur semble être complètement retirée. La forme la plus courante de cancer du côlon est l’ adénocarcinome , constituant entre 95 % [77] et 98 % [78] de tous les cas de cancer colorectal. D’autres types plus rares comprennent le lymphome , le carcinome adénosquameux et épidermoïde . Certains sous-types se sont avérés plus agressifs. [79] L’immunohistochimie peut être utilisée dans des cas incertains. [80]
Mise en scène
La stadification du cancer est basée à la fois sur les résultats radiologiques et pathologiques. Comme pour la plupart des autres formes de cancer, la stadification tumorale est basée sur le système TNM qui tient compte de l’étendue de la propagation de la tumeur initiale et de la présence de métastases dans les ganglions lymphatiques et les organes plus éloignés. [18] La 8e édition de l’AJCC a été publiée en 2018. [81]
La prévention
On estime qu’environ la moitié des cas de cancer colorectal sont dus à des facteurs liés au mode de vie et qu’environ un quart de tous les cas sont évitables. [82] L’augmentation de la surveillance, la pratique d’une activité physique, une alimentation riche en fibres et la réduction du tabagisme et de la consommation d’alcool diminuent le risque. [83] [84]
Mode de vie
Les facteurs de risque liés au mode de vie avec des preuves solides comprennent le manque d’exercice, le tabagisme, l’alcool et l’obésité. [85] [86] Le risque de cancer du côlon peut être réduit en maintenant un poids corporel normal grâce à une combinaison d’exercice suffisant et d’une alimentation saine . [87]
Les recherches actuelles associent systématiquement la consommation de plus de viande rouge et de viande transformée à un risque plus élevé de contracter la maladie. [88] À partir des années 1970, les recommandations diététiques pour prévenir le cancer colorectal comprenaient souvent l’augmentation de la consommation de grains entiers, de fruits et de légumes et la réduction de la consommation de viande rouge et de viandes transformées . Ceci était basé sur des études animales et des études observationnelles rétrospectives. Cependant, des études prospectives à grande échelle n’ont pas réussi à démontrer un effet protecteur significatif, et en raison des multiples causes de cancer et de la complexité de l’étude des corrélations entre l’alimentation et la santé, il n’est pas certain que des interventions alimentaires spécifiques (en dehors d’une alimentation saine) auront des effets protecteurs importants. [89]: 432–433 [90] : 125–126 En 2018, l’ Institut national du cancer a déclaré qu'”il n’existe aucune preuve fiable qu’un régime alimentaire commencé à l’âge adulte, pauvre en graisses et en viande et riche en fibres, fruits et légumes, réduise le risque du CCR par un degré cliniquement important. » [85] [91]
Selon le Fonds mondial de recherche sur le cancer , la consommation de boissons alcoolisées et la consommation de viande transformée augmentent toutes deux le risque de cancer colorectal [92]
En ce qui concerne les fibres alimentaires, le rapport sur le cancer de l’Organisation mondiale de la santé de 2014 a noté qu’il a été émis l’hypothèse que les fibres pourraient aider à prévenir le cancer colorectal, mais la plupart des études ne l’ont pas confirmé et l’état de la science restait incertain en 2014. [90] Une revue de 2019, cependant, a trouvé des preuves des avantages des fibres alimentaires et des grains entiers. [93] Le Fonds mondial de recherche sur le cancer a classé les avantages des fibres pour la prévention du cancer colorectal comme « probables » en 2017. [94]
Une activité physique plus intense est recommandée. [19] [95] L’exercice physique est associé à une réduction modeste du risque de cancer du côlon mais pas du rectum. [96] [97] Des niveaux élevés d’activité physique réduisent le risque de cancer du côlon d’environ 21 %. [98] La position assise régulière pendant des périodes prolongées est associée à une mortalité plus élevée due au cancer du côlon. Le risque n’est pas annulé par l’exercice régulier, bien qu’il soit réduit. [99]
Médicaments et suppléments
L’aspirine et le célécoxib semblent diminuer le risque de cancer colorectal chez les personnes à haut risque. [100] [101] L’aspirine est recommandée chez les personnes âgées de 50 à 60 ans, qui n’ont pas de risque accru de saignement et qui sont à risque de maladie cardiovasculaire pour prévenir le cancer colorectal. [102] Il n’est pas recommandé chez les personnes à risque moyen. [103]
Il existe des preuves provisoires de la supplémentation en calcium , mais elles ne sont pas suffisantes pour faire une recommandation. [104] L’apport en vitamine D et les taux sanguins sont associés à un risque moindre de cancer du côlon. [105] [106]
Dépistage
Comme plus de 80 % des cancers colorectaux proviennent de polypes adénomateux , le dépistage de ce cancer est efficace à la fois pour la détection précoce et pour la prévention. [18] [107] Le diagnostic des cas de cancer colorectal par dépistage a tendance à se produire 2 à 3 ans avant le diagnostic des cas présentant des symptômes. [18] Tous les polypes détectés peuvent être retirés, généralement par coloscopie ou sigmoïdoscopie , et ainsi les empêcher de se transformer en cancer. Le dépistage a le potentiel de réduire de 60 % les décès par cancer colorectal. [108]
Les trois principaux tests de dépistage sont la coloscopie , la recherche de sang occulte dans les selles et la sigmoïdoscopie flexible . Des trois, seule la sigmoïdoscopie ne permet pas de dépister le côté droit du côlon où se trouvent 42 % des cancers. [109] La sigmoïdoscopie flexible, cependant, a la meilleure preuve pour réduire le risque de décès quelle qu’en soit la cause. [110]
Le test de sang occulte dans les selles (FOBT) des selles est généralement recommandé tous les deux ans et peut être basé sur le gaïac ou immunochimique . [18] Si des résultats anormaux de RSOS sont trouvés, les participants sont généralement référés pour un examen de suivi par coloscopie. Lorsqu’il est effectué une fois tous les 1 à 2 ans, le dépistage par RSOS réduit les décès par cancer colorectal de 16 % et parmi ceux qui participent au dépistage, les décès par cancer colorectal peuvent être réduits jusqu’à 23 %, bien qu’il n’ait pas été prouvé qu’il réduisait la mortalité toutes causes confondues. [111] Les tests immunochimiques sont précis et ne nécessitent pas de changements alimentaires ou de médicaments avant le test. [112]
D’autres options incluent la coloscopie virtuelle et le test de dépistage de l’ADN dans les selles (FIT-DNA). La coloscopie virtuelle via un scanner semble aussi efficace que la coloscopie standard pour détecter les cancers et les gros adénomes, mais elle est coûteuse, associée à l’exposition aux rayonnements et ne peut éliminer les croissances anormales détectées comme le peut la coloscopie standard. [18] Le test de dépistage de l’ADN dans les selles recherche des biomarqueurs associés au cancer colorectal et aux lésions précancéreuses, y compris l’ADN altéré et l’hémoglobine sanguine . Un résultat positif doit être suivi d’une coloscopie . FIT-DNA a plus de faux positifs que FIT et entraîne donc plus d’effets indésirables. [5]Une étude plus approfondie est nécessaire à partir de 2016 pour déterminer si un intervalle de dépistage de trois ans est correct. [5]
Recommandations
Aux États-Unis, le dépistage est généralement recommandé entre 50 et 75 ans. [5] [113] L’ American Cancer Society recommande de commencer à l’âge de 45 ans. [114] Pour les personnes âgées de 76 à 85 ans, la décision de faire un dépistage doit être individualisée. [5] Pour les personnes à haut risque, les dépistages commencent généralement vers 40 ans. [18] [115]
Plusieurs méthodes de dépistage sont recommandées, notamment des tests sur les selles tous les 2 ans, une sigmoïdoscopie tous les 10 ans avec un test immunochimique fécal tous les deux ans et une coloscopie tous les 10 ans. [113] On ne sait pas laquelle de ces deux méthodes est la meilleure. [116] La coloscopie peut détecter plus de cancers dans la première partie du côlon, mais elle est associée à un coût plus élevé et à davantage de complications. [116] Pour les personnes à risque moyen qui ont subi une coloscopie de haute qualité avec des résultats normaux, l’ American Gastroenterological Association ne recommande aucun type de dépistage dans les 10 ans suivant la coloscopie. [117] [118]Pour les personnes de plus de 75 ans ou celles dont l’espérance de vie est inférieure à 10 ans, le dépistage n’est pas recommandé. [119] Il faut environ 10 ans après le dépistage pour qu’une personne sur 1000 en bénéficie. [120] L’USPSTF énumère sept stratégies potentielles de dépistage, la chose la plus importante étant qu’au moins une de ces stratégies soit utilisée de manière appropriée. [5]
Au Canada, parmi les personnes âgées de 50 à 75 ans à risque normal, un test immunochimique fécal ou RSOS est recommandé tous les deux ans ou une sigmoïdoscopie tous les 10 ans. [121] La coloscopie est moins préférée. [121]
Certains pays ont des programmes nationaux de dépistage colorectal qui offrent un dépistage RSOS à tous les adultes d’un certain groupe d’âge, commençant généralement entre 50 et 60 ans. Parmi les exemples de pays pratiquant le dépistage organisé figurent le Royaume-Uni, [122] l’Australie, [123] les Pays-Bas, [124] Hong Kong et Taïwan. [125]
Traitement
Le traitement du cancer colorectal peut viser la guérison ou la palliation. La décision sur le but à adopter dépend de divers facteurs, dont la santé et les préférences de la personne, ainsi que le stade de la tumeur. [126] L’évaluation au sein d’équipes multidisciplinaires est un élément essentiel pour déterminer si le patient est apte ou non à subir une intervention chirurgicale. [127] Lorsque le cancer colorectal est détecté tôt, la chirurgie peut être curative. Cependant, lorsqu’elle est détectée à des stades ultérieurs (pour lesquels des métastases sont présentes), cela est moins probable et le traitement est souvent axé sur les soins palliatifs, pour soulager les symptômes causés par la tumeur et maintenir la personne aussi confortable que possible. [18]
Opération

 Un schéma d’une résection locale d’un cancer du côlon à un stade précoce
Un schéma d’une résection locale d’un cancer du côlon à un stade précoce 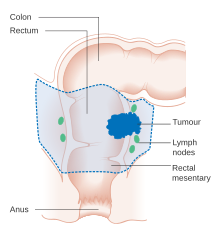
 Un schéma de chirurgie locale pour le cancer du rectum
Un schéma de chirurgie locale pour le cancer du rectum
Si le cancer est détecté à un stade précoce, il peut être retiré lors d’une coloscopie en utilisant l’une des nombreuses techniques, y compris la résection endoscopique de la muqueuse ou la dissection endoscopique de la sous-muqueuse . [6] Pour les personnes atteintes d’un cancer localisé, le traitement préféré est l’ablation chirurgicale complète avec des marges adéquates , avec une tentative de guérison. La procédure de choix est une colectomie partielle (ou proctocolectomie pour les lésions rectales) où la partie affectée du côlon ou du rectum est enlevée avec des parties de son mésocôlon et de son apport sanguin pour faciliter l’élimination des ganglions lymphatiques drainants . Cela peut être fait soit par une ouverturelaparotomie ou laparoscopie , en fonction de facteurs liés à la personne individuelle et des facteurs lésionnels. [18] Le côlon peut alors être reconnecté ou une personne peut subir une colostomie . [6]
S’il n’y a que quelques métastases dans le foie ou les poumons, celles-ci peuvent également être retirées. La chimiothérapie peut être utilisée avant la chirurgie pour réduire le cancer avant de tenter de l’enlever. Les deux sites de récidive les plus fréquents du cancer colorectal sont le foie et les poumons . [18] Pour la carcinomatose péritonéale, la chirurgie cytoréductrice, parfois en combinaison avec HIPEC, peut être utilisée pour tenter d’éliminer le cancer. [128]
Chimiothérapie
Dans les cancers du côlon et du rectum , la chimiothérapie peut être utilisée en complément de la chirurgie dans certains cas. La décision d’ajouter la chimiothérapie dans la prise en charge des cancers du côlon et du rectum dépend du stade de la maladie. [129]
Dans le cancer du côlon de stade I, aucune chimiothérapie n’est proposée et la chirurgie est le traitement définitif. Le rôle de la chimiothérapie dans le cancer du côlon de stade II est discutable et n’est généralement pas proposé à moins que des facteurs de risque tels qu’une tumeur T4, une tumeur indifférenciée, une invasion vasculaire et périneurale ou un échantillonnage inadéquat des ganglions lymphatiques ne soient identifiés. [130] On sait également que les personnes porteuses d’anomalies des gènes de réparation des mésappariements ne bénéficient pas de la chimiothérapie. Pour le cancer du côlon de stade III et de stade IV, la chimiothérapie fait partie intégrante du traitement. [18]
Si le cancer s’est propagé aux ganglions lymphatiques ou aux organes distants, ce qui est le cas respectivement du cancer du côlon de stade III et de stade IV, l’ajout d’agents de chimiothérapie fluorouracile , capécitabine ou oxaliplatine augmente l’espérance de vie. Si les ganglions lymphatiques ne contiennent pas de cancer, les bénéfices de la chimiothérapie sont controversés. Si le cancer est largement métastatique ou non résécable, le traitement est alors palliatif . Généralement, dans ce contexte, un certain nombre de médicaments de chimiothérapie différents peuvent être utilisés. [18] Les médicaments de chimiothérapie pour cette condition peuvent inclure la capécitabine , le fluorouracile , l’ irinotécan , l’oxaliplatineet UFT . [131] Les médicaments capécitabine et fluorouracile sont interchangeables, la capécitabine étant un médicament oral et le fluorouracile étant un médicament intraveineux. Certains régimes spécifiques utilisés pour le CCR sont CAPOX , FOLFOX , FOLFOXIRI et FOLFIRI . [132] Des médicaments anti-angiogéniques tels que le bevacizumab sont souvent ajoutés au traitement de première intention. Une autre classe de médicaments utilisés en deuxième intention sont les inhibiteurs des récepteurs du facteur de croissance épidermique , dont les trois approuvés par la FDA sont l’ aflibercept , le cétuximab et le panitumumab .. [133] [134]
La principale différence dans l’approche du cancer rectal de stade inférieur est l’incorporation de la radiothérapie. Souvent, il est utilisé en conjonction avec une chimiothérapie de manière néoadjuvante pour permettre une résection chirurgicale, de sorte qu’en fin de compte une colostomie n’est pas nécessaire. Cependant, cela peut ne pas être possible dans les tumeurs basses, auquel cas une colostomie permanente peut être nécessaire. Le cancer du rectum de stade IV est traité de la même manière que le cancer du côlon de stade IV.
Le cancer colorectal de stade IV dû à une carcinomatose péritonéale peut être traité par HIPEC associé à une chirurgie cytoréductive, chez certaines personnes. [135] [136] [137]
Radiothérapie
Bien qu’une combinaison de radiothérapie et de chimiothérapie puisse être utile pour le cancer du rectum [18] , pour certaines personnes nécessitant un traitement, la chimioradiothérapie peut augmenter la toxicité aiguë liée au traitement et n’a pas démontré qu’elle améliore les taux de survie par rapport à la radiothérapie seule, bien qu’elle soit associée avec moins de récidive locale. [128] L’utilisation de la radiothérapie dans le cancer du côlon n’est pas systématique en raison de la sensibilité des intestins aux radiations. [138] Comme pour la chimiothérapie, la radiothérapie peut être utilisée comme néo-adjuvant pour les stades cliniques T3 et T4 du cancer du rectum. [139]Cela entraîne une réduction de la taille ou une réduction de la taille de la tumeur, la préparant à une résection chirurgicale, et diminue également les taux de récidive locale. [139] Pour le cancer du rectum localement avancé, la chimioradiothérapie néoadjuvante est devenue le traitement de référence. [140] De plus, lorsque la chirurgie n’est pas possible, la radiothérapie a été suggérée comme un traitement efficace contre les métastases pulmonaires du CCR, qui sont développées par 10 à 15 % des personnes atteintes de CCR. [141]
Immunothérapie
L’immunothérapie avec des inhibiteurs de point de contrôle immunitaire s’est avérée utile pour un type de cancer colorectal avec un déficit de réparation des mésappariements et une instabilité des microsatellites. [142] [143] Le pembrolizumab est approuvé pour les tumeurs CRC avancées qui sont déficientes en ROR et ont échoué aux traitements habituels. [144] La plupart des gens qui s’améliorent, cependant, s’aggravent encore après des mois ou des années. [143] D’autres types de cancer colorectal à partir de 2017 sont toujours à l’étude. [142] [143]
Soins palliatifs
Les soins palliatifs sont recommandés pour toute personne atteinte d’un cancer du côlon avancé ou présentant des symptômes importants. [145] [146]
L’implication des soins palliatifs peut être bénéfique pour améliorer la qualité de vie de la personne et de sa famille, en atténuant les symptômes, l’anxiété et en prévenant les admissions à l’hôpital. [147]
Chez les personnes atteintes d’un cancer colorectal incurable, les soins palliatifs peuvent consister en des procédures qui soulagent les symptômes ou les complications du cancer, mais ne tentent pas de guérir le cancer sous-jacent, améliorant ainsi la qualité de vie . Les options chirurgicales peuvent inclure l’ablation chirurgicale non curative d’une partie du tissu cancéreux, le contournement d’une partie des intestins ou la mise en place d’un stent. Ces procédures peuvent être envisagées pour améliorer les symptômes et réduire les complications telles que les saignements de la tumeur, les douleurs abdominales et l’obstruction intestinale. [148] Les méthodes non opératoires de traitement symptomatique comprennent la radiothérapie pour réduire la taille de la tumeur ainsi que les analgésiques. [149]
Suivi
Le US National Comprehensive Cancer Network et l’American Society of Clinical Oncology fournissent des lignes directrices pour le suivi du cancer du côlon. [150] [151] Une anamnèse et un examen physique sont recommandés tous les 3 à 6 mois pendant 2 ans, puis tous les 6 mois pendant 5 ans. Les mesures du taux sanguin d’antigène carcinoembryonnaire suivent le même calendrier, mais ne sont conseillées que pour les personnes atteintes de lésions T2 ou plus qui sont candidates à une intervention. Un scannerdu thorax, de l’abdomen et du bassin peut être envisagée annuellement pendant les 3 premières années pour les personnes à haut risque de récidive (par exemple, celles qui ont eu des tumeurs peu différenciées ou une invasion veineuse ou lymphatique) et sont candidates à une chirurgie curative (avec le viser à guérir). Une coloscopie peut être réalisée après 1 an, sauf si elle n’a pas pu être réalisée lors de la stadification initiale en raison d’une masse obstructive, auquel cas elle doit être réalisée au bout de 3 à 6 mois. Si un polype villeux, un polype >1 centimètre ou une dysplasie de haut grade est retrouvé, il peut être répété au bout de 3 ans, puis tous les 5 ans. Pour les autres anomalies, la coloscopie peut être répétée après 1 an. [129]
La TEP ou l’échographie de routine , les radiographies pulmonaires , la formule sanguine complète ou les tests de la fonction hépatique ne sont pas recommandés. [150] [151]
Pour les personnes qui ont subi une chirurgie curative ou un traitement adjuvant (ou les deux) pour traiter un cancer colorectal non métastatique, il n’a pas été démontré qu’une surveillance intense et un suivi étroit offrent des avantages supplémentaires en termes de survie. [152]
Exercer
L’exercice pourrait être recommandé à l’avenir comme thérapie secondaire pour les survivants du cancer. Dans les études épidémiologiques, l’exercice peut diminuer la mortalité spécifique au cancer colorectal et la mortalité toutes causes confondues. Les résultats pour les quantités spécifiques d’exercice nécessaires pour observer un bénéfice étaient contradictoires. Ces différences peuvent refléter des différences dans la biologie tumorale et l’expression des biomarqueurs. Les personnes atteintes de tumeurs dépourvues d’ expression de CTNNB1 (β-caténine), impliquée dans la voie de signalisation Wnt , avaient besoin de plus de 18 équivalents métaboliques(MET) heures par semaine, une mesure d’exercice, pour observer une réduction de la mortalité par cancer colorectal. Le mécanisme par lequel l’exercice profite à la survie peut être impliqué dans la surveillance immunitaire et les voies de l’inflammation. Dans les études cliniques, une réponse pro-inflammatoire a été trouvée chez les personnes atteintes d’un cancer colorectal de stade II-III qui ont subi 2 semaines d’exercice modéré après avoir terminé leur traitement primaire. L’équilibre oxydatif peut être un autre mécanisme possible des avantages observés. Une diminution significative du 8-oxo-dG a été constatée dans l’urine des personnes ayant subi 2 semaines d’exercice modéré après le traitement primaire. D’autres mécanismes possibles peuvent impliquer les hormones métaboliques et les hormones stéroïdes sexuelles, bien que ces voies puissent être impliquées dans d’autres types de cancers [153] [154]
Un autre biomarqueur potentiel pourrait être p27 . Les survivants avec des tumeurs qui exprimaient p27 et effectuaient plus ou moins 18 heures MET par semaine avaient une survie à la mortalité par cancer colorectal réduite par rapport à ceux avec moins de 18 heures MET par semaine. Les survivants sans expression de p27 qui ont fait de l’exercice se sont avérés avoir de moins bons résultats. L’activation constitutive de la voie PI3K/AKT/mTOR peut expliquer la perte de p27 et un bilan énergétique excessif peut réguler à la hausse p27 pour empêcher les cellules cancéreuses de se diviser. [154]
L’activité physique est bénéfique pour les personnes atteintes d’un cancer colorectal non avancé. Des améliorations de la capacité aérobique, de la fatigue liée au cancer et de la qualité de vie liée à la santé ont été signalées à court terme. [155] Cependant, ces améliorations n’ont pas été observées au niveau de la santé mentale liée à la maladie, comme l’anxiété et la dépression. [155]
Pronostic
Moins de 600 gènes sont liés aux résultats du cancer colorectal. [46] Ceux-ci incluent à la fois des gènes défavorables, où une expression élevée est liée à un mauvais résultat, par exemple la protéine de choc thermique 70 kDa 1 (HSPA1A) , et des gènes favorables où une expression élevée est associée à une meilleure survie, par exemple la putative liaison à l’ARN protéine 3 (RBM3) . [46]
Taux de récidive
Le taux moyen de récidive à cinq ans chez les personnes dont la chirurgie réussit est de 5 % pour les cancers de stade I, de 12 % pour le stade II et de 33 % pour le stade III. Cependant, selon le nombre de facteurs de risque, il varie de 9 à 22 % au stade II et de 17 à 44 % au stade III. [156]
Taux de survie
En Europe, le taux de survie à cinq ans pour le cancer colorectal est inférieur à 60 %. Dans le monde développé, environ un tiers des personnes qui contractent la maladie en meurent. [18]
La survie est directement liée à la détection et au type de cancer en cause, mais dans l’ensemble, elle est médiocre pour les cancers symptomatiques, car ils sont généralement assez avancés. Les taux de survie pour la détection à un stade précoce sont environ cinq fois supérieurs à ceux des cancers à un stade avancé. Les personnes atteintes d’une tumeur qui n’a pas franchi la muqueuse musculaire(stade TNM Tis, N0, M0) ont un taux de survie à cinq ans de 100 %, tandis que ceux atteints d’un cancer invasif de T1 (dans la couche sous-muqueuse) ou T2 (dans la couche musculaire) ont un taux de survie moyen à cinq ans de environ 90 %. Ceux qui ont une tumeur plus invasive mais sans atteinte ganglionnaire (T3-4, N0, M0) ont un taux de survie moyen à cinq ans d’environ 70 %. Les personnes avec des ganglions lymphatiques régionaux positifs (tout T, N1-3, M0) ont un taux de survie moyen à cinq ans d’environ 40 %, tandis que celles avec des métastases à distance (tout T, tout N, M1) ont un mauvais pronostic et les cinq la survie annuelle varie de <5 % à 31 %. [157] [158] [159] [160] [161]Le pronostic dépend d’une multitude de facteurs, notamment le niveau de forme physique de la personne, l’étendue des métastases et le grade de la tumeur. [ citation nécessaire ]
Alors que l’impact du cancer colorectal sur ceux qui survivent varie considérablement, il sera souvent nécessaire de s’adapter aux résultats physiques et psychologiques de la maladie et de son traitement. [162] Par exemple, il est courant que les gens souffrent d’incontinence, [163] de dysfonction sexuelle, [164] de problèmes de soins de stomie [165] et de peur de la récidive du cancer [166] après la fin du traitement primaire.
Une revue systématique qualitative publiée en 2021 a mis en évidence qu’il existe trois principaux facteurs influençant l’adaptation à vivre avec et au-delà du cancer colorectal : les mécanismes de soutien, la sévérité des effets tardifs du traitement et l’adaptation psychosociale. Il est donc essentiel que les personnes reçoivent un soutien approprié pour les aider à mieux s’adapter à la vie après le traitement. [167]
Épidémiologie
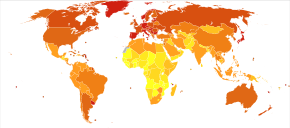
 Décès par cancer du côlon et du rectum par million de personnes en 2012 3–17 18–21 22–27 28–36 37–54 55–77 78–162 163–244 245–329 330–533
Décès par cancer du côlon et du rectum par million de personnes en 2012 3–17 18–21 22–27 28–36 37–54 55–77 78–162 163–244 245–329 330–533
À l’échelle mondiale, plus d’un million de personnes contractent un cancer colorectal chaque année [18] , entraînant environ 715 000 décès en 2010, contre 490 000 en 1990. [168]
En 2012 [mettre à jour], il s’agit de la deuxième cause de cancer chez les femmes (9,2 % des diagnostics) et de la troisième chez les hommes (10,0 %) [12] : 16 , la quatrième cause de décès par cancer après le cancer du poumon . , cancer de l’ estomac et du foie . [169] Elle est plus fréquente dans les pays développés que dans les pays en développement. [170] À l’échelle mondiale, les incidences varient de 10 fois avec les taux les plus élevés en Australie, en Nouvelle-Zélande, en Europe et aux États-Unis et les taux les plus bas en Afrique et en Asie du Sud-Centre. [171]
États-Unis
En 2022, l’incidence du cancer colorectal aux États-Unis devrait être d’environ 151 000 adultes, dont plus de 106 000 nouveaux cas de cancer du côlon (environ 54 000 hommes et 52 000 femmes) et environ 45 000 nouveaux cas de cancer rectal. [172] Depuis les années 1980, l’incidence du cancer colorectal a diminué, chutant d’environ 2 % par an de 2014 à 2018 chez les adultes de 50 ans et plus, principalement en raison de l’amélioration du dépistage. [172]
Royaume-Uni
Au Royaume-Uni, environ 41 000 personnes par an contractent un cancer du côlon, ce qui en fait le quatrième type le plus courant. [173]
Australie
Un homme sur 19 et une femme sur 28 en Australie développeront un cancer colorectal avant l’âge de 75 ans ; un homme sur 10 et une femme sur 15 le développeront à 85 ans. [174]
Papouasie Nouvelle Guinée
Dans les pays en développement comme la Papouasie-Nouvelle-Guinée et d’autres États insulaires du Pacifique, y compris les Îles Salomon, le cancer colorectal est un cancer très rare parmi la population, qui est moins fréquent que le cancer du poumon, de l’estomac, du foie ou du sein. On estime qu’au moins 8 personnes sur 100 000 sont les plus susceptibles de développer un cancer colorectal chaque année, contrairement au cancer du poumon ou du sein, où, pour ce dernier seul, 24 sur 100 000 des femmes seules. [175]
Histoire
Un cancer rectal a été diagnostiqué chez une momie égyptienne antique qui avait vécu dans l’ oasis de Dakhleh pendant la période ptolémaïque . [176]
Société et culture
Aux États-Unis, mars est le mois de la sensibilisation au cancer colorectal . [108]
Rechercher
Des preuves in vitro préliminaires suggèrent que les bactéries lactiques (par exemple, les lactobacilles , les streptocoques ou les lactocoques ) peuvent protéger contre le développement et la progression du cancer colorectal par plusieurs mécanismes tels que l’activité antioxydante , l’ immunomodulation , la promotion de la mort cellulaire programmée , les effets antiprolifératifs et la modification épigénétique de cellules cancéreuses. [177]
Des modèles murins de cancer colorectal et intestinal ont été développés et sont utilisés en recherche. [178] [179] [180]
- L’Atlas du génome du cancer [48]
- L’Atlas du cancer colorectal intégrant des données génomiques et protéomiques relatives aux tissus et aux lignées cellulaires du cancer colorectal a été développé. [181]
Références
- ^ un bcd ” Informations générales sur le cancer du côlon “ . NCI . 12 mai 2014. Archivé de l’original le 4 juillet 2014 . Consulté le 29 juin 2014 .
- ^ un bcdefghijkl Bosman FT ( 2014 ) . _ _ _ _ _ “Chapitre 5.5 : Cancer colorectal” . Dans Stewart BW, Wild CP (éd.). Rapport mondial sur le cancer . Centre international de recherche sur le cancer, Organisation mondiale de la santé. p. 392–402. ISBN 978-92-832-0443-5.
- ^ un bc « Prévention du cancer colorectal ( PDQ® ) » . Institut national du cancer . 27 février 2014. Archivé de l’original le 5 juillet 2014 . Consulté le 29 juin 2014 .
- ^ un b Theodoratou E, Timofeeva M, Li X, Meng X, Ioannidis JP (août 2017). « Nature, culture et risques de cancer : contributions génétiques et nutritionnelles au cancer » . Revue annuelle de la nutrition (Revue). 37 : 293–320. doi : 10.1146/annurev-nutr-071715-051004 . PMC 6143166 . PMID 28826375 .
- ^ un bcdefgh Bibbins – Domingo K , Grossman DC, Curry SJ, Davidson KW, Epling JW, García FA, et al. (juin 2016). “Dépistage du cancer colorectal : déclaration de recommandation du groupe de travail sur les services préventifs des États-Unis” . JAMA . 315 (23): 2564-2575. doi : 10.1001/jama.2016.5989 . PMID 27304597 .
- ^ un bcdefg ” Traitement du cancer du côlon ( PDQ® )” . NCI . 12 mai 2014. Archivé de l’original le 5 juillet 2014 . Consulté le 29 juin 2014 .
- ^ un b “Feuilles d’information SEER Stat: Cancer du côlon et du rectum” . NCI . Archivé de l’original le 24 juin 2014 . Consulté le 18 juin 2014 .
- ^ Vos T, Barber RM, Bell B, Bertozzi-Villa A, Biryukov S, Bolliger I, et al. (GBD 2015 Disease and Injury Incidence and Prevalence Collaborators) (octobre 2016). “Incidence, prévalence et années vécues avec un handicap au niveau mondial, régional et national pour 310 maladies et blessures, 1990-2015 : une analyse systématique pour l’étude Global Burden of Disease Study 2015” . Lancette . 388 (10053): 1545-1602. doi : 10.1016/S0140-6736(16)31678-6 . PMC 5055577 . PMID 27733282 .
- ^ un b Bray F, Ferlay J, Soerjomataram I, Siegel RL, Torre LA, Jemal A (novembre 2018). “Statistiques mondiales sur le cancer 2018 : estimations GLOBOCAN de l’incidence et de la mortalité dans le monde pour 36 cancers dans 185 pays” . CA : Un journal sur le cancer pour les cliniciens . 68 (6): 394–424. doi : 10.3322/caac.21492 . PMID 30207593 . S2CID 52188256 .
- ^ Thorat MA, Cuzick J (décembre 2013). “Rôle de l’aspirine dans la prévention du cancer” . Rapports d’oncologie actuels . 15 (6): 533–540. doi : 10.1007/s11912-013-0351-3 . PMID 24114189 . S2CID 40187047 .
- ^ “Aspirine de routine ou anti-inflammatoires non stéroïdiens pour la prévention primaire du cancer colorectal : déclaration de recommandation” . Médecin de famille américain . 76 (1): 109–113. Juillet 2007. PMID 17668849 . Archivé de l’original le 14 juillet 2014.
- ^ un b Forman D, Ferlay J (2014). “Chapitre 1.1 : Le fardeau mondial et régional du cancer” . Dans Stewart BW, Wild CP (éd.). Rapport mondial sur le cancer . Centre international de recherche sur le cancer, Organisation mondiale de la santé. p. 16–53. ISBN 978-92-832-0443-5.
- ^ Alpers DH, Kalloo AN, Kaplowitz N, Owyang C, Powell DW (2008). Yamada T (éd.). Principes de la gastro-entérologie clinique . Chichester, West Sussex : Wiley-Blackwell. p. 381.ISBN _ 978-1-4051-6910-3. Archivé de l’original le 28 septembre 2015.
- ^ Juul JS, Hornung N, Andersen B, Laurberg S, Olesen F, Vedsted P (août 2018). “L’intérêt d’utiliser le test immunochimique fécal en médecine générale sur des patients présentant des symptômes non alarmants de cancer colorectal” . Journal britannique du cancer . 119 (4): 471–479. doi : 10.1038/s41416-018-0178-7 . PMC 6133998 . PMID 30065255 .
- ^ un b Astin M, Griffin T, Neal RD, Rose P, Hamilton W (mai 2011). “La valeur diagnostique des symptômes du cancer colorectal en soins primaires : une revue systématique” . Le Journal britannique de médecine générale . 61 (586): e231–e243. doi : 10.3399/bjgp11X572427 . PMC 3080228 . PMID 21619747 .
- ^ Adelstein BA, Macaskill P, Chan SF, Katelaris PH, Irwig L (mai 2011). “La plupart des symptômes du cancer de l’intestin n’indiquent pas un cancer colorectal et des polypes : une revue systématique” . BMC Gastroentérologie . 11 : 65. doi : 10.1186/1471-230X-11-65 . PMC 3120795 . PMID 21624112 .
- ^ un b Watson AJ, Collins PD (2011). « Cancer du côlon : un trouble de la civilisation » . Maladies digestives . 29 (2): 222–228. doi : 10.1159/000323926 . PMID 21734388 . S2CID 7640363 .
- ^ un bcd e f g h i j k l m n o p q r s t Cunningham D, Atkin W, Lenz HJ, Lynch HT, Minsky B, Nordlinger B, Starling N (mars 2010). “Cancer colorectal”. Lancette . 375 (9719): 1030–1047. doi : 10.1016/S0140-6736(10)60353-4 . PMID 20304247 . S2CID 25299272 .
- ^ un b “Rapport 2011 sur le Cancer Colorectal : Alimentation, Nutrition, Activité Physique et la Prévention du Cancer Colorectal” (PDF) . Fonds mondial de recherche sur le cancer et Institut américain de recherche sur le cancer. 2011. Archivé (PDF) de l’original le 9 septembre 2016.
- ^ Lee IM, Shiroma EJ, Lobelo F, Puska P, Blair SN, Katzmarzyk PT (juillet 2012). “Effet de l’inactivité physique sur les principales maladies non transmissibles dans le monde : une analyse du fardeau de la maladie et de l’espérance de vie” . Lancette . 380 (9838): 219–229. doi : 10.1016/S0140-6736(12)61031-9 . PMC 3645500 . PMID 22818936 .
- ^ Fedirko V, Tramacere I, Bagnardi V, Rota M, Scotti L, Islami F, et al. (septembre 2011). “Consommation d’alcool et risque de cancer colorectal : une méta-analyse globale et dose-réponse des études publiées” . Annales d’oncologie . 22 (9): 1958–1972. doi : 10.1093/annonc/mdq653 . PMID 21307158 .
- ^ Valtin H (novembre 2002). ” “Boire au moins huit verres d’eau par jour.” Vraiment? Existe-t-il des preuves scientifiques pour “8 x 8″ ?”. American Journal of Physiology. Regulatory, Integrative and Comparative Physiology . 283 (5): R993-1004. doi : 10.1152/ajpregu.00365.2002 . PMID 12376390 . S2CID 2256436 .
- ^ Boleij A, van Gelder MM, Swinkels DW, Tjalsma H (novembre 2011). “Importance clinique de l’infection à Streptococcus gallolyticus chez les patients atteints de cancer colorectal : revue systématique et méta-analyse” . Maladies infectieuses cliniques . 53 (9): 870–878. doi : 10.1093/cid/cir609 . PMID 21960713 .
- ^ Jans C, Meile L, Lacroix C, Stevens MJ (juillet 2015). “Génomique, évolution et épidémiologie moléculaire du complexe Streptococcus bovis / Streptococcus equinus (SBSEC)”. Infection, génétique et évolution . 33 : 419–436. doi : 10.1016/j.meegid.2014.09.017 . PMID 25233845 .
- ^ un bc Abdulamir AS, Hafidh RR, Abu Bakar F (janvier 2011). “L’association de Streptococcus bovis/gallolyticus avec les tumeurs colorectales : la nature et les mécanismes sous-jacents de son rôle étiologique” . Journal de recherche expérimentale et clinique sur le cancer . 30 (1): 11. doi : 10.1186/1756-9966-30-11 . PMC 3032743 . PMID 21247505 .
![]()
![]() Cet article incorpore des textes d’Ahmed S Abdulamir, Rand R Hafidh et Fatimah Abu Bakar disponibles sous la licence CC BY 2.0 .
Cet article incorpore des textes d’Ahmed S Abdulamir, Rand R Hafidh et Fatimah Abu Bakar disponibles sous la licence CC BY 2.0 . - ^ Arthur JC (juin 2020). “Microbiote et cancer colorectal : la colibactine s’impose”. Revues naturelles. Gastro-entérologie et hépatologie . 17 (6): 317–318. doi : 10.1038/s41575-020-0303-y . PMID 32317778 . S2CID 216033220 .
- ^ Jawad N, Direkze N, Leedham SJ (2011). “Maladie inflammatoire de l’intestin et cancer du côlon”. Inflammation et cancers gastro-intestinaux . Résultats récents de la recherche sur le cancer. Vol. 185. p. 99–115. doi : 10.1007/978-3-642-03503-6_6 . ISBN 978-3-642-03502-9. PMID 21822822 .
- ^ Hu T, Li LF, Shen J, Zhang L, Cho CH (2015). “Inflammation chronique et cancer colorectal : le rôle du facteur de croissance endothélial vasculaire”. Conception pharmaceutique actuelle . 21 (21): 2960-2967. doi : 10.2174/1381612821666150514104244 . PMID 26004415 .
- ^ un bcd Triantaflidis JK, Nasioulas G, Kosmidis PA (juillet 2009). « Cancer colorectal et maladies inflammatoires de l’intestin : épidémiologie, facteurs de risque, mécanismes de cancérogenèse et stratégies de prévention ». Recherche anticancéreuse . 29 (7): 2727–2737. PMID 19596953 .
- ^ a b Bye WA, Nguyen TM, Parker CE, Jairath V, East JE (septembre 2017). “Stratégies de détection du cancer du côlon chez les patients atteints d’une maladie inflammatoire de l’intestin” . La base de données Cochrane des revues systématiques . 9 : CD000279. doi : 10.1002/14651858.cd000279.pub4 . PMC 6483622 . PMID 28922695 .
- ^ Juhn E, Khachemoune A (2010). “Syndrome de Gardner : manifestations cutanées, diagnostic différentiel et prise en charge”. Journal américain de dermatologie clinique . 11 (2): 117–122. doi : 10.2165/11311180-000000000-00000 . PMID 20141232 . S2CID 36836169 .
- ^ Demi E, Bercovich D, Rozen P (octobre 2009). “Polypose adénomateuse familiale” . Revue Orphanet des maladies rares . 4 : 22. doi : 10.1186/1750-1172-4-22 . PMC 2772987 . PMID 19822006 .
- ^ Möslein G, Pistorius S, Saeger HD, Schackert HK (mars 2003). “Chirurgie préventive du cancer du côlon dans la polypose adénomateuse familiale et le syndrome de cancer colorectal héréditaire sans polypose”. Archives de Chirurgie de Langenbeck . 388 (1): 9–16. doi : 10.1007/s00423-003-0364-8 . PMID 12690475 . S2CID 21385340 .
- ^ Mankaney G, Rouphael C, Burke CA (avril 2020). « Syndrome de la polypose dentelée » . Gastro-entérologie clinique et hépatologie . 18 (4): 777–779. doi : 10.1016/j.cgh.2019.09.006 . PMID 31520728 .
- ^ Fan C, Younis A, Bookhout CE, Crockett SD (mars 2018). “Gestion des polypes dentelés du côlon” . Options de traitement actuelles en gastroentérologie . 16 (1): 182–202. doi : 10.1007/s11938-018-0176-0 . PMC 6284520 . PMID 29445907 .
- ^ Bourdais R, Rousseau B, Pujals A, Boussion H, Joly C, Guillemin A, et al. (mai 2017). “Mutations du domaine de relecture de la polymérase : nouvelles opportunités pour l’immunothérapie dans le cancer colorectal hypermuté au-delà du déficit en MMR”. Revues critiques en oncologie/hématologie . 113 : 242–248. doi : 10.1016/j.critrevonc.2017.03.027 . PMID 28427513 .
- ^ Stein U, Walther W, Arlt F, Schwabe H, Smith J, Fichtner I, et al. (janvier 2009). “MACC1, un régulateur clé nouvellement identifié de la signalisation HGF-MET, prédit les métastases du cancer du côlon”. Médecine naturelle . 15 (1): 59–67. doi : 10.1038/nm.1889 . PMID 19098908 . S2CID 8854895 .
- ^ Stein U (2013) MACC1 – une nouvelle cible pour les cancers solides. Expert Opin Ther Cibles
- ^ Schuebel KE, Chen W, Cope L, Glöckner SC, Suzuki H, Yi JM, et al. (septembre 2007). “Comparaison de l’hyperméthylome d’ADN avec des mutations génétiques dans le cancer colorectal humain” . Génétique PLOS . 3 (9) : 1709-1723. doi : 10.1371/journal.pgen.0030157 . PMC 1988850 . PMID 17892325 .
- ^ “Quelle est la relation entre les juifs ashkénazes et le cancer colorectal?” . WebMD . Consulté le 17 octobre 2019 .
- ^ Ionov Y, Peinado MA, Malkhosyan S, Shibata D, Perucho M (juin 1993). “Les mutations somatiques omniprésentes dans des séquences répétées simples révèlent un nouveau mécanisme de carcinogenèse colique”. Nature . 363 (6429): 558–561. Bibcode : 1993Natur.363..558I . doi : 10.1038/363558a0 . PMID 8505985 . S2CID 4254940 .
- ^ Chakravarthi S, Krishnan B, Madhavan M (1999). “Apoptose et expression de p53 dans les néoplasmes colorectaux”. Indien J. Med. Rés . 86 (7): 95–102.
- ^ Abdul Khalek FJ, Gallicano GI, Mishra L (novembre 2010). “Cellules souches du cancer du côlon” . Recherche sur le cancer gastro-intestinal (Suppl 1) : S16–S23. PMC 3047031 . PMID 21472043 .
- ^ un bcd Markowitz SD, Bertagnolli MM (décembre 2009). “Origines moléculaires du cancer : Bases moléculaires du cancer colorectal” . Le New England Journal of Medicine . 361 (25): 2449–2460. doi : 10.1056/NEJMra0804588 . PMC 2843693 . PMID 20018966 .
- ^ Mehlen P, Fearon ER (août 2004). “Rôle du récepteur à dépendance DCC dans la pathogenèse du cancer colorectal”. Journal d’oncologie clinique . 22 (16): 3420–3428. doi : 10.1200/JCO.2004.02.019 . PMID 15310786 .
- ^ un bc Uhlen M, Zhang C , Lee S, Sjöstedt E, Fagerberg L, Bidkhori G, et al. (août 2017). “Un atlas de pathologie du transcriptome du cancer humain” . Sciences . 357 (6352): eaan2507. doi : 10.1126/science.aan2507 . PMID 28818916 .
- ^ Vogelstein B, Kinzler KW (août 2004). “Les gènes du cancer et les voies qu’ils contrôlent”. Médecine naturelle . 10 (8): 789–799. doi : 10.1038/nm1087 . PMID 15286780 . S2CID 205383514 .
- ^ un bc Muzny DM, Bainbridge MN, Chang K, Dinh HH, Drummond JA, Fowler G, et al. (Cancer Genome Atlas Network) (juillet 2012). “Caractérisation moléculaire complète du côlon humain et du cancer rectal” . Nature . 487 (7407): 330–337. Bibcode : 2012Natur.487..330T . doi : 10.1038/nature11252 . PMC 3401966 . PMID 22810696 .
- ^ Gatalica Z, Vranic S, Xiu J, Swensen J, Reddy S (juillet 2016). “Carcinome colorectal à haute instabilité microsatellite (MSI-H) : bref examen des biomarqueurs prédictifs à l’ère de la médecine personnalisée” . Cancer Familial . 15 (3): 405–412. doi : 10.1007/s10689-016-9884-6 . PMC 4901118 . PMID 26875156 .
- ^ un bc Ryan E, Sheahan K, Creavin B, Mohan HM, Winter DC (août 2017). « La valeur actuelle de la détermination de l’état de réparation des mésappariements du cancer colorectal : une justification pour les tests de routine ». Revues critiques en oncologie/hématologie . 116 : 38–57. doi : 10.1016/j.critrevonc.2017.05.006 . PMID 28693799 .
- ^ Hissong E, Crowe EP, Yantiss RK, Chen YT (novembre 2018). “Évaluer l’état de réparation de l’inadéquation du cancer colorectal à l’ère moderne : une enquête sur les pratiques actuelles et la réévaluation du rôle des tests d’instabilité des microsatellites” . Pathologie moderne . 31 (11): 1756-1766. doi : 10.1038/s41379-018-0094-7 . PMID 29955148 .
- ^ un bcd Grady WM , Markowitz SD (mars 2015). “La pathogenèse moléculaire du cancer colorectal et son application potentielle au dépistage du cancer colorectal” . Maladies et sciences digestives . 60 (3): 762–772. doi : 10.1007/s10620-014-3444-4 . PMC 4779895 . PMID 25492499 .
- ^ Abattage DP, Southwick HW, Smejkal W (septembre 1953). “Cancerisation de terrain dans l’épithélium squameux stratifié oral; implications cliniques d’origine multicentrique”. Cancer . 6 (5): 963–968. doi : 10.1002/1097-0142(195309)6:5<963::AID-CNCR2820060515>3.0.CO;2-Q . PMID 13094644 .
- ^ Giovannucci E, Ogino S (septembre 2005). “Méthylation de l’ADN, effets de champ et cancer colorectal” . Journal de l’Institut national du cancer . 97 (18): 1317–1319. doi : 10.1093/jnci/dji305 . PMID 16174847 .
- ^ Bernstein C, Bernstein H, Payne CM, Dvorak K, Garewal H (février 2008). “Défauts de terrain dans la progression vers les cancers du tractus gastro-intestinal” . Lettres cancéreuses . 260 (1–2) : 1–10. doi : 10.1016/j.canlet.2007.11.027 . PMC 2744582 . PMID 18164807 .
- ^ Nguyen H, Loustaunau C, Facista A, Ramsey L, Hassounah N, Taylor H, et al. (juillet 2010). “Pms2 déficient, ERCC1, Ku86, CcOI dans les défauts de champ au cours de la progression vers le cancer du côlon” . Journal of Visualized Experiments (41) : 1931. doi : 10.3791/1931 . PMC 3149991 . PMID 20689513 . vidéo de 28 minutes
- ^ Rubin H (mars 2011). “Champs et cancérisation des champs: les origines prénéoplasiques du cancer: les champs hyperplasiques asymptomatiques sont des précurseurs de la néoplasie, et leur progression vers les tumeurs peut être suivie par la densité de saturation en culture”. Bioessais . 33 (3): 224-231. doi : 10.1002/bies.201000067 . PMID 21254148 . S2CID 44981539 .
- ^ Tsao JL, Yatabe Y, Salovaara R, Järvinen HJ, Mecklin JP, Aaltonen LA, et al. (Février 2000). “Reconstruction génétique des antécédents individuels de tumeurs colorectales” . Actes de l’Académie nationale des sciences des États-Unis d’Amérique . 97 (3): 1236-1241. Bibcode : 2000PNAS…97.1236T . doi : 10.1073/pnas.97.3.1236 . PMC 15581 . PMID 10655514 .
- ^ un b Vogelstein B, Papadopoulos N, Velculescu VE, Zhou S, Diaz LA, Kinzler KW (mars 2013). « Paysages du génome du cancer » . Sciences . 339 (6127): 1546-1558. Bibcode : 2013Sci…339.1546V . doi : 10.1126/science.1235122 . PMC 3749880 . PMID 23539594 .
- ^ Bernstein, Carol; Nfonsam, Valentin ; Prasad, Anil Ramarao; Bernstein, Harris (15 mars 2013). “Défauts de champ épigénétiques dans la progression vers le cancer” . Journal mondial d’oncologie gastro-intestinale . 5 (3): 43–49. doi : 10.4251/wjgo.v5.i3.43 . ISSN 1948-5204 . PMC 3648662 . PMID 23671730 .
- ^ Lochhead P, Chan AT, Nishihara R, Fuchs CS, Beck AH, Giovannucci E, Ogino S (janvier 2015). “Effet de champ étiologique : réévaluation du concept d’effet de champ dans la prédisposition et la progression du cancer” . Pathologie moderne . 28 (1): 14-29. doi : 10.1038/modpathol.2014.81 . PMC 4265316 . PMID 24925058 .
- ^ Wilbur B, éd. (2009). Le monde de la cellule (7e éd.). San Fransisco, C.
- ^ Les pages de biologie de Kimball. “Oncogènes” Texte intégral gratuit
- ^ Kanwal R, Gupta S (avril 2012). “Modifications épigénétiques dans le cancer” . Génétique Clinique . 81 (4): 303–311. doi : 10.1111/j.1399-0004.2011.01809.x . PMC 3590802 . PMID 22082348 .
- ^ un b Schnekenburger M, Diederich M (mars 2012). “L’épigénétique offre de nouveaux horizons pour la prévention du cancer colorectal” . Rapports actuels sur le cancer colorectal . 8 (1): 66–81. doi : 10.1007/s11888-011-0116-z . PMC 3277709 . PMID 22389639 .
- ^ un bcd Lao VV , Grady WM (octobre 2011). “Epigénétique et cancer colorectal” . Revues naturelles. Gastro-entérologie et hépatologie . 8 (12): 686–700. doi : 10.1038/nrgastro.2011.173 . PMC 3391545 . PMID 22009203 .
- ^ Klutstein M, Nejman D, Greenfield R, Cedar H (juin 2016). “Méthylation de l’ADN dans le cancer et le vieillissement” . Recherche sur le cancer . 76 (12): 3446–3450. doi : 10.1158/0008-5472.CAN-15-3278 . PMID 27256564 .
- ^ Jacinto FV, Esteller M (juillet 2007). “Voies de mutation déclenchées par le silençage épigénétique dans le cancer humain” . Mutagenèse . 22 (4): 247-253. doi : 10.1093/mutage/gem009 . PMID 17412712 .
- ^ Lahtz C, Pfeifer GP (février 2011). “Modifications épigénétiques des gènes de réparation de l’ADN dans le cancer” . Tourillon de biologie cellulaire moléculaire . 3 (1): 51-58. doi : 10.1093/jmcb/mjq053 . PMC 3030973 . PMID 21278452 .
- ^ Bernstein C, Nfonsam V, Prasad AR, Bernstein H (mars 2013). “Défauts de champ épigénétiques dans la progression vers le cancer” . Journal mondial d’oncologie gastro-intestinale . 5 (3): 43–49. doi : 10.4251/wjgo.v5.i3.43 . PMC 3648662 . PMID 23671730 .
- ^ “Cancer colorectal” . La bibliothèque de concepts médicaux Lecturio . Consulté le 22 juillet 2021 .
- ^ Coppedè F, Lopomo A, Spisni R, Migliore L (janvier 2014). “Biomarqueurs génétiques et épigénétiques pour le diagnostic, le pronostic et le traitement du cancer colorectal” . Journal mondial de gastroentérologie . 20 (4): 943–956. doi : 10.3748/wjg.v20.i4.943 . PMC 3921546 . PMID 24574767 .
- ^ Guinney J, Dienstmann R, Wang X, de Reyniès A, Schlicker A, Soneson C, et al. (novembre 2015). “Les sous-types moléculaires consensus du cancer colorectal” . Médecine naturelle . 21 (11): 1350–1356. doi : 10.1038/nm.3967 . PMC 4636487 . PMID 26457759 .
- ^ Orouji E, Raman AT, Singh AK, Sorokin A, Arslan E, Ghosh AK, et al. (mai 2021). “La dynamique de l’état de la chromatine confère des stratégies thérapeutiques spécifiques dans les sous-types amplificateurs du cancer colorectal”. Intestin . doi : 10.1136/gutjnl-2020-322835 . PMC 8745382. PMID 34059508 . S2CID 235269540 .
- ^ un b “le Cancer colorectal” . La bibliothèque de concepts médicaux Lecturio . Consulté le 10 juillet 2021 .
- ^ Kang H, O’Connell JB, Leonardi MJ, Maggard MA, McGory ML, Ko CY (février 2007). “Tumeurs rares du côlon et du rectum : une revue nationale”. Journal international des maladies colorectales . 22 (2): 183–189. doi : 10.1007/s00384-006-0145-2 . PMID 16845516 . S2CID 34693873 .
- ^ “Termes et définitions équivalents du côlon, du rectosigmoïde et du rectum C180-C189, C199, C209, (exclut le lymphome et la leucémie M9590 – M9992 et le sarcome de Kaposi M9140) – Règles de la tumeur solide du côlon 2018. Mise à jour de juillet 2019” (PDF) . Institut national du cancer .
- ^ “Types de cancer colorectal” . Centres de traitement du cancer d’Amérique . 4 octobre 2018 . Consulté le 16 janvier 2020 .
- ^ Di Como JA, Mahendraraj K, Lau CS, Chamberlain RS (octobre 2015). “Carcinome adénosquameux du côlon et du rectum: une étude de résultats cliniques basée sur la population impliquant 578 patients de la base de données Surveillance Epidemiology and End Result (SEER) (1973–2010)”. Journal du Collège américain des chirurgiens . 221 (4): 56. doi : 10.1016/j.jamcollsurg.2015.08.044 .
- ^ Whiteside G, Munglani R (septembre 1998). “Triple étiquetage TUNEL, Hoechst et immunohistochimie : une méthode améliorée pour la détection de l’apoptose dans les coupes de tissus – une mise à jour”. Recherche sur le cerveau. Protocoles de recherche sur le cerveau . 3 (1): 52–53. doi : 10.1016/s1385-299x(98)00020-8 . PMID 9767106 .
- ^ “Mise en scène TNM du carcinome colorectal (AJCC 8e édition)” . www.pathologyoutlines.com . Consulté le 24 février 2019 .
- ^ Parkin DM, Boyd L, Walker LC (décembre 2011). “16. La fraction du cancer attribuable au mode de vie et aux facteurs environnementaux au Royaume-Uni en 2010” . Journal britannique du cancer . 105 (S2) : S77–S81. doi : 10.1038/bjc.2011.489 . PMC 3252065 . PMID 22158327 .
- ^ Cherche D (2006). Épidémiologie et prévention du cancer (3 éd.). Presse universitaire d’Oxford. p. 809. ISBN 978-0199747979. Archivé de l’original le 28 septembre 2015.
- ^ Rennert G (2007). Prévention du cancer . Springer. p. 179. ISBN 978-3540376965. Archivé de l’original le 3 octobre 2015.
- ^ un b “l’Aperçu de Prévention de Cancer Colorectal” . Institut national du cancer . 1 mars 2018 . Consulté le 26 octobre 2018 .
- ^ “Prévention du cancer” . Organisation mondiale de la santé . Consulté le 27 octobre 2018 .
- ^ Lauby-Secretan B, Scoccianti C, Loomis D, Grosse Y, Bianchini F, Straif K (août 2016). « L’adiposité corporelle et le cancer – Point de vue du groupe de travail du CIRC » . Le New England Journal of Medicine . 375 (8) : 794–798. doi : 10.1056/nejmsr1606602 . PMC 6754861 . PMID 27557308 .
- ^ “Cancer colorectal – Facteurs de risque et prévention” . 25 juin 2012.
- ^ Willett WC (2014). « Régime, nutrition et cancer : quel avenir pour la santé publique ? » . Dans Stewart BW, Wild CP (éd.). Rapport mondial sur le cancer . Centre international de recherche sur le cancer, Organisation mondiale de la santé. p. 432–435. ISBN 978-92-832-0443-5.
- ^ un b Willett WC, Clé T, Romieu I (2014). “Chapitre 2.6 : Alimentation, obésité et activité physique” . Dans Stewart BW, Wild CP (éd.). Rapport mondial sur le cancer . Centre international de recherche sur le cancer, Organisation mondiale de la santé. p. 124–133. ISBN 978-92-832-0443-5. Plusieurs grandes études de cohorte prospectives sur les fibres alimentaires et le risque de cancer du côlon n’ont pas soutenu une association, bien qu’une relation inverse ait été observée dans la grande étude prospective européenne sur le cancer et la nutrition (EPIC) et une méta-analyse récente. La variation des résultats des études prospectives doit être mieux comprise ; les fibres alimentaires sont complexes et hétérogènes, et la relation avec le cancer colorectal pourrait différer selon la source alimentaire. (p.127)
- ^ “Description de la preuve de la prévention du cancer colorectal” . Institut national du cancer . 1 mars 2018 . Consulté le 26 octobre 2018 .
- ^ “Cancer colorectal” .
- ^ Reynolds A, Mann J, Cummings J, Winter N, Mete E, Te Morenga L (février 2019). “Qualité des glucides et santé humaine : une série de revues systématiques et de méta-analyses” . Lancette . 393 (10170): 434–445. doi : 10.1016/S0140-6736(18)31809-9 . PMID 30638909 . S2CID 58632705 .
- ^ Chanson M, Chan AT (janvier 2019). “Facteurs environnementaux, microbiote intestinal et prévention du cancer colorectal” . Gastro-entérologie clinique et hépatologie . 17 (2): 275–289. doi : 10.1016/j.cgh.2018.07.012 . PMC 6314893 . PMID 30031175 . Malgré l’hypothèse de longue date selon laquelle une alimentation riche en fibres peut protéger contre le cancer colorectal… les études épidémiologiques associant l’apport en fibres alimentaires au risque ultérieur de cancer colorectal ont donné des résultats incohérents… Néanmoins, sur la base des preuves existantes, le rapport d’expert le plus récent de le Fonds mondial de recherche sur le cancer et l’Institut américain de recherche sur le cancer en 2017 concluent qu’il existe des preuves probables
- ^ Pérez-Cueto FJ, Verbeke W (avril 2012). “Implications pour les consommateurs de la mise à jour permanente du WCRF sur le cancer colorectal”. Sciences de la viande . 90 (4): 977–978. doi : 10.1016/j.meatsci.2011.11.032 . PMID 22196090 .
- ^ Harriss DJ, Atkinson G, Batterham A, George K, Cable NT, Reilly T, et al. (septembre 2009). “Facteurs de style de vie et risque de cancer colorectal (2): une revue systématique et une méta-analyse des associations avec l’activité physique pendant les loisirs”. Maladie colorectale . 11 (7): 689–701. doi : 10.1111/j.1463-1318.2009.01767.x . PMID 19207713 . S2CID 8026021 .
- ^ Robsahm TE, Aagnes B, Hjartåker A, Langseth H, Bray FI, Larsen IK (novembre 2013). “Indice de masse corporelle, activité physique et cancer colorectal par sous-sites anatomiques : une revue systématique et une méta-analyse d’études de cohorte”. Journal européen de prévention du cancer . 22 (6): 492–505. doi : 10.1097/CEJ.0b013e328360f434 . PMID 23591454 . S2CID 24764995 .
- ^ Kyu HH, Bachman VF, Alexander LT, Mumford JE, Afshin A, Estep K, et al. (août 2016). “Activité physique et risque de cancer du sein, de cancer du côlon, de diabète, de cardiopathie ischémique et d’accidents vasculaires cérébraux ischémiques : examen systématique et méta-analyse dose-réponse pour l’étude Global Burden of Disease Study 2013” . BMJ . 354 : i3857. doi : 10.1136/bmj.i3857 . PMC 4979358 . PMID 27510511 .
- ^ Biswas A, Oh PI, Faulkner GE, Bajaj RR, Silver MA, Mitchell MS, Alter DA (janvier 2015). “Le temps sédentaire et son association avec le risque d’incidence de la maladie, de mortalité et d’hospitalisation chez les adultes: une revue systématique et une méta-analyse”. Annales de médecine interne . 162 (2): 123–132. doi : 10.7326/M14-1651 . PMID 25599350 . S2CID 7256176 .
- ^ Cooper K, Squires H, Carroll C, Papaioannou D, Booth A, Logan RF, et al. (juin 2010). « Chimioprévention du cancer colorectal : revue systématique et évaluation économique » . Évaluation des technologies de la santé . 14 (32): 1–206. doi : 10.3310/hta14320 . PMID 20594533 .
- ^ Emilsson L, Holme Ø, Bretthauer M, Cook NR, Buring JE, Løberg M, et al. (janvier 2017). “Revue systématique avec méta-analyse : l’efficacité comparative de l’aspirine par rapport au dépistage pour la prévention du cancer colorectal” . Pharmacologie Alimentaire & Thérapeutique . 45 (2): 193–204. doi : 10.1111/apt.13857 . PMID 27859394 .
- ^ Bibbins-Domingo K (juin 2016). “Utilisation d’aspirine pour la prévention primaire des maladies cardiovasculaires et du cancer colorectal : déclaration de recommandation du groupe de travail sur les services de prévention des États-Unis” . Annales de médecine interne . 164 (12): 836–845. doi : 10.7326/M16-0577 . PMID 27064677 .
- ^ Agence pour la recherche et la qualité des soins de santé. “Aspirine ou anti-inflammatoires non stéroïdiens pour la prévention primaire du cancer colorectal” . Département américain de la santé et des services sociaux. Archivé de l’original le 5 janvier 2016. 2010/2011
- ^ Weingarten MA, Zalmanovici A, Yaphe J (janvier 2008). “Supplémentation alimentaire en calcium pour prévenir le cancer colorectal et les polypes adénomateux” . La base de données Cochrane des revues systématiques . 2010 (1) : CD003548. doi : 10.1002/14651858.CD003548.pub4 . PMC 8719254 . PMID 18254022 .
- ^ Ma Y, Zhang P, Wang F, Yang J, Liu Z, Qin H (octobre 2011). « Association entre la vitamine D et le risque de cancer colorectal : une revue systématique des études prospectives ». Journal d’oncologie clinique . 29 (28): 3775–3782. doi : 10.1200/JCO.2011.35.7566 . PMID 21876081 .
- ^ Yin L, Grandi N, Raum E, Haug U, Arndt V, Brenner H (2011). “Méta-analyse: vitamine D sérique et risque d’adénome colorectal”. Médecine Préventive . 53 (1–2) : 10–16. doi : 10.1016/j.ypmed.2011.05.013 . PMID 21672549 .
- ^ “Que puis-je faire pour réduire mon risque de cancer colorectal?” . Centres de contrôle et de prévention des maladies . 2 avril 2014. Archivé de l’original le 26 février 2015 . Consulté le 5 mars 2015 .
- ^ un b He J, Efron JE (2011). “Dépistage du cancer colorectal”. Les progrès de la chirurgie . 45 : 31–44. doi : 10.1016/j.yasu.2011.03.006 . manche : 2328/11906 . PMID 21954677 .
- ^ Siegel RL, Ward EM, Jemal A (mars 2012). “Tendances des taux d’incidence du cancer colorectal aux États-Unis par localisation et stade de la tumeur, 1992-2008” . Épidémiologie du cancer, biomarqueurs et prévention . 21 (3): 411–416. doi : 10.1158/1055-9965.EPI-11-1020 . PMID 22219318 .
- ^ Swartz AW, Eberth JM, Josey MJ, Strayer SM (octobre 2017). “Réanalyse de la mortalité toutes causes confondues dans le rapport de preuves 2016 du groupe de travail sur les services préventifs des États-Unis sur le dépistage du cancer colorectal” . Annales de médecine interne . 167 (8): 602–603. doi : 10.7326/M17-0859 . PMC 5823607 . PMID 28828493 .
- ^ Hewitson P, Glasziou P, Watson E, Towler B, Irwig L (juin 2008). “Revue systématique Cochrane du dépistage du cancer colorectal à l’aide du test de sang occulte fécal (hemoccult) : une mise à jour”. Le Journal américain de gastroentérologie . 103 (6): 1541-1549. PMID 18479499 .
- ^ Lee JK, Liles EG, Bent S, Levin TR, Corley DA (février 2014). “Exactitude des tests immunochimiques fécaux pour le cancer colorectal : revue systématique et méta-analyse” . Annales de médecine interne . 160 (3): 171. doi : 10.7326/M13-1484 . PMC 4189821 . PMID 24658694 .
- ^ un b Qaseem A, Crandall CJ, Mustafa RA, Hicks LA, Wilt TJ, Forciea MA, et al. (novembre 2019). “Dépistage du cancer colorectal chez les adultes asymptomatiques à risque moyen : une déclaration d’orientation de l’American College of Physicians” . Annales de médecine interne . 171 (9): 643–654. doi : 10.7326/M19-0642 . PMC 8152103 . PMID 31683290 .
- ^ Wolf AM, Fontham ET, Church TR, Flowers CR, Guerra CE, LaMonte SJ, et al. (juillet 2018). “Dépistage du cancer colorectal chez les adultes à risque moyen : mise à jour des lignes directrices 2018 de l’American Cancer Society” . CA : Un journal sur le cancer pour les cliniciens . 68 (4): 250–281. doi : 10.3322/caac.21457 . PMID 29846947 .
- ^ “Dépistage du cancer colorectal” . Groupe de travail américain sur les services préventifs . 2008. Archivé de l’original le 7 février 2015 . Consulté le 19 décembre 2011 .
- ^ un b Brenner H, Stock C, Hoffmeister M (avril 2014). “Effet de la sigmoïdoscopie de dépistage et de la coloscopie de dépistage sur l’incidence et la mortalité du cancer colorectal : examen systématique et méta-analyse d’essais contrôlés randomisés et d’études observationnelles” . BMJ . 348 (avr09 1): g2467. doi : 10.1136/bmj.g2467 . PMC 3980789 . PMID 24922745 .
- ^ Association gastro-entérologique américaine . “Cinq choses que les médecins et les patients devraient remettre en question” (PDF) . Choisir avec soin : une initiative de la Fondation ABIM . Archivé de l’original (PDF) le 9 août 2012 . Consulté le 17 août 2012 .
- ^ Winawer S, Fletcher R, Rex D, Bond J, Burt R, Ferrucci J, et al. (février 2003). “Dépistage et surveillance du cancer colorectal : directives cliniques et justification – Mise à jour basée sur de nouvelles preuves”. Gastroentérologie . 124 (2): 544-560. doi : 10.1053/gast.2003.50044 . PMID 12557158 . S2CID 29354772 .
- ^ Qaseem A, Denberg TD, Hopkins RH, Humphrey LL, Levine J, Sweet DE, Shekelle P (mars 2012). “Dépistage du cancer colorectal : une déclaration d’orientation de l’American College of Physicians” . Annales de médecine interne . 156 (5): 378–386. doi : 10.7326/0003-4819-156-5-201203060-00010 . PMID 22393133 .
- ^ Tang V, Boscardin WJ, Stijacic-Cenzer I, Lee SJ (avril 2015). “Il est temps de bénéficier du dépistage du cancer colorectal : méta-analyse de survie des essais de sigmoïdoscopie flexibles” . BMJ . 350 : h1662. doi : 10.1136/bmj.h1662 . PMC 4399600 . PMID 25881903 .
- ^ un b Bacchus CM, Dunfield L, Gorber SC, Holmes NM, Birtwhistle R, Dickinson JA, Lewin G, Singh H, Klarenbach S, Mai V, Tonelli M (mars 2016). “Recommandations sur le dépistage du cancer colorectal en soins primaires” . JAMC . 188 (5): 340–348. doi : 10.1503/cmaj.151125 . PMC 4786388 . PMID 26903355 .
- ^ “Programme de dépistage du cancer de l’intestin du NHS” . cancerscreening.nhs.uk . Archivé de l’original le 29 novembre 2014.
- ^ “Accueil – Cancer de l’intestin Australie” . bowelcanceraustralia.org . Archivé de l’original le 24 décembre 2014.
- ^ “Bevolkingsonderzoek darmkanker” . rivm.nl . Archivé de l’original le 17 décembre 2014.
- ^ Tepus M, Yau TO (juillet 2020). « Dépistage non invasif du cancer colorectal : un aperçu » . Tumeurs gastro-intestinales . 7 (3) : 62–73. doi : 10.1159/000507701 . PMC 7445682 . PMID 32903904 .
- ^ Stein A, Atanackovic D, Bokemeyer C (septembre 2011). “Normes actuelles et nouvelles tendances dans le traitement primaire du cancer colorectal”. Journal européen du cancer . 47 (Suppl 3) : S312–S314. doi : 10.1016/S0959-8049(11)70183-6 . PMID 21943995 .
- ^ Chiorean EG, Nandakumar G, Fadelu T, Temin S, Alarcon-Rozas AE, Bejarano S, et al. (mars 2020). “Traitement des patients atteints d’un cancer colorectal à un stade avancé : ligne directrice stratifiée par les ressources de l’ASCO” . Oncologie mondiale JCO . 6 (6): 414–438. doi : 10.1200/JGO.19.00367 . PMC 7124947 . PMID 32150483 .
- ^ un b McCarthy K, Pearson K, Fulton R, Hewitt J, et autres. (Groupe Cochrane sur le cancer colorectal) (décembre 2012). “La chimioradiothérapie préopératoire pour le cancer rectal localement avancé non métastatique”. La base de données Cochrane des revues systématiques . 12 : CD008368. doi : 10.1002/14651858.CD008368.pub2 . PMID 23235660 .
- ^ un b “Le cancer colorectal (côlon)” . Clinique de Cleveland . Consulté le 9 juillet 2021 .
- ^ Böckelman C, Engelmann BE, Kaprio T, Hansen TF, Glimelius B (janvier 2015). « Risque de récidive chez les patients atteints de cancer du côlon de stade II et III : une revue systématique et une méta-analyse de la littérature récente » . Acta Oncologica . 54 (1): 5–16. doi : 10.3109/0284186x.2014.975839 . PMID 25430983 .
- ^ “La chimiothérapie du cancer colorectal métastatique”. Prescrire International . 19 (109): 219-224. Octobre 2010. PMID 21180382 .
- ^ Fakih MG (juin 2015). « Cancer colorectal métastatique : état actuel et orientations futures » . Journal d’oncologie clinique . 33 (16): 1809–1824. doi : 10.1200/JCO.2014.59.7633 . PMID 25918280 .
- ^ Shaib W, Mahajan R, El-Rayes B (septembre 2013). “Marqueurs de résistance à la thérapie anti-EGFR dans le cancer colorectal” . Journal d’oncologie gastro-intestinale . 4 (3): 308–318. doi : 10.3978/j.issn.2078-6891.2013.029 . PMC 3712296 . PMID 23997942 .
- ^ Yau TO (octobre 2019). “Traitement de précision du cancer colorectal : maintenant et demain” . Ouvert HGJ . 3 (5): 361–369. doi : 10.1002/jgh3.12153 . PMC 6788378 . PMID 31633039 .
- ^ Sugarbaker PH, Van der Speeten K (février 2016). “Technologie chirurgicale et pharmacologie de la chimiothérapie hyperthermique périopératoire” . Journal d’oncologie gastro-intestinale . 7 (1) : 29–44. doi : 10.3978/j.issn.2078-6891.2015.105 . PMC 4754302 . PMID 26941982 .
- ^ Segura-Sampedro JJ, Morales-Soriano R (août 2020). “L’HIPEC prophylactique avec l’oxaliplatine pourrait être bénéfique dans le cancer T4 et le cancer du côlon perforé : une autre interprétation possible des résultats du COLOPEC” . Revista Española de Enfermedades Digestivas . 112 (8): 666. doi : 10.17235/reed.2020.6755/2019 . PMID 32686435 .
- ^ Esquivel J, Sticca R, Sugarbaker P, Levine E, Yan TD, Alexander R, et al. (janvier 2007). “Chirurgie cytoréductrice et chimiothérapie intrapéritonéale hyperthermique dans la gestion des tumeurs malignes de la surface péritonéale d’origine colique: une déclaration de consensus. Société d’oncologie chirurgicale”. Annales d’oncologie chirurgicale . 14 (1): 128–133. doi : 10.1245/s10434-006-9185-7 . PMID 17072675 . S2CID 21282326 .
- ^ DeVita VT, Lawrence TS, Rosenberg SA (2008). DeVita, Hellman et le cancer de Rosenberg : principes et pratique de l’oncologie . Lippincott Williams & Wilkins. pp. 1258–. ISBN 978-0-7817-7207-5.
- ^ un b Feeney G, Sehgal R, Sheehan M, Hogan A, Regan M, Joyce M, Kerin M (septembre 2019). “La radiothérapie néoadjuvante pour la gestion du cancer du rectum” . Journal mondial de gastroentérologie . 25 (33): 4850–4869. doi : 10.3748/wjg.v25.i33.4850 . PMC 6737323 . PMID 31543678 .
- ^ Li Y, Wang J, Ma X, Tan L, Yan Y, Xue C, et al. (2016). “Un examen de la chimioradiothérapie néoadjuvante pour le cancer rectal localement avancé” . Journal international des sciences biologiques . 12 (8): 1022-1031. doi : 10.7150/ijbs.15438 . PMC 4971740 . PMID 27489505 .
- ^ Cao C, Wang D, Tian DH, Wilson-Smith A, Huang J, Rimner A (décembre 2019). “Une revue systématique et une méta-analyse de la radiothérapie corporelle stéréotaxique pour les métastases pulmonaires colorectales” . Journal des maladies thoraciques . 11 (12): 5187–5198. doi : 10.21037/jtd.2019.12.12 . PMC 6988072 . PMID 32030236 .
- ^ un b Boland PM, Ma WW (mai 2017). “Immunothérapie du cancer colorectal” . Cancers . 9 (5): 50. doi : 10.3390/cancers9050050 . PMC 5447960 . PMID 28492495 .
- ^ un bc Syn NL, Teng MW, Mok TS, Soo RA (décembre 2017). “Résistance de novo et acquise au ciblage des points de contrôle immunitaire”. Le Lancet. Oncologie . 18 (12) : e731–e741. doi : 10.1016/s1470-2045(17)30607-1 . PMID 29208439 .
- ^ “La FDA accorde une approbation accélérée au pembrolizumab pour la première indication agnostique de tissu/site” . Administration américaine des aliments et médicaments . 9 février 2019.
- ^ “Soins palliatifs ou de soutien” . Société américaine du cancer. Archivé de l’original le 21 août 2014 . Consulté le 20 août 2014 .
- ^ “Opinion clinique provisoire d’ASCO : L’intégration des soins palliatifs dans les soins d’oncologie standard” . ASCO. Archivé de l’original le 21 août 2014 . Récupéré le 20 août 2014 .
- ^ Higginson IJ, Evans CJ (septembre-octobre 2010). “Quelle est la preuve que les équipes de soins palliatifs améliorent les résultats pour les patients atteints de cancer et leurs familles?”. Journal du cancer . 16 (5): 423–435. doi : 10.1097/PPO.0b013e3181f684e5 . PMID 20890138 . S2CID 39881122 .
- ^ Wasserberg N, Kaufman HS (décembre 2007). “Palliation du cancer colorectal”. Oncologie chirurgicale . 16 (4): 299–310. doi : 10.1016/j.suronc.2007.08.008 . PMID 17913495 .
- ^ Amersi F, Stamos MJ, Ko CY (juillet 2004). “Soins palliatifs du cancer colorectal”. Cliniques d’oncologie chirurgicale d’Amérique du Nord . 13 (3): 467–477. doi : 10.1016/j.soc.2004.03.002 . PMID 15236729 .
- ^ un b “le Réseau de Cancer Complet national” (PDF) . nccn.org . Archivé (PDF) de l’original le 25 mars 2009.
- ^ un b Desch CE, Benson AB, Somerfield MR, Flynn PJ, Krause C, Loprinzi CL, et al. (novembre 2005). “Surveillance du cancer colorectal : mise à jour 2005 d’une directive de pratique de l’American Society of Clinical Oncology”. Journal d’oncologie clinique . 23 (33): 8512–8519. doi : 10.1200/JCO.2005.04.0063 . PMID 16260687 .
- ^ Jeffery M, Hickey BE, Hider PN (septembre 2019). “Stratégies de suivi des patients traités pour un cancer colorectal non métastatique” . La base de données Cochrane des revues systématiques . 2019 (9) : CD002200. doi : 10.1002/14651858.CD002200.pub4 . PMC 6726414 . PMID 31483854 .
- ^ Betof AS, Dewhirst MW , Jones LW (mars 2013). “Effets et mécanismes potentiels de l’entraînement physique sur la progression du cancer : une perspective translationnelle” . Cerveau, comportement et immunité . 30 (suppl.) : S75–S87. doi : 10.1016/j.bbi.2012.05.001 . PMC 3638811 . PMID 22610066 .
- ^ un b Ballard-Barbash R, Friedenreich CM, Courneya KS, Siddiqi SM, McTiernan A, Alfano CM (juin 2012). “Activité physique, biomarqueurs et résultats de la maladie chez les survivants du cancer : une revue systématique” . Journal de l’Institut national du cancer . 104 (11): 815–840. doi : 10.1093/jnci/djs207 . PMC 3465697 . PMID 22570317 .
- ^ un b McGettigan M, Cardwell CR, Cantwell MM, Tully MA (mai 2020). “Interventions d’activité physique pour la santé physique et mentale liée à la maladie pendant et après le traitement chez les personnes atteintes d’un cancer colorectal non avancé” . La base de données Cochrane des revues systématiques . 2020 (5) : CD012864. doi : 10.1002/14651858.cd012864.pub2 . PMC 7196359 . PMID 32361988 .
- ^ Osterman E, Glimelius B (septembre 2018). “Risque de récidive après la mise en scène, la chirurgie et la pathologie du cancer du côlon à jour : analyse de l’ensemble de la population suédoise” . Maladies du côlon et du rectum . 61 (9): 1016-1025. doi : 10.1097/dcr.0000000000001158 . PMID 30086050 . S2CID 51934598 .
- ^ Zacharakis M, Xynos ID, Lazaris A, Smaro T, Kosmas C, Dokou A, et al. (février 2010). “Prédicteurs de survie dans le cancer colorectal métastatique de stade IV” . Recherche anticancéreuse . 30 (2): 653–660. PMID 20332485 .
- ^ Encadré 3-1, Page 107 dans: Agabegi ED, Agabegi SS (2008). Step-Up to Medicine (Série Step-Up) . Hagerstwon, MD : Lippincott Williams & Wilkins. ISBN 978-0-7817-7153-5.
- ^ Hong Y (30 juin 2020). « Étude clinique de l’opération du cancer colorectal : Analyse de survie » . Journal coréen d’oncologie clinique 2020 . 16 : 3–8. doi : 10.14216/kjco.20002 . Consulté le 9 mai 2021 .
- ^ “Taux de survie sur cinq ans” . Institut national du cancer . Consulté le 9 mai 2021 .
- ^ Xu Z, Becerra AZ, Fleming FJ, Aquina CT, Dolan JG, Monson JR, et al. (octobre 2019). “Traitements pour le cancer du côlon de stade IV et la survie globale”. Le Journal de la recherche chirurgicale . 242 : 47–54. doi : 10.1016/j.jss.2019.04.034 . PMID 31071604 . S2CID 149443256 .
- ^ Drageset S, Lindstrøm TC, Underlid K (avril 2016). ” “Je dois juste passer à autre chose : expériences et réflexions d’adaptation des femmes après leur première année après la chirurgie primaire du cancer du sein”. European Journal of Oncology Nursing . 21 : 205–211. doi : 10.1016/j.ejon.2015.10.005 . PMID 26521054 .
- ^ Restivo A, Zorcolo L, D’Alia G, Cocco F, Cossu A, Scintu F, Casula G (février 2016). “Risque de complications et d’altérations fonctionnelles à long terme après excision locale des tumeurs rectales avec microchirurgie endoscopique transanale (TEM)”. Journal international des maladies colorectales . 31 (2): 257-266. doi : 10.1007/s00384-015-2371-y . PMID 26298182 . S2CID 29087556 .
- ^ Bregendahl S, Emmertsen KJ, Lindegaard JC, Laurberg S (janvier 2015). “Dysfonctionnement urinaire et sexuel chez les femmes après résection avec et sans radiothérapie préopératoire pour le cancer du rectum : une étude transversale basée sur la population”. Maladie colorectale . 17 (1): 26–37. doi : 10.1111/codi.12758 . PMID 25156386 . S2CID 42069306 .
- ^ Ramirez M, McMullen C, Grant M, Altschuler A, Hornbrook MC, Krouse RS (décembre 2009). “Comprendre le sexe dans un corps reconfiguré : expériences de femmes survivantes du cancer colorectal avec stomies” . Femmes & Santé . 49 (8): 608–624. doi : 10.1080/03630240903496093 . PMC 2836795 . PMID 20183104 .
- ^ Steele N, Haigh R, Knowles G, Mackean M (septembre 2007). “Dépistage de l’antigène carcinoembryonnaire (ACE) dans le suivi du cancer colorectal : qu’en pensent les patients ?” . Revue médicale postdoctorale . 83 (983): 612–614. doi : 10.1136/pgmj.2007.059634 . PMC 2600007 . PMID 17823231 .
- ^ McGeechan GJ, Byrnes K, Campbell M, Carthy N, Eberhardt J, Paton W, et al. (janvier 2021). “Une revue systématique et une synthèse qualitative de l’expérience de vivre avec le cancer colorectal en tant que maladie chronique” . Psychologie & Santé : 1–25. doi : 10.1080/08870446.2020.1867137 . PMID 33499649 . S2CID 231771176 .
- ^ Lozano R, Naghavi M, Foreman K, Lim S, Shibuya K, Aboyans V, et al. (Décembre 2012). “Mortalité mondiale et régionale de 235 causes de décès pour 20 groupes d’âge en 1990 et 2010: une analyse systématique pour l’étude Global Burden of Disease Study 2010”. Lancette . 380 (9859): 2095–2128. doi : 10.1016/S0140-6736(12)61728-0 . hdl : 10536/DRO/DU:30050819 . PMID 23245604 . S2CID 1541253 .
- ^ OMS (février 2010). “Cancer” . Organisation mondiale de la santé. Archivé de l’original le 29 décembre 2010 . Consulté le 5 janvier 2011 .
- ^ Merika E, Saif MW, Katz A, Syrigos K, Syrigos C, Morse M (2010). “Examen. Vaccins contre le cancer du côlon : une mise à jour”. In vivo . 24 (5): 607–628. PMID 20952724 .
- ^ Ferlay J, Shin HR, Bray F, Forman D, Mathers C, Parkin DM (2010). “Incidence, mortalité et prévalence du cancer colorectal dans le monde en 2008 – Résumé” . Archivé de l’original le 17 octobre 2012. ; “GLOBOCAN 2008 v2.0, Incidence et mortalité du cancer dans le monde : IARC CancerBase No. 10” . Lyon, France : Centre international de recherche sur le cancer. Archivé de l’original le 8 mai 2011.
- ^ un b “Le cancer colorectal : Statistiques” . Cancer.net, Société américaine d’oncologie clinique. Février 2022 . Consulté le 13 mai 2022 .
- ^ “Cancer de l’intestin | À propos du cancer de l’intestin | Cancer Research UK” . www.cancerresearchuk.org . Archivé de l’original le 9 mars 2017 . Consulté le 12 mai 2017 .
- ^ Cancer en Australie: un aperçu, 2014. Série Cancer No 90. Cat. N° CAN 88 . Canberra : Institut australien de la santé et du bien-être. 2014. ISBN 978-1-74249-677-1.
- ^ Cancer en Papouasie-Nouvelle-Guinée: un aperçu, 2016. Série Cancer n ° 176. Cat. N° CAN 88 . Département de la santé de Papouasie-Nouvelle-Guinée. 2016.
- ^ Rehemtulla A (décembre 2010). “Dinosaures et civilisations anciennes : réflexions sur le traitement du cancer” . Néoplasie . 12 (12): 957–968. doi : 10.1593/neo.101588 . PMC 3003131 . PMID 21170260 .
- ^ Zhong L, Zhang X, Covasa M (juin 2014). “Rôles émergents des bactéries lactiques dans la protection contre le cancer colorectal” . Journal mondial de gastroentérologie . 20 (24): 7878–7886. doi : 10.3748/wjg.v20.i24.7878 . PMC 4069315 . PMID 24976724 .
- ^ Golovko D, Kedrin D, Yilmaz ÖH, Roper J (2015). “Modèles de cancer colorectal pour la découverte de nouveaux médicaments” . Avis d’expert sur la découverte de médicaments . 10 (11): 1217–1229. doi : 10.1517/17460441.2015.1079618 . PMC 4872297 . PMID 26295972 .
- ^ Oh BY, Hong HK, Lee WY, Cho YB (février 2017). “Modèles animaux de cancer colorectal avec métastases hépatiques”. Lettres cancéreuses . 387 : 114–120. doi : 10.1016/j.canlet.2016.01.048 . PMID 26850374 .
- ^ Evans JP, Sutton PA, Winiarski BK, Fenwick SW, Malik HZ, Vimalachandran D, et al. (février 2016). « Des souris aux hommes : Modèles murins de cancer colorectal à utiliser dans la recherche translationnelle ». Revues critiques en oncologie/hématologie . 98 : 94–105. doi : 10.1016/j.critrevonc.2015.10.009 . PMID 26558688 .
- ^ “Atlas du cancer colorectal” . Archivé de l’original le 13 janvier 2016.
Liens externes
| Wikimedia Commons a des médias liés au cancer colorectal . |
- Cancer colorectal à Curlie
Portails : ![]()
![]() La biologie
La biologie ![]()
![]() Médecine
Médecine
