Molécule
Une molécule est un groupe de deux ou plusieurs atomes maintenus ensemble par des forces attractives appelées liaisons chimiques ; selon le contexte, le terme peut ou non inclure des ions qui satisfont à ce critère. [4] [5] [6] [7] [8] En physique quantique , en chimie organique et en biochimie , la distinction avec les ions est abandonnée et la molécule est souvent utilisée pour désigner les ions polyatomiques .
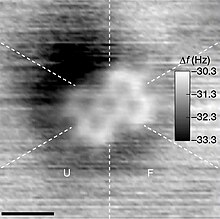 Image de microscopie à force atomique (AFM) d’une molécule de PTCDA , dans laquelle les cinq anneaux à six carbones sont visibles. [1]
Image de microscopie à force atomique (AFM) d’une molécule de PTCDA , dans laquelle les cinq anneaux à six carbones sont visibles. [1]  Une image de Microscopie à effet tunnel de molécules de pentacène , constituées de chaînes linéaires de cinq anneaux de carbone. [2]
Une image de Microscopie à effet tunnel de molécules de pentacène , constituées de chaînes linéaires de cinq anneaux de carbone. [2]  Image AFM du 1,5,9-trioxo-13-azatriangulène et de sa structure chimique. [3]
Image AFM du 1,5,9-trioxo-13-azatriangulène et de sa structure chimique. [3]
Dans la théorie cinétique des gaz , le terme molécule est souvent utilisé pour toute particule gazeuse quelle que soit sa composition. Cela assouplit l’exigence qu’une molécule contienne deux atomes ou plus, puisque les gaz nobles sont des atomes individuels. [9]
Une molécule peut être homonucléaire , c’est-à-dire qu’elle est constituée d’atomes d’un élément chimique , par exemple deux atomes dans la molécule d’oxygène (O 2 ); ou il peut être Hétéronucléaire , un composé chimique composé de plus d’un élément, par exemple l’eau (deux atomes d’hydrogène et un atome d’oxygène ; H 2 O).
Les atomes et les complexes reliés par des Interactions non covalentes , telles que des liaisons hydrogène ou des liaisons ioniques , ne sont généralement pas considérés comme des molécules uniques. [dix]
Les molécules en tant que composants de la matière sont courantes. Ils constituent également la majeure partie des océans et de l’atmosphère. La plupart des substances organiques sont des molécules. Les substances de la vie sont des molécules, par exemple les protéines, les acides aminés qui les composent, les acides nucléiques (ADN et ARN), les sucres, les glucides, les graisses et les vitamines. Les minéraux nutritifs sont généralement des composés ioniques, ce ne sont donc pas des molécules, par exemple le sulfate de fer.
Cependant, la majorité des substances solides familières sur Terre sont constituées en partie ou en totalité de cristaux ou de composés ioniques, qui ne sont pas constitués de molécules. Ceux-ci incluent tous les minéraux qui composent la substance de la Terre, le sable, l’argile, les cailloux, les roches, les rochers, le substratum rocheux , l’ intérieur en fusion et le noyau de la Terre . Tous ces éléments contiennent de nombreuses liaisons chimiques, mais ne sont pas constitués de molécules identifiables.
Aucune molécule typique ne peut être définie pour les sels ni pour les cristaux covalents , bien que ceux-ci soient souvent composés de cellules unitaires répétitives qui s’étendent soit dans un plan , par exemple le graphène ; ou en trois dimensions, par exemple diamant , quartz , chlorure de sodium . Le thème de la structure cellulaire unitaire répétée vaut également pour la plupart des métaux qui sont des phases condensées avec une liaison métallique . Ainsi, les métaux solides ne sont pas constitués de molécules.
Dans les verres , qui sont des solides qui existent dans un état vitreux désordonné, les atomes sont maintenus ensemble par des liaisons chimiques sans la présence d’aucune molécule définissable, ni aucune de la régularité de la structure cellulaire unitaire répétitive qui caractérise les sels, les cristaux covalents et les métaux.
Sciences moléculaires
La science des molécules est appelée chimie moléculaire ou physique moléculaire , selon que l’accent est mis sur la chimie ou la physique. La chimie moléculaire traite des lois régissant l’interaction entre les molécules qui aboutit à la formation et à la rupture de liaisons chimiques , tandis que la physique moléculaire traite des lois régissant leur structure et leurs propriétés. En pratique, cependant, cette distinction est vague. En sciences moléculaires, une molécule est constituée d’un système stable ( état lié ) composé de deux atomes ou plus . Les ions polyatomiques peuvent parfois être utilement considérés comme des molécules chargées électriquement. Le terme molécule instable est utilisé pour trèsdes espèces réactives , c’est-à-dire des assemblages de courte durée ( résonances ) d’électrons et de noyaux , tels que des radicaux , des ions moléculaires , des molécules de Rydberg , des états de transition , des complexes de van der Waals ou des systèmes d’atomes en collision comme dans le condensat de Bose-Einstein .
Histoire et étymologie
Selon Merriam-Webster et le dictionnaire d’étymologie en ligne , le mot “molécule” dérive du latin ” taupes ” ou petite unité de masse.
- Molecule (1794) – “particule extrêmement minute”, du français molécule (1678), du nouveau latin molecula , diminutif du latin taupes “masse, barrière”. Un sens vague au début; la vogue du mot (utilisé jusqu’à la fin du XVIIIe siècle uniquement sous forme latine) remonte à la philosophie de Descartes . [11] [12]
La définition de la molécule a évolué au fur et à mesure que la connaissance de la structure des molécules s’est accrue. Les définitions antérieures étaient moins précises, définissant les molécules comme les plus petites particules de substances chimiques pures qui conservent encore leur composition et leurs propriétés chimiques. [13] Cette définition tombe souvent en panne puisque de nombreuses substances dans l’expérience ordinaire, telles que les roches , les sels et les métaux , sont composées de grands réseaux cristallins d’ atomes ou d’ ions chimiquement liés , mais ne sont pas constituées de molécules discrètes.
Collage
Les molécules sont généralement maintenues ensemble par une Liaison covalente . Plusieurs éléments non métalliques n’existent que sous forme de molécules dans l’environnement, soit dans des composés, soit sous forme de molécules homonucléaires, et non sous forme d’atomes libres : par exemple, l’hydrogène.
Alors que certaines personnes disent qu’un cristal métallique peut être considéré comme une seule molécule géante maintenue ensemble par une liaison métallique , [14] d’autres soulignent que les métaux se comportent très différemment des molécules. [15]
covalent

 Une Liaison covalente formant H 2 (à droite) où deux atomes d’hydrogène partagent les deux électrons
Une Liaison covalente formant H 2 (à droite) où deux atomes d’hydrogène partagent les deux électrons
Une Liaison covalente est une liaison chimique qui implique le partage de paires d’électrons entre les atomes . Ces paires d’électrons sont appelées paires partagées ou paires de liaison , et l’équilibre stable des forces attractives et répulsives entre les atomes, lorsqu’ils partagent des électrons, est appelé Liaison covalente . [16]
Ionique

 Sodium et fluor subissant une réaction redox pour former du fluorure de sodium . Le sodium perd son électron externe pour lui donner une configuration électronique stable , et cet électron pénètre dans l’atome de fluor de manière Exothermique .
Sodium et fluor subissant une réaction redox pour former du fluorure de sodium . Le sodium perd son électron externe pour lui donner une configuration électronique stable , et cet électron pénètre dans l’atome de fluor de manière Exothermique .
La Liaison ionique est un type de liaison chimique qui implique l’ attraction Électrostatique entre des ions chargés de manière opposée , et est la principale interaction se produisant dans les composés ioniques . Les ions sont des atomes qui ont perdu un ou plusieurs électrons (appelés cations ) et des atomes qui ont gagné un ou plusieurs électrons (appelés anions ). [17] Ce transfert d’électrons est appelé électrovalence par opposition à covalence . Dans le cas le plus simple, le Cation est un atome de métal et l’Anion est un non- métalatome, mais ces ions peuvent être de nature plus compliquée, par exemple des ions moléculaires comme NH 4 + ou SO 4 2− . À des températures et des pressions normales, la Liaison ionique crée principalement des solides (ou parfois des liquides) sans molécules identifiables séparées, mais la vaporisation/sublimation de ces matériaux produit des molécules séparées où les électrons sont encore suffisamment transférés pour que les liaisons soient considérées comme ioniques plutôt que covalentes. .
Taille moléculaire
La plupart des molécules sont beaucoup trop petites pour être vues à l’œil nu, bien que les molécules de nombreux polymères puissent atteindre des tailles macroscopiques , y compris des biopolymères tels que l’ADN . Les molécules couramment utilisées comme blocs de construction pour la synthèse organique ont une dimension de quelques angströms (Å) à plusieurs dizaines d’Å, soit environ un milliardième de mètre. Les molécules simples ne peuvent généralement pas être observées à la lumière (comme indiqué ci-dessus), mais de petites molécules et même les contours d’atomes individuels peuvent être tracés dans certaines circonstances à l’aide d’un Microscope à force atomique . Certaines des plus grosses molécules sont des macromolécules ou des supermolécules .
La plus petite molécule est l’ hydrogène diatomique (H 2 ), avec une longueur de liaison de 0,74 Å. [18]
Le rayon moléculaire effectif est la taille qu’une molécule affiche en solution. [19] [20] Le tableau de permsélectivité pour différentes substances contient des exemples.
Formules moléculaires
Types de formules chimiques
La formule chimique d’une molécule utilise une ligne de symboles d’ éléments chimiques , des nombres et parfois aussi d’autres symboles, tels que des parenthèses, des tirets, des crochets et des signes plus (+) et moins (-). Ceux-ci sont limités à une ligne typographique de symboles, qui peuvent inclure des indices et des exposants.
La formule empirique d’un composé est un type très simple de formule chimique. [21] C’est le rapport entier le plus simple des éléments chimiques qui le constituent. [22] Par exemple, l’eau est toujours composée d’un rapport 2:1 d’atomes d’ hydrogène et d’ oxygène , et l’ éthanol (alcool éthylique) est toujours composé de carbone , d’hydrogène et d’oxygène dans un rapport 2:6:1. Cependant, cela ne détermine pas uniquement le type de molécule – l’éther diméthylique a les mêmes ratios que l’éthanol, par exemple. Molécules avec les mêmes atomesdans différents arrangements sont appelés isomères . De plus, les glucides, par exemple, ont le même rapport (carbone : hydrogène : oxygène = 1 : 2 : 1) (et donc la même formule empirique) mais des nombres totaux d’atomes différents dans la molécule.
La formule moléculaire reflète le nombre exact d’atomes qui composent la molécule et caractérise ainsi différentes molécules. Cependant différents isomères peuvent avoir la même composition atomique tout en étant des molécules différentes.
La formule empirique est souvent la même que la formule moléculaire mais pas toujours. Par exemple, la molécule d’ acétylène a la formule moléculaire C 2 H 2 , mais le rapport entier le plus simple des éléments est CH.
La masse moléculaire peut être calculée à partir de la formule chimique et est exprimée en unités de masse atomique conventionnelles égales à 1/12 de la masse d’un atome neutre de carbone 12 ( isotope 12 C ). Pour les solides de réseau , le terme unité de formule est utilisé dans les calculs stoechiométriques .
Formule structurelle
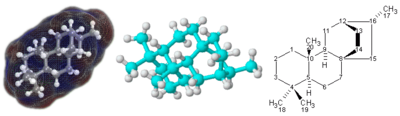
 Représentations 3D (gauche et centre) et 2D (droite) de la molécule terpénoïde atisane
Représentations 3D (gauche et centre) et 2D (droite) de la molécule terpénoïde atisane
Pour les molécules ayant une structure tridimensionnelle compliquée, impliquant en particulier des atomes liés à quatre substituants différents, une formule moléculaire simple ou même une formule chimique semi-structurelle peut ne pas suffire à spécifier complètement la molécule. Dans ce cas, un type de formule graphique appelé formule structurelle peut être nécessaire. Les formules structurelles peuvent à leur tour être représentées par un nom chimique unidimensionnel, mais une telle nomenclature chimique nécessite de nombreux mots et termes qui ne font pas partie des formules chimiques.
Géométrie moléculaire
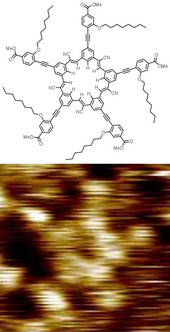
 Structure et image STM d’une molécule de dendrimère “cyanostar” . [23]
Structure et image STM d’une molécule de dendrimère “cyanostar” . [23]
Les molécules ont des géométries d’ équilibre fixes – longueurs et angles de liaison – autour desquelles elles oscillent en permanence par des mouvements de vibration et de rotation. Une substance pure est composée de molécules ayant la même structure géométrique moyenne. La formule chimique et la structure d’une molécule sont les deux facteurs importants qui déterminent ses propriétés, notamment sa réactivité . Les isomères partagent une formule chimique mais ont normalement des propriétés très différentes en raison de leurs structures différentes. Les stéréoisomères , un type particulier d’isomère, peuvent avoir des propriétés physico-chimiques très similaires et en même temps des activités biochimiques différentes .
Spectroscopie moléculaire
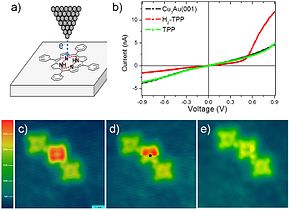
 L’hydrogène peut être éliminé des molécules individuelles de H 2 TPP en appliquant une tension excessive à la pointe d’un microscope à effet tunnel (STM, a) ; cette suppression modifie les courbes courant-tension (IV) des molécules de TPP, mesurées à l’aide de la même pointe STM, de type diode (courbe rouge en b) à résistance (courbe verte). L’image (c) montre une rangée de molécules TPP, H 2 TPP et TPP. Lors de la numérisation de l’image (d), une tension excessive a été appliquée à H 2TPP au niveau du point noir, qui élimine instantanément l’hydrogène, comme indiqué dans la partie inférieure de (d) et dans l’image de renumérisation (e). De telles manipulations peuvent être utilisées dans l’électronique à une seule molécule . [24]
L’hydrogène peut être éliminé des molécules individuelles de H 2 TPP en appliquant une tension excessive à la pointe d’un microscope à effet tunnel (STM, a) ; cette suppression modifie les courbes courant-tension (IV) des molécules de TPP, mesurées à l’aide de la même pointe STM, de type diode (courbe rouge en b) à résistance (courbe verte). L’image (c) montre une rangée de molécules TPP, H 2 TPP et TPP. Lors de la numérisation de l’image (d), une tension excessive a été appliquée à H 2TPP au niveau du point noir, qui élimine instantanément l’hydrogène, comme indiqué dans la partie inférieure de (d) et dans l’image de renumérisation (e). De telles manipulations peuvent être utilisées dans l’électronique à une seule molécule . [24]
La spectroscopie moléculaire traite de la réponse ( spectre ) de molécules interagissant avec des signaux de sondage d’ énergie connue (ou fréquence , selon la formule de Planck ). Les molécules ont des niveaux d’énergie quantifiés qui peuvent être analysés en détectant l’échange d’énergie de la molécule par absorbance ou émission . [25] La spectroscopie ne fait généralement pas référence aux études de diffraction où des particules telles que les neutrons , les électrons ou les rayons X à haute énergie interagissent avec un arrangement régulier de molécules (comme dans un cristal).
La spectroscopie micro-ondes mesure généralement les changements dans la rotation des molécules et peut être utilisée pour identifier des molécules dans l’espace. La spectroscopie infrarouge mesure la vibration des molécules, y compris les mouvements d’étirement, de flexion ou de torsion. Il est couramment utilisé pour identifier les types de liaisons ou de groupes fonctionnels dans les molécules. Les changements dans l’arrangement des électrons produisent des raies d’absorption ou d’émission dans l’ultraviolet, le visible ou le proche infrarouge , et se traduisent par la couleur. La spectroscopie par résonance nucléaire mesure l’environnement de noyaux particuliers dans la molécule et peut être utilisée pour caractériser le nombre d’atomes dans différentes positions dans une molécule.
Aspects théoriques
L’étude des molécules par la physique moléculaire et la chimie théorique est largement basée sur la mécanique quantique et est essentielle pour la compréhension de la liaison chimique . La plus simple des molécules est l’ ion-molécule d’hydrogène , H 2 + , et la plus simple de toutes les liaisons chimiques est la liaison à un électron . H 2 + est composé de deux protons chargés positivement et d’un électron chargé négativement , ce qui signifie que l’ équation de Schrödingercar le système peut être résolu plus facilement en raison du manque de répulsion électron-électron. Avec le développement des ordinateurs numériques rapides, des solutions approximatives pour des molécules plus complexes sont devenues possibles et constituent l’un des principaux aspects de la chimie computationnelle .
En essayant de définir rigoureusement si un arrangement d’atomes est suffisamment stable pour être considéré comme une molécule, l’IUPAC suggère qu’il “doit correspondre à une dépression sur la surface d’énergie potentielle suffisamment profonde pour confiner au moins un état vibrationnel”. [4] Cette définition ne dépend pas de la nature de l’interaction entre les atomes, mais uniquement de la force de l’interaction. En fait, il comprend des espèces faiblement liées qui ne seraient pas traditionnellement considérées comme des molécules, telles que le dimère d’ hélium , He 2 , qui a un état lié vibrationnel [26]et est si faiblement lié qu’il n’est susceptible d’être observé qu’à de très basses températures.
Qu’un arrangement d’atomes soit suffisamment stable ou non pour être considéré comme une molécule est par nature une définition opérationnelle. Philosophiquement, donc, une molécule n’est pas une entité fondamentale (contrairement, par exemple, à une particule élémentaire ) ; le concept de molécule est plutôt la façon dont le chimiste fait une déclaration utile sur les forces des interactions à l’échelle atomique dans le monde que nous observons.
Voir également
- Atome
- Polarité chimique
- Structure chimique
- Une Liaison covalente
- Molécule diatomique
- Liste des composés
- Liste des molécules interstellaires et circumstellaires
- Biologie moléculaire
- Logiciel de conception moléculaire
- Ingénierie moléculaire
- Géométrie moléculaire
- Hamiltonien moléculaire
- Ion moléculaire
- Modélisation moléculaire
- La promiscuité moléculaire
- Orbitale moléculaire
- Liaison non covalente
- Systèmes périodiques de petites molécules
- Petite molécule
- Comparaison de logiciels de modélisation de la mécanique moléculaire
- Molécule de Van der Waals
- Matrice moléculaire mondiale
Portails : ![]()
![]() Chimie
Chimie ![]()
![]() La biologie
La biologie ![]()
![]() La physique
La physique
Références
- ^ Iwata, Kota; Yamazaki, Shiro; Mutombo, Pingo ; Hapala, Prokop; Ondráček, Martin; Jelinek, Pavel; Sugimoto, Yoshiaki (2015). “Imagerie de la structure chimique d’une seule molécule par microscopie à force atomique à température ambiante” . Communication Nature . 6 : 7766. Bibcode : 2015NatCo…6.7766I . doi : 10.1038/ncomms8766 . PMC 4518281 . PMID 26178193 .
- ^ Dinca, LE; De Marchi, F.; MacLeod, JM; Lipton-Duffin, J.; Gatti, R.; Furieux.; Perepitchka, DF ; Rosei, F. (2015). “Pentacène sur Ni (111): Emballage moléculaire à température ambiante et conversion activée par la température en graphène”. À l’échelle nanométrique . 7 (7): 3263–9. Bib code : 2015Nanos …7.3263D . doi : 10.1039/C4NR07057G . PMID 25619890 .
- ^ Hapala, Prokop; Švec, Martin; Stetsovitch, Oleksandre; Van Der Heijden, Nadine J.; Ondráček, Martin; Van Der Lit, Joost ; Mutombo, Pingo ; Swart, Ingmar; Jelinek, Pavel (2016). “Cartographier le champ de force Électrostatique de molécules uniques à partir d’images de sondes à balayage haute résolution” . Communication Nature . 7 : 11560. Bibcode : 2016NatCo…711560H . doi : 10.1038/ncomms11560 . PMC 4894979 . PMID 27230940 .
- ^ un b IUPAC , Compendium de Terminologie Chimique , 2ème rédacteur. (le “Livre d’or”) (1997). Version corrigée en ligne : (2006–) ” Molécule “. doi : 10.1351/goldbook.M04002
- ^ Ebbin, Darrell D. (1990). Chimie générale (3e éd.). Boston: Houghton Mifflin Co.ISBN 978-0-395-43302-7.
- ^ Marron, TL ; Kenneth C. Kemp; Théodore L. Brown; Harold Eugène LeMay; Bruce Edward Bursten (2003). Chimie – la science centrale (9e éd.). New Jersey : Prentice Hall . ISBN 978-0-13-066997-1.
- ^ Chang, Raymond (1998). Chimie (6e éd.). New York : McGraw Hill . ISBN 978-0-07-115221-1.
- ^ Zumdahl, Steven S. (1997). Chimie (4e éd.). Boston : Houghton Mifflin. ISBN 978-0-669-41794-4.
- ^ Chandra, Sulekh (2005). Chimie inorganique complète . Éditeurs du nouvel âge. ISBN 978-81-224-1512-4.
- ^ “Molécule” . Encyclopædia Britannica . 22 janvier 2016 . Récupéré le 23 février 2016 .
- ^ Harper, Douglas. “molécule” . Dictionnaire d’étymologie en ligne . Récupéré le 22 février 2016 .
- ^ “molécule” . Merriam-Webster . Récupéré le 22 février 2016 .
- ^ Définition de la molécule archivée le 13 octobre 2014 à la Wayback Machine ( Frostburg State University )
- ^ Harry, B. Gray. Liaisons chimiques : Une introduction à la structure atomique et moléculaire (PDF) . p. 210–211 . Récupéré le 22 novembre 2021 .
- ^ “Combien d’atomes d’or font de l’or métal?” . phys.org . Récupéré le 22 novembre 2021 .
- ^ Campbell, Neil A.; Brad Williamson; Robin J. Heyden (2006). Biologie : Explorer la vie . Boston : Pearson Prentice Hall . ISBN 978-0-13-250882-7. Récupéré le 5 février 2012 .
- ^ Campbell, Flake C. (2008). Éléments de métallurgie et alliages d’ingénierie . ASM International . ISBN 978-1-61503-058-3.
- ^ Roger L. DeKock; Harry B. Gray; Harry B. Gray (1989). Structure chimique et liaison . Livres scientifiques universitaires. p. 199. ISBN 978-0-935702-61-3.
- ^ Chang RL; Deen WM; Robertson CR; Brenner BM (1975). “Permsélectivité de la paroi capillaire glomérulaire : III. Transport restreint de polyanions” . Rein Int . 8 (4): 212–218. doi : 10.1038/ki.1975.104 . PMID 1202253 .
- ^ Chang RL; Ueki SI ; Troy JL; Deen WM; Robertson CR; Brenner BM (1975). “Permsélectivité de la paroi capillaire glomérulaire aux macromolécules. II. Études expérimentales chez le rat utilisant du dextrane neutre” . Biophys. J. _ 15 (9): 887–906. Bibcode : 1975BpJ….15..887C . doi : 10.1016/S0006-3495(75)85863-2 . PMC 1334749 . PMID 1182263 .
- ^ Clin d’œil, Donald J.; Fetzer-Gislason, Sharon; McNicholas, Sheila (2003). La pratique de la chimie . Macmillan. ISBN 978-0-7167-4871-7.
- ^ “ChemTeam : Formule empirique” . www.chemteam.info . Récupéré le 16 avril 2017 .
- ^ Hirsch, Brandon E.; Lee, Sémin ; Qiao, Bo; Chen, Chun-Hsing; McDonald, Kevin P.; Tait, Steven L.; Inondation, Amar H. (2014). “Dimérisation induite par les anions de cyanostars symétriques 5 fois dans des solides cristallins 3D et des cristaux auto-assemblés 2D” . Communications chimiques . 50 (69): 9827–30. doi : 10.1039/C4CC03725A . PMID 25080328 .
- ^ Zoldan, VC; Facio, R; Pasa, AA (2015). “Caractère de type N et p des diodes à molécule unique” . Rapports scientifiques . 5 : 8350. Bibcode : 2015NatSR…5E8350Z . doi : 10.1038/srep08350 . PMC 4322354 . PMID 25666850 .
- ^ IUPAC , Compendium de terminologie chimique , 2e éd. (le “Livre d’or”) (1997). Version corrigée en ligne : (2006–) ” Spectroscopie “. doi : 10.1351/goldbook.S05848
- ^ Anderson JB (mai 2004). “Commentaire sur” Un calcul Monte Carlo quantique exact du potentiel intermoléculaire hélium-hélium “[J. Chem. Phys. 115, 4546 (2001)]” . J Chem Phys . 120 (20): 9886–7. Bibcode : 2004JChPh.120.9886A . doi : 10.1063/1.1704638 . PMID 15268005 .
Liens externes
Moléculedans les projets frères de Wikipédia
-
![]()
![]() Définitions du Wiktionnaire
Définitions du Wiktionnaire -
![]()
![]() Médias de Commons
Médias de Commons -
![]()
![]() Citations de Wikiquote
Citations de Wikiquote -
![]()
![]() Textes de Wikisource
Textes de Wikisource -
![]()
![]() Données de Wikidata
Données de Wikidata
- Molécule du mois – École de chimie, Université de Bristol
