COVID-19 [feminine]
La maladie à coronavirus 2019 ( COVID-19 ) est une maladie contagieuse causée par un virus, le coronavirus 2 du syndrome respiratoire aigu sévère (SARS-CoV-2). Le premier cas connu a été identifié à Wuhan , en Chine, en décembre 2019. [7] La maladie s’est propagée dans le monde entier, entraînant la pandémie de COVID-19 . [8]
| Maladie à coronavirus 2019 (COVID-19) |
|
|---|---|
| Autres noms | COVID, (le) coronavirus |
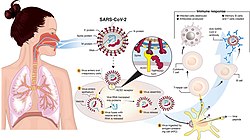 |
|
| Transmission et cycle de vie du SARS-CoV-2 causant le COVID-19. | |
| Prononciation |
|
| Spécialité | Maladie infectieuse |
| Les symptômes | Fièvre, toux, fatigue, essoufflement, vomissements, perte de goût ou d’odorat ; certains cas asymptomatiques [2] [3] |
| Complications | Pneumonie , septicémie virale , syndrome de détresse respiratoire aiguë , insuffisance rénale , syndrome de relargage de cytokines , insuffisance respiratoire , fibrose pulmonaire , syndrome inflammatoire multisystémique pédiatrique , long COVID |
| Début habituel | 2 à 14 jours (généralement 5) après l’infection |
| Durée | 5 jours à chronique |
| causes | Coronavirus 2 du syndrome respiratoire aigu sévère (SARS-CoV-2) |
| Méthode diagnostique | Test rRT-PCR , CT scan , Test antigénique rapide |
| La prévention | Couvre-visage, quarantaine , distanciation physique/ sociale , ventilation, lavage des mains, [4] vaccination [5] |
| Traitement | Symptomatique et de soutien |
| La fréquence | 521 544 771 [6] cas confirmés |
| Décès | 6 264 097 [6] |
Les symptômes de la COVID‐19 sont variables, mais comprennent souvent de la fièvre, [9] de la toux, des maux de tête, [10] de la fatigue, des difficultés respiratoires , une perte d’odorat et une perte de goût . [11] [12] [13] Les symptômes peuvent commencer un à quatorze jours après l’exposition au virus. Au moins un tiers des personnes infectées ne développent pas de symptômes perceptibles . [14] Parmi les personnes qui développent des symptômes suffisamment perceptibles pour être considérées comme des patients, la plupart (81 %) développent des symptômes légers à modérés (jusqu’à une pneumonie légère ), tandis que 14 % développent des symptômes graves ( dyspnée ,hypoxie ou plus de 50 % d’atteinte pulmonaire à l’imagerie) et 5 % souffrent de symptômes critiques ( insuffisance respiratoire , choc ou dysfonctionnement multiviscéral ). [15] Les personnes âgées courent un risque plus élevé de développer des symptômes graves. Certaines personnes continuent de ressentir une gamme d’effets ( long COVID ) pendant des mois après leur rétablissement, et des dommages aux organes ont été observés. [16] Des études pluriannuelles sont en cours pour étudier plus avant les effets à long terme de la maladie. [16]
La COVID‐19 se transmet lorsque les gens respirent de l’air contaminé par des gouttelettes et de petites particules en suspension dans l’air contenant le virus. Le risque de les respirer est plus élevé lorsque les personnes se trouvent à proximité, mais elles peuvent être inhalées sur de plus longues distances, en particulier à l’intérieur. La transmission peut également se produire en cas d’éclaboussures ou de pulvérisation de fluides contaminés dans les yeux, le nez ou la bouche et, rarement, via des surfaces contaminées. Les gens restent contagieux jusqu’à 20 jours et peuvent propager le virus même s’ils ne développent pas de symptômes. [17] [18]
Plusieurs méthodes de test COVID-19 ont été développées pour diagnostiquer la maladie. La méthode de diagnostic standard consiste à détecter l’ acide nucléique du virus par réaction en chaîne par polymérase de transcription inverse en temps réel (rRT-PCR), amplification médiée par transcription (TMA) ou par amplification isotherme médiée par boucle de transcription inverse (RT-LAMP) à partir de un écouvillon nasopharyngé .
Plusieurs vaccins COVID-19 ont été approuvés et distribués dans divers pays, qui ont lancé des campagnes de vaccination de masse . D’autres mesures préventives comprennent la distanciation physique ou sociale , la mise en quarantaine , la ventilation des espaces intérieurs, la couverture de la toux et des éternuements, le lavage des mains et le maintien des mains non lavées loin du visage. L’ utilisation de masques faciaux ou de revêtements a été recommandée dans les lieux publics pour minimiser le risque de transmission. Alors que des travaux sont en cours pour développer des médicaments qui inhibent le virus, le traitement primaire est symptomatique. La prise en charge implique le traitement des symptômes, soins de soutien , isolement et mesures expérimentales .
Nomenclature
Lors de l’épidémie initiale à Wuhan , le virus et la maladie étaient communément appelés “coronavirus” et “coronavirus de Wuhan”, [19] [20] [21] avec la maladie parfois appelée “pneumonie de Wuhan”. [22] [23] Dans le passé, de nombreuses maladies ont été nommées d’après des lieux géographiques, tels que la grippe espagnole , [24] le syndrome respiratoire du Moyen-Orient et le virus Zika . [25] En janvier 2020, l’ Organisation mondiale de la santé (OMS) a recommandé les maladies respiratoires aiguës 2019-nCoV [26] et 2019-nCoV [27]en tant que noms provisoires pour le virus et la maladie conformément aux directives de 2015 et aux directives internationales contre l’utilisation de lieux géographiques ou de groupes de personnes dans les noms de maladies et de virus pour prévenir la stigmatisation sociale . [28] [29] [30] Les noms officiels COVID‐19 et SARS-CoV-2 ont été émis par l’OMS le 11 février 2020. [31] Le directeur général , Tedros Adhanom , a expliqué que CO signifie corona , VI pour virus , D pour maladie et 19 pour 2019, année au cours de laquelle l’épidémie a été identifiée pour la première fois. [32]L’OMS utilise en outre “le virus COVID‐19” et “le virus responsable du COVID‐19” dans les communications publiques. [31] [33]
Signes et symptômes
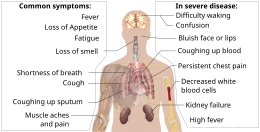
 Symptômes de la COVID-19
Symptômes de la COVID-19
Les symptômes du COVID-19 sont variables, allant de symptômes bénins à une maladie grave et éventuellement mortelle. [34] [35] Les symptômes courants comprennent la toux , la fièvre , la perte de l’odorat (anosmie) et du goût (agueusie), les moins courants comprenant les maux de tête , la congestion nasale et l’écoulement nasal , les douleurs musculaires , les maux de gorge , la diarrhée , l’irritation des yeux , [ 36] et orteils gonflés ou virant au violet, [37] et dans les cas modérés à graves difficultés respiratoires. [38] Les personnes infectées par le COVID-19 peuvent avoir des symptômes différents et leurs symptômes peuvent changer avec le temps. Trois groupes communs de symptômes ont été identifiés : un groupe de symptômes respiratoires avec toux, crachats , essoufflement et fièvre ; un groupe de symptômes musculo-squelettiques avec des douleurs musculaires et articulaires, des maux de tête et de la fatigue ; un groupe de symptômes digestifs avec des douleurs abdominales, des vomissements et de la diarrhée. [38] Chez les personnes sans troubles antérieurs de l’oreille, du nez et de la gorge, une perte de goût combinée à une perte d’odorat est associée à la COVID-19 et est signalée dans jusqu’à 88 % des cas symptomatiques. [39] [40] [41]
Parmi les personnes qui présentent des symptômes, 81 % ne développent que des symptômes légers à modérés (jusqu’à une pneumonie légère ), tandis que 14 % développent des symptômes sévères ( dyspnée , hypoxie ou plus de 50 % d’atteinte pulmonaire à l’imagerie) nécessitant une hospitalisation et 5 % des patients souffrez de symptômes critiques ( insuffisance respiratoire , choc septique ou dysfonctionnement multiviscéral ) nécessitant une admission aux soins intensifs. [42] Au moins un tiers des personnes infectées par le virus ne développent à aucun moment des symptômes perceptibles. [43] [44] Ces porteurs asymptomatiques ont tendance à ne pas se faire tester et peuvent quand même propager la maladie. [44][45] [46] [47] D’autres personnes infectées développeront des symptômes plus tard, appelés “pré-symptomatiques”, ou auront des symptômes très légers et pourront également propager le virus. [47]
Comme c’est souvent le cas avec les infections, il y a un délai entre le moment où une personne est infectée pour la première fois et l’apparition des premiers symptômes. Le délai médian pour COVID-19 est de quatre à cinq jours [48] pouvant être infectieux pendant 1 à 4 de ces jours. [49] La plupart des personnes symptomatiques ressentent des symptômes dans les deux à sept jours suivant l’exposition, et presque toutes ressentiront au moins un symptôme dans les 12 jours. [48] [50]
La plupart des gens se remettent de la phase aiguë de la maladie. Cependant, certaines personnes – plus de la moitié d’une cohorte de jeunes adultes isolés à domicile [51] [52] – continuent de ressentir une gamme d’effets, tels que la fatigue , pendant des mois même après leur rétablissement, une condition appelée COVID long ; des dommages à long terme aux organes ont été observés. Des études pluriannuelles sont en cours pour étudier plus avant les effets potentiels à long terme de la maladie. [53]
Cause
La COVID‐19 est causée par une infection par une souche de coronavirus connue sous le nom de coronavirus 2 du syndrome respiratoire aigu sévère (SRAS-CoV-2). [54]
Transmission

 Transmission de la COVID‐19
Transmission de la COVID‐19 
 La voie respiratoire de propagation du COVID-19, englobant des gouttelettes et des aérosols plus gros.
La voie respiratoire de propagation du COVID-19, englobant des gouttelettes et des aérosols plus gros.
Le COVID-19 se transmet principalement lorsque les personnes respirent de l’air contaminé par des gouttelettes / aérosols et de petites particules en suspension dans l’air contenant le virus. Les personnes infectées exhalent ces particules lorsqu’elles respirent, parlent, toussent, éternuent ou chantent. [55] [56] [57] [58] La transmission est d’autant plus probable que les personnes sont physiquement proches. Cependant, l’infection peut se produire sur de plus longues distances, en particulier à l’intérieur. [55] [59]
L’infectiosité peut commencer quatre à cinq jours avant l’apparition des symptômes, [60] bien que la recherche des contacts ne commence généralement que deux à trois jours avant l’apparition des symptômes. [61] Les personnes infectées peuvent propager la maladie même si elles sont pré-symptomatiques ou asymptomatiques . [61] Le plus souvent, la charge virale maximale dans les échantillons des voies respiratoires supérieures se produit près du moment de l’apparition des symptômes et diminue après la première semaine après le début des symptômes. [61]Les preuves actuelles suggèrent une durée d’excrétion virale et une période d’infectiosité allant jusqu’à dix jours après l’apparition des symptômes pour les personnes atteintes de COVID-19 léger à modéré, et jusqu’à 20 jours pour les personnes atteintes de COVID-19 sévère, y compris les personnes immunodéprimées. [62] [61]
Les particules infectieuses varient en taille depuis les aérosols qui restent en suspension dans l’air pendant de longues périodes jusqu’aux gouttelettes plus grosses qui restent brièvement en suspension dans l’air ou tombent au sol. [63] [64] [65] [66] De plus, la recherche sur le COVID-19 a redéfini la compréhension traditionnelle de la transmission des virus respiratoires. [66] [67] Les plus grosses gouttelettes de liquide respiratoire ne voyagent pas loin, mais peuvent être inhalées ou atterrir sur les muqueuses des yeux, du nez ou de la bouche pour les infecter. [65] La concentration des aérosols est la plus élevée lorsque les personnes sont à proximité, ce qui facilite la transmission virale lorsque les personnes sont physiquement proches, [65] [66][67] mais la transmission aérienne peut se produire à de plus longues distances, principalement dans des endroits mal ventilés ; [65] dans ces conditions, de petites particules peuvent rester en suspension dans l’air pendant des minutes ou des heures. [65]
Le nombre de personnes généralement infectées par une personne infectée varie, [68] mais on estime que le nombre R 0 (“R zéro” ou “R zéro”) est d’environ 2,5. [69] La maladie se propage souvent en grappes , où les infections peuvent être retracées à un cas index ou à un emplacement géographique. [70] Souvent, dans ces cas, des événements de grande propagation se produisent, où de nombreuses personnes sont infectées par une seule personne. [68]
Virologie

 Illustration du virion du SRASr-CoV
Illustration du virion du SRASr-CoV
Le coronavirus 2 du syndrome respiratoire aigu sévère (SRAS-CoV-2) est un nouveau coronavirus du syndrome respiratoire aigu sévère. Il a d’abord été isolé chez trois personnes atteintes de pneumonie liées au groupe de cas de maladies respiratoires aiguës à Wuhan. [71] Toutes les caractéristiques structurelles de la nouvelle particule virale SARS-CoV-2 se produisent dans des coronavirus apparentés dans la nature. [72]
Hors du corps humain, le virus est détruit par le savon de Marseille, qui fait éclater sa bulle protectrice . [73]
Le SARS-CoV-2 est étroitement lié au SARS-CoV d’ origine . [74] On pense qu’il a une origine animale ( zoonotique ). L’analyse génétique a révélé que le coronavirus se regroupe génétiquement avec le genre Betacoronavirus , dans le sous-genre Sarbecovirus (lignée B) avec deux souches dérivées de chauves-souris. Il est identique à 96 % au niveau du génome entier aux autres échantillons de coronavirus de chauve-souris (BatCov RaTG13 ). [75] [76] [77] Les protéines structurelles du SRAS-CoV-2 comprennent la glycoprotéine membranaire (M), la protéine d’enveloppe (E), la protéine de nucléocapside (N) et laprotéine de pointe (S). La protéine M du SARS-CoV-2 est similaire à environ 98 % à la protéine M du SARS-CoV de chauve-souris, maintient une homologie d’environ 98 % avec le pangolin SARS-CoV et a 90 % d’homologie avec la protéine M du SARS-CoV ; alors que la similitude n’est que d’environ 38 % avec la protéine M du MERS-CoV. [78]
Variantes du SRAS-CoV-2
Les milliers de variantes du SRAS-CoV-2 sont regroupées en clades ou en lignées . [79] [80] L’OMS, en collaboration avec des partenaires, des réseaux d’experts, des autorités nationales, des institutions et des chercheurs, a établi des systèmes de nomenclature pour nommer et suivre les lignées génétiques du SRAS-CoV-2 par GISAID , Nextstrain et Pango . À l’heure actuelle, le groupe d’experts convoqué par l’OMS a recommandé l’étiquetage des variantes utilisant des lettres de l’ alphabet grec , par exemple, Alpha , Beta , Delta et Gamma, en justifiant qu’ils “seront plus faciles et plus pratiques à discuter par des publics non scientifiques”. [81] Nextstrain divise les variantes en cinq clades (19A, 19B, 20A, 20B et 20C), tandis que GISAID les divise en sept (L, O, V, S, G, GH et GR). [82] L’outil Pango regroupe les variantes en lignées , de nombreuses lignées en circulation étant classées sous la lignée B.1. [80] [83]
Plusieurs variantes notables du SRAS-CoV-2 sont apparues tout au long de 2020. [84] [85] Le groupe 5 a émergé parmi les visons et les éleveurs de visons au Danemark . [86] Après des quarantaines strictes et une campagne d’euthanasie des visons, le groupe a été évalué comme ne circulant plus parmi les humains au Danemark à partir du 1er février 2021. [87]
En décembre 2021 [update], il existe cinq variantes dominantes du SRAS-CoV-2 qui se propagent parmi les populations mondiales : la variante Alpha (B.1.1.7, anciennement appelée variante britannique), trouvée pour la première fois à Londres et dans le Kent, la variante bêta (B. .1.351, anciennement appelée variante Afrique du Sud), la variante Gamma (P.1, anciennement appelée variante Brésil), la variante Delta (B.1.617.2, anciennement appelée variante Inde), [88] et la variante Omicron (B.1.1.529), qui s’était propagé à 57 pays au 7 décembre. [89] [90]
Physiopathologie

 Pathogenèse de la COVID‐19
Pathogenèse de la COVID‐19
Le virus SARS-CoV-2 peut infecter un large éventail de cellules et de systèmes du corps. La COVID‐19 est surtout connue pour affecter les voies respiratoires supérieures (sinus, nez et gorge) et les voies respiratoires inférieures (trachée et poumons). [91] Les poumons sont les organes les plus touchés par la COVID‐19 car le virus accède aux cellules hôtes via le récepteur de l’enzyme de conversion de l’angiotensine 2 (ACE2), qui est le plus abondant à la surface des cellules alvéolaires de type II des poumons . [92] Le virus utilise une glycoprotéine de surface spéciale appelée « spike » pour se connecter au récepteur ACE2 et pénétrer dans la cellule hôte. [93]
Voies respiratoires
Après l’entrée virale, la COVID‐19 infecte l’épithélium cilié du nasopharynx et des voies respiratoires supérieures. [94]
Système nerveux
Un symptôme courant, la perte d’odorat, résulte d’ une infection des cellules de soutien de l’épithélium olfactif , avec des dommages ultérieurs aux neurones olfactifs . [95] L’implication du système nerveux central et périphérique dans la COVID-19 a été rapportée dans de nombreuses publications médicales. [96] Il est clair que de nombreuses personnes atteintes de la COVID-19 présentent des problèmes neurologiques ou de santé mentale . Le virus n’est pas détecté dans le SNC de la majorité des patients COVID-19 souffrant de problèmes neurologiques . Cependant, le SRAS-CoV-2 a été détecté à de faibles niveaux dans le cerveau de personnes décédées du COVID‐19, mais ces résultats doivent être confirmés. [97]Alors que le virus a été détecté dans le liquide céphalo-rachidien des autopsies, le mécanisme exact par lequel il envahit le SNC reste incertain et peut d’abord impliquer l’invasion des nerfs périphériques étant donné les faibles niveaux d’ACE2 dans le cerveau. [98] [99] [100] Le virus peut également entrer dans la circulation sanguine à partir des poumons et traverser la barrière hémato-encéphalique pour accéder au SNC, éventuellement dans un globule blanc infecté. [97]

 Tropisme et lésions d’organes multiples dans l’infection par le SRAS-CoV-2
Tropisme et lésions d’organes multiples dans l’infection par le SRAS-CoV-2
Des recherches menées lorsque Alpha était la variante dominante ont suggéré que le COVID-19 pourrait causer des lésions cérébrales. On ignore actuellement si ces dommages sont temporaires ou permanents, et si Omicron a des effets similaires. [101] [102] Les individus observés infectés par le COVID-19 (la plupart avec des cas bénins) ont subi une perte supplémentaire de 0,2 % à 2 % de tissu cérébral dans les régions du cerveau liées à l’odorat par rapport aux individus non infectés, et l’ensemble l’effet sur le cerveau équivalait en moyenne à au moins une année supplémentaire de vieillissement normal ; les individus infectés ont également obtenu des scores inférieurs à plusieurs tests cognitifs. Tous les effets étaient plus prononcés chez les personnes âgées. [103]
Tube digestif
Le virus affecte également les organes gastro-intestinaux car l’ACE2 est abondamment exprimé dans les cellules glandulaires de l’ épithélium gastrique , duodénal et rectal [104] ainsi que dans les cellules endothéliales et les entérocytes de l’ intestin grêle . [105]
Système cardiovasculaire
Le virus peut causer des lésions myocardiques aiguës et des dommages chroniques au système cardiovasculaire . [106] Une lésion cardiaque aiguë a été découverte chez 12 % des personnes infectées admises à l’hôpital de Wuhan, en Chine, [107] et est plus fréquente dans les cas de maladie grave. [108] Les taux de symptômes cardiovasculaires sont élevés, en raison de la réponse inflammatoire systémique et des troubles du système immunitaire au cours de la progression de la maladie, mais les lésions myocardiques aiguës peuvent également être liées aux récepteurs ACE2 dans le cœur. [106] Les récepteurs ACE2 sont fortement exprimés dans le cœur et sont impliqués dans la fonction cardiaque. [106] [109] Une incidence élevée de thrombose etdes thromboembolies veineuses ont été découvertes chez des personnes transférées dans des unités de soins intensifs (USI) avec des infections à la COVID‐19, et peuvent être liées à un mauvais pronostic. [110] On pense que le dysfonctionnement des vaisseaux sanguins et la formation de caillots (comme le suggèrent les niveaux élevés de D-dimères causés par les caillots sanguins) jouent un rôle important dans la mortalité, les incidences de caillots conduisant à des embolies pulmonaires et des événements ischémiques dans le cerveau ont été notés . comme des complications entraînant la mort chez les personnes infectées par le SRAS-CoV-2. L’infection semble déclencher une chaîne de réponses vasoconstrictrices dans le corps, la constriction des vaisseaux sanguins dans la circulation pulmonairea également été présenté comme un mécanisme dans lequel l’oxygénation diminue parallèlement à la présentation d’une pneumonie virale. [111] En outre, des dommages aux vaisseaux sanguins microvasculaires ( artérioles et capillaires ) ont été signalés dans un petit nombre d’échantillons de tissus du cerveau – sans détection du SRAS-CoV-2 – et des bulbes olfactifs de personnes décédées du COVID‐19. [112] [113] [114] Il a également été constaté que la COVID-19 provoquait des changements substantiels – y compris morphologiques et mécaniques – des cellules sanguines – comme une augmentation de la taille – persistant parfois pendant des mois après la sortie de l’hôpital. [115] [116]
Autres organes
Les complications liées aux reins sont une autre cause fréquente de décès . [111] Les premiers rapports montrent que jusqu’à 30% des patients hospitalisés en Chine et à New York ont subi des lésions rénales, y compris certaines personnes sans problèmes rénaux antérieurs. [117]
Les autopsies de personnes décédées du COVID‐19 ont révélé des lésions alvéolaires diffuses et des infiltrats inflammatoires contenant des lymphocytes dans les poumons. [118]
Immunopathologie

 Composants clés de la réponse immunitaire adaptative au SARS-CoV-2
Composants clés de la réponse immunitaire adaptative au SARS-CoV-2
Bien que le SRAS-CoV-2 ait un tropisme pour les cellules épithéliales exprimant l’ACE2 des voies respiratoires, les personnes atteintes de COVID-19 sévère présentent des symptômes d’hyperinflammation systémique. Résultats de laboratoire clinique d’élévation de l’IL‐2 , de l’IL‐7 , de l’IL‐6 , du facteur de stimulation des colonies de granulocytes et de macrophages (GM‐CSF), de la protéine 10 induite par l’interféron gamma (IP‐10), de la protéine chimiotactique des monocytes 1 (MCP1), la protéine inflammatoire des macrophages 1‐alpha (MIP‐1‐alpha) et le facteur de nécrose tumorale (TNF‐α) indiquant le syndrome de libération des cytokines (SRC) suggèrent une immunopathologie sous-jacente. [107]
De plus, les personnes atteintes de COVID‐19 et du syndrome de détresse respiratoire aiguë (SDRA) présentent des biomarqueurs sériques classiques du SRC, notamment une élévation de la protéine C-réactive (CRP), de la lactate déshydrogénase (LDH), des D-dimères et de la ferritine . [119]
L’inflammation systémique entraîne une vasodilatation , permettant une infiltration lymphocytaire et monocytaire inflammatoire du poumon et du cœur. En particulier, il a été démontré que les cellules T pathogènes sécrétant du GM-CSF étaient en corrélation avec le recrutement de monocytes inflammatoires sécrétant de l’IL-6 et une pathologie pulmonaire sévère chez les personnes atteintes de COVID-19. [120] Des infiltrats lymphocytaires ont également été signalés à l’autopsie. [118]
Facteurs viraux et hôtes
Protéines virales 
 L’association entre le SRAS-CoV-2 et le système rénine-angiotensine-aldostérone (RAAS)
L’association entre le SRAS-CoV-2 et le système rénine-angiotensine-aldostérone (RAAS)
De multiples facteurs viraux et hôtes affectent la pathogenèse du virus. La protéine S, autrement connue sous le nom de protéine de pointe, est le composant viral qui se fixe au récepteur de l’hôte via les récepteurs ACE2 . Il comprend deux sous-unités : S1 et S2. S1 détermine la gamme virus-hôte et le tropisme cellulaire via le domaine de liaison au récepteur. S2 assure la médiation de la fusion membranaire du virus à son hôte cellulaire potentiel via les régions H1 et HR2, qui sont des régions répétées heptades . Des études ont montré que le domaine S1 induisait des niveaux d’anticorps IgG et IgA à une capacité beaucoup plus élevée. C’est l’expression des protéines de pointe focalisées qui est impliquée dans de nombreux vaccins efficaces contre la COVID‐19. [121]
La protéine M est la protéine virale responsable du transport transmembranaire des nutriments. Il est à l’origine du débourrement et de la formation de l’enveloppe virale. [122] Les protéines N et E sont des protéines accessoires qui interfèrent avec la réponse immunitaire de l’hôte. [122]
Facteurs d’accueil
L’ enzyme de conversion de l’angiotensine humaine 2 (hACE2) est le facteur hôte ciblé par le virus SARS-COV2, provoquant la COVID‐19. Théoriquement, l’utilisation de bloqueurs des récepteurs de l’angiotensine (ARA) et d’ inhibiteurs de l’ECA régulant à la hausse l’expression de l’ACE2 pourrait augmenter la morbidité avec le COVID‐19, bien que les données animales suggèrent un effet protecteur potentiel de l’ARA ; cependant, aucune étude clinique n’a prouvé la sensibilité ou les résultats. Jusqu’à ce que de nouvelles données soient disponibles, les lignes directrices et les recommandations pour les patients hypertendus demeurent. [123]
L’effet du virus sur les surfaces des cellules ACE2 entraîne une infiltration leucocytaire, une perméabilité accrue des vaisseaux sanguins, une perméabilité de la paroi alvéolaire, ainsi qu’une diminution de la sécrétion de surfactants pulmonaires. Ces effets provoquent la majorité des symptômes respiratoires. Cependant, l’aggravation de l’inflammation locale provoque une tempête de cytokines conduisant finalement à un syndrome de réponse inflammatoire systémique . [124]
Parmi les adultes en bonne santé non exposés au SRAS-CoV-2, environ 35 % ont des lymphocytes T CD4 + qui reconnaissent la protéine S du SRAS-CoV-2 (en particulier la sous-unité S2) et environ 50 % réagissent aux autres protéines du virus, suggérant un croisement -réactivité des précédents rhumes courants causés par d’autres coronavirus. [125]
On ne sait pas si différentes personnes utilisent des gènes d’anticorps similaires en réponse à la COVID‐19. [126]
Réponse des cytokines de l’hôte
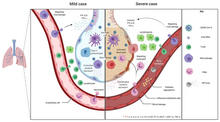
 Réponse immunitaire légère ou sévère lors d’ une infection virale
Réponse immunitaire légère ou sévère lors d’ une infection virale
La sévérité de l’inflammation peut être attribuée à la sévérité de ce qu’on appelle la tempête de cytokines . [127] Les niveaux d’ interleukine 1B , d’interféron-gamma , de protéine inductible par l’interféron 10 et de protéine chimiotactique des monocytes 1 étaient tous associés à la gravité de la maladie COVID‐19. Un traitement a été proposé pour lutter contre la tempête de cytokines car elle reste l’une des principales causes de morbidité et de mortalité dans la maladie COVID‐19. [128]
Une tempête de cytokines est due à une réponse hyperinflammatoire aiguë qui est responsable de maladies cliniques dans un éventail de maladies, mais dans le cas de la COVID‐19, elle est liée à un pronostic plus sombre et à une mortalité accrue. La tempête provoque un syndrome de détresse respiratoire aiguë, des événements de coagulation sanguine tels que des accidents vasculaires cérébraux, un infarctus du myocarde, une encéphalite , une lésion rénale aiguë et une vascularite . La production d’ IL-1 , d’IL-2 , d’IL-6 , de TNF-alpha et d’interféron-gamma , tous des composants cruciaux des réponses immunitaires normales, devient par inadvertance la cause d’une tempête de cytokines. Les cellules du système nerveux central , la microglie, les neurones et les astrocytes sont également impliqués dans la libération de cytokines pro-inflammatoires affectant le système nerveux, et les effets des tempêtes de cytokines sur le SNC ne sont pas rares. [129]
Réponse de grossesse
Il existe de nombreuses inconnues pour les femmes enceintes pendant la pandémie de COVID‐19. Étant donné qu’ils sont susceptibles de souffrir de complications et d’infections graves par d’autres types de coronavirus, ils ont été identifiés comme un groupe vulnérable et invités à prendre des mesures préventives supplémentaires. [130]
Les réponses physiologiques à la grossesse peuvent inclure :
- Immunologique : La réponse immunologique au COVID-19, comme à d’autres virus, dépend d’un système immunitaire fonctionnel. Il s’adapte au cours de la grossesse pour permettre le développement du fœtus dont la charge génétique n’est que partiellement partagée avec sa mère, entraînant une réaction immunologique différente aux infections au cours de la grossesse. [130]
- Respiratoire : De nombreux facteurs peuvent rendre les femmes enceintes plus vulnérables aux infections respiratoires dures. L’un d’eux est la réduction totale de la capacité et de l’incapacité des poumons à éliminer les sécrétions. [130]
- Coagulation : pendant la grossesse, les taux de facteurs de coagulation circulants sont plus élevés et la pathogenèse de l’infection par le SRAS-CoV-2 peut être impliquée. Les événements thromboemboliques avec mortalité associée sont un risque pour les femmes enceintes. [130]
Cependant, à partir de la base de preuves, il est difficile de conclure si les femmes enceintes courent un risque accru de conséquences graves de ce virus. [130]
En plus de ce qui précède, d’autres études cliniques ont prouvé que le SRAS-CoV-2 peut affecter la période de grossesse de différentes manières. D’une part, il existe peu de preuves de son impact jusqu’à 12 semaines de gestation. D’autre part, l’infection au COVID-19 peut entraîner une augmentation des taux d’issues défavorables au cours de la grossesse. Quelques exemples de ceux-ci pourraient être la restriction de croissance fœtale, la naissance prématurée et la mortalité périnatale, qui fait référence à la mort fœtale après 22 ou 28 semaines complètes de grossesse ainsi qu’au décès d’enfants nés vivants jusqu’à sept jours complets de vie. [130]
Les femmes non vaccinées aux derniers stades de la grossesse atteintes de COVID-19 sont plus susceptibles que les autres patientes d’avoir besoin de soins très intensifs. Les bébés nés de mères atteintes de COVID-19 sont plus susceptibles d’avoir des problèmes respiratoires. Les femmes enceintes sont fortement encouragées à se faire vacciner . [131]
Diagnostic
La COVID‐19 peut être provisoirement diagnostiquée sur la base des symptômes et confirmée à l’aide de la réaction en chaîne par polymérase de transcription inverse (RT-PCR) ou d’autres tests d’ acide nucléique des sécrétions infectées. [132] [133] Parallèlement aux tests de laboratoire, les tomodensitogrammes thoraciques peuvent être utiles pour diagnostiquer la COVID-19 chez les personnes présentant une forte suspicion clinique d’infection. [134] La détection d’une infection passée est possible grâce à des tests sérologiques , qui détectent les anticorps produits par l’organisme en réponse à l’infection. [132]
Test viral

 Démonstration d’un prélèvement nasopharyngé pour le test COVID‐19
Démonstration d’un prélèvement nasopharyngé pour le test COVID‐19
Les méthodes standard de test de présence du SRAS-CoV-2 sont les tests d’acide nucléique , [132] [135] qui détectent la présence de fragments d’ARN viral. [136] Comme ces tests détectent l’ARN mais pas le virus infectieux, sa “capacité à déterminer la durée de l’infectiosité des patients est limitée”. [137] Le test est généralement effectué sur des échantillons respiratoires obtenus par un prélèvement nasopharyngé ; cependant, un écouvillon nasal ou un échantillon d’expectoration peut également être utilisé. [138] [139] Les résultats sont généralement disponibles en quelques heures. [132] L’OMS a publié plusieurs protocoles de test pour la maladie. [140]
Plusieurs laboratoires et entreprises ont développé des tests sérologiques, qui détectent les anticorps produits par l’organisme en réponse à une infection. Plusieurs ont été évalués par Public Health England et approuvés pour une utilisation au Royaume-Uni. [141]
Le CEBM de l’Université d’Oxford a mis en évidence des preuves de plus en plus nombreuses [142] [143] selon lesquelles “une bonne proportion de” nouveaux “cas bénins et de personnes retestant des résultats positifs après la mise en quarantaine ou la sortie de l’hôpital ne sont pas infectieux, mais disparaissent simplement inoffensifs particules virales que leur système immunitaire a traitées efficacement” et ont appelé à “un effort international pour normaliser et calibrer périodiquement les tests” [144] Le 7 septembre, le gouvernement britannique a publié “des directives sur les procédures à mettre en œuvre dans les laboratoires pour fournir l’assurance résultats positifs pour l’ARN du SRAS-CoV-2 pendant les périodes de faible prévalence, lorsqu’il y a une réduction de la valeur prédictive des résultats de test positifs ». [145]
Imagerie

 Une tomodensitométrie d’une personne atteinte de COVID-19 montre des lésions (régions lumineuses) dans les poumons
Une tomodensitométrie d’une personne atteinte de COVID-19 montre des lésions (régions lumineuses) dans les poumons 
 CT scan du stade de progression rapide du COVID-19
CT scan du stade de progression rapide du COVID-19 
 Radiographie pulmonaire montrant une pneumonie à la COVID‐19
Radiographie pulmonaire montrant une pneumonie à la COVID‐19
Les tomodensitogrammes thoraciques peuvent être utiles pour diagnostiquer la COVID‐19 chez les personnes présentant une forte suspicion clinique d’infection, mais ne sont pas recommandés pour le dépistage de routine. [134] [146] Les opacités bilatérales multilobaires en verre dépoli avec une distribution périphérique, asymétrique et postérieure sont courantes dans les infections précoces. [134] [147] La dominance sous-pleurale, le pavage fou (épaississement septal lobulaire avec remplissage alvéolaire variable) et la consolidation peuvent apparaître au fur et à mesure que la maladie progresse. [134] [148] Caractéristiques d’imagerie caractéristiques sur les radiographies thoraciques et la tomodensitométrie(TDM) des personnes symptomatiques comprennent des opacités périphériques asymétriques en verre dépoli sans épanchement pleural . [149]
De nombreux groupes ont créé des ensembles de données COVID-19 qui incluent des images, comme la Société italienne de radiologie qui a compilé une base de données internationale en ligne des résultats d’imagerie pour les cas confirmés. [150] En raison du chevauchement avec d’autres infections telles que l’adénovirus , l’imagerie sans confirmation par rRT-PCR est d’une spécificité limitée pour l’identification de la COVID‐19. [149] Une vaste étude en Chine a comparé les résultats du scanner thoracique à la PCR et a démontré que bien que l’imagerie soit moins spécifique de l’infection, elle est plus rapide et plus sensible . [133]
Codage
Fin 2019, l’OMS a attribué les codes de maladie d’urgence CIM-10 U07.1 pour les décès dus à une infection par le SRAS-CoV-2 confirmée en laboratoire et U07.2 pour les décès dus au COVID‐19 diagnostiqué cliniquement ou épidémiologiquement sans SRAS-CoV-confirmé en laboratoire. 2 infections. [151]
Pathologie
Les principales constatations pathologiques à l’autopsie sont les suivantes :
- Macroscopie : péricardite , condensation pulmonaire et œdème pulmonaire [118]
- Résultats pulmonaires :
- exsudation séreuse mineure , exsudation mineure de fibrine [118]
- œdème pulmonaire, hyperplasie des pneumocytes , gros pneumocytes atypiques , inflammation interstitielle avec infiltration lymphocytaire et formation de cellules géantes multinucléées [118]
- lésions alvéolaires diffuses (DAD) avec exsudats alvéolaires diffus . Le DAD est la cause du syndrome de détresse respiratoire aiguë (SDRA) et de l’ hypoxémie sévère . [118]
- organisation des exsudats dans les cavités alvéolaires et fibrose interstitielle pulmonaire [118]
- plasmocytose dans BAL [152]
- Sang et vaisseaux : coagulation intravasculaire disséminée (CIVD) ; [153] réaction leucoérythroblastique, [154] endothéliite , [155] hémophagocytose [155]
- Cœur : nécrose des cellules musculaires cardiaques [155]
- Foie : stéatose microvésiculaire [118]
- Nez : excrétion de l’épithélium olfactif [95]
- Cerveau : infarctus [155]
- Reins : lésions tubulaires aiguës. [155]
- Rate : épuisement de la pulpe blanche . [155]
La prévention

 Sans mesures de confinement de la pandémie – telles que la distanciation sociale, la vaccination et les masques faciaux – les agents pathogènes peuvent se propager de manière exponentielle. [156] Ce graphique montre comment l’adoption précoce de mesures de confinement tend à protéger des pans plus larges de la population.
Sans mesures de confinement de la pandémie – telles que la distanciation sociale, la vaccination et les masques faciaux – les agents pathogènes peuvent se propager de manière exponentielle. [156] Ce graphique montre comment l’adoption précoce de mesures de confinement tend à protéger des pans plus larges de la population.
Les mesures préventives pour réduire les risques d’infection consistent à se faire vacciner, à rester à la maison, à porter un masque en public, à éviter les endroits bondés, à se tenir à distance des autres, à ventiler les espaces intérieurs, à gérer les durées d’exposition potentielles, [157] à se laver souvent les mains à l’eau et au savon et pendant au moins vingt secondes, en pratiquant une bonne hygiène respiratoire et en évitant de se toucher les yeux, le nez ou la bouche avec des mains non lavées. [158] [159]
Les personnes diagnostiquées avec COVID-19 ou qui pensent qu’elles peuvent être infectées sont invitées par le CDC à rester à la maison, sauf pour obtenir des soins médicaux, à appeler à l’avance avant de consulter un prestataire de soins de santé, à porter un masque facial avant d’entrer dans le bureau du prestataire de soins de santé et dans n’importe quelle pièce ou véhicule avec une autre personne, couvrez la toux et les éternuements avec un mouchoir, lavez-vous régulièrement les mains à l’eau et au savon et évitez de partager des articles ménagers personnels. [160] [161]
Le premier vaccin COVID‐19 a obtenu l’approbation réglementaire le 2 décembre 2020 par l’autorité britannique de réglementation des médicaments MHRA . [162] Il a été évalué pour le statut d’ autorisation d’utilisation d’urgence (EUA) par la FDA américaine et dans plusieurs autres pays. [163] Initialement, les directives des National Institutes of Health des États-Unis ne recommandent aucun médicament pour la prévention de la COVID‐19, avant ou après l’exposition au virus SARS-CoV-2, en dehors du cadre d’un essai clinique. [164] [165]En l’absence de vaccin, d’autres mesures prophylactiques ou de traitements efficaces, un élément clé de la gestion de la COVID‐19 consiste à tenter de diminuer et de retarder le pic épidémique, connu sous le nom d'”aplatissement de la courbe “. [166] Cela se fait en ralentissant le taux d’infection pour réduire le risque de surcharge des services de santé, en permettant un meilleur traitement des cas actifs et en retardant les cas supplémentaires jusqu’à ce que des traitements efficaces ou un vaccin soient disponibles. [166] [167]
Vaccin

 Centre de vaccination COVID-19 de l’ Université de médecine de Gdańsk , Pologne
Centre de vaccination COVID-19 de l’ Université de médecine de Gdańsk , Pologne 
 Différents types de vaccins candidats en développement pour le SRAS-CoV-2
Différents types de vaccins candidats en développement pour le SRAS-CoV-2
Un vaccin COVID‐19 est un vaccin destiné à fournir une immunité acquise contre le coronavirus 2 du syndrome respiratoire aigu sévère (SRAS‐CoV‐2), le virus qui cause la maladie à coronavirus 2019 ( COVID‐19 ).
Avant la pandémie de COVID‐19 , il existait un ensemble établi de connaissances sur la structure et la fonction des coronavirus causant des maladies comme le syndrome respiratoire aigu sévère (SRAS) et le syndrome respiratoire du Moyen-Orient (MERS). Ces connaissances ont accéléré le développement de diverses plateformes de vaccins au début de 2020. [168] L’objectif initial des vaccins contre le SRAS-CoV-2 était de prévenir les maladies symptomatiques, souvent graves. [169] Le 10 janvier 2020, les données de séquence génétique du SARS-CoV-2 ont été partagées via GISAID et, le 19 mars, l’industrie pharmaceutique mondiale a annoncé un engagement majeur pour lutter contre le COVID‐19.[170]
Les vaccins contre la COVID‐19 sont largement reconnus pour leur rôle dans la réduction de la gravité et des décès causés par la COVID‐19. [171] [172] De nombreux pays ont mis en place des plans de distribution progressive qui donnent la priorité aux personnes les plus à risque de complications, comme les personnes âgées, et celles à haut risque d’exposition et de transmission, comme les travailleurs de la santé. [173]
Au 11 mai 2022 [update], 11,68 milliards de doses de vaccins COVID‐19 ont été administrées dans le monde sur la base des rapports officiels des agences nationales de santé publique . [174] En décembre 2020, plus de 10 milliards de doses de vaccin avaient été précommandées par les pays, [175] avec environ la moitié des doses achetées par les pays à revenu élevé comprenant 14 % de la population mondiale. [176]
Malgré le développement extrêmement rapide de vaccins efficaces à base d’ ARNm et de vecteurs viraux , l’ équité mondiale en matière de vaccins n’a pas été atteinte. Le développement et l’utilisation de virus entiers inactivés (WIV) et de vaccins à base de protéines ont également été recommandés, en particulier pour une utilisation dans les pays en développement en développement . [177] [178]
Masques faciaux et hygiène respiratoire

 Masques avec soupape d’expiration. Les valves sont un point faible qui peut transmettre les virus vers l’extérieur.
Masques avec soupape d’expiration. Les valves sont un point faible qui peut transmettre les virus vers l’extérieur.
L’OMS et le CDC américain recommandent aux individus de porter des couvre-visages non médicaux dans les lieux publics où il existe un risque accru de transmission et où les mesures de distanciation sociale sont difficiles à maintenir. [179] [180] Cette recommandation vise à réduire la propagation de la maladie par les personnes asymptomatiques et pré-symptomatiques et est complémentaire aux mesures préventives établies telles que la distanciation sociale. [180] [181] Les couvre-visages limitent le volume et la distance parcourue par les gouttelettes expiratoires dispersées lors de la conversation, de la respiration et de la toux. [180] [181] Un couvre-visage sans évents ni trous filtrera également les particules contenant le virus de l’air inhalé et expiré, réduisant ainsi les risques d’infection.[182] Mais, si le masque comprend une valve d’expiration , un porteur infecté (peut-être sans l’avoir remarqué, et asymptomatique) transmettra le virus vers l’extérieur à travers lui, malgré toute certification qu’il peut avoir. Ainsi, les masques avec soupape d’expiration ne sont pas destinés aux porteurs infectés et ne sont pas fiables pour arrêter la pandémie à grande échelle. De nombreux pays et juridictions locales encouragent ou imposent l’utilisation de masques faciaux ou de couvre-visages en tissu par les membres du public pour limiter la propagation du virus. [183]
Les masques sont également fortement recommandés pour les personnes susceptibles d’avoir été infectées et celles qui s’occupent d’une personne susceptible d’avoir la maladie. [184] Lorsque vous ne portez pas de masque, le CDC recommande de vous couvrir la bouche et le nez avec un mouchoir lorsque vous toussez ou éternuez et recommande d’utiliser l’intérieur du coude si aucun mouchoir n’est disponible. Une bonne hygiène des mains après une toux ou un éternuement est encouragée. Il est conseillé aux professionnels de la santé qui interagissent directement avec des personnes atteintes de la COVID‐19 d’utiliser des respirateurs au moins aussi protecteurs que le N95 certifié NIOSH ou l’équivalent, en plus d’autres équipements de protection individuelle . [185]
Ventilation intérieure et évitement des espaces intérieurs encombrés
Le CDC recommande d’éviter les espaces intérieurs bondés. [186] À l’intérieur, l’augmentation du taux de renouvellement de l’air, la diminution de la recirculation de l’air et l’augmentation de l’utilisation de l’air extérieur peuvent réduire la transmission. [186] [187] L’OMS recommande la ventilation et la filtration de l’air dans les espaces publics pour aider à éliminer les aérosols infectieux. [188] [189] [190]
Les particules respiratoires expirées peuvent s’accumuler dans des espaces clos avec une ventilation inadéquate . Le risque d’infection par la COVID‐19 augmente en particulier dans les espaces où les personnes s’adonnent à des efforts physiques ou élèvent la voix (par exemple, faire de l’exercice, crier, chanter), car cela augmente l’expiration des gouttelettes respiratoires. Une exposition prolongée à ces conditions, généralement plus de 15 minutes, entraîne un risque d’infection plus élevé. [186]
La ventilation par déplacement avec de grandes entrées naturelles peut déplacer l’air vicié directement vers l’échappement en flux laminaire tout en réduisant considérablement la concentration de gouttelettes et de particules. La ventilation passive réduit la consommation d’énergie et les coûts de maintenance, mais peut manquer de contrôlabilité et de récupération de chaleur. La ventilation par déplacement peut également être réalisée mécaniquement avec des coûts énergétiques et de maintenance plus élevés. L’utilisation de conduits et d’ouvertures de grande taille permet d’éviter le mélange dans les environnements fermés. La recirculation et le mélange doivent être évités car la recirculation empêche la dilution des particules nocives et redistribue l’air éventuellement contaminé, et le mélange augmente la concentration et la gamme de particules infectieuses et maintient les particules plus grosses dans l’air. [191]
Lavage des mains et hygiène

 Des étudiants rwandais se lavent les mains et portent des masques faciaux pendant la pandémie de COVID‐19 dans le pays .
Des étudiants rwandais se lavent les mains et portent des masques faciaux pendant la pandémie de COVID‐19 dans le pays .
Une bonne hygiène des mains après une toux ou un éternuement est nécessaire. [192] L’OMS recommande également de se laver souvent les mains à l’eau et au savon pendant au moins vingt secondes, surtout après être allé aux toilettes ou lorsque les mains sont visiblement sales, avant de manger et après s’être mouché. [193] Lorsque l’eau et le savon ne sont pas disponibles, le CDC recommande d’utiliser un désinfectant pour les mains à base d’alcool contenant au moins 60 % d’alcool. [194] Pour les zones où les désinfectants pour les mains commerciaux ne sont pas facilement disponibles, l’OMS propose deux formulations pour la production locale. Dans ces formulations, l’activité antimicrobienne provient de l’ éthanol ou est utilisée pour aider à éliminer les spores bactériennes de l’ isopropanol . Peroxyde d’hydrogène dans l’alcool; ce n’est “pas une substance active pour l’ antisepsie des mains “. Le glycérol est ajouté comme humectant . [195]
Distanciation sociale
La distanciation sociale (également connue sous le nom de distanciation physique) comprend des actions de contrôle des infections destinées à ralentir la propagation de la maladie en minimisant les contacts étroits entre les individus. Les méthodes incluent les quarantaines ; restrictions de voyage; et la fermeture d’écoles, de lieux de travail, de stades, de théâtres ou de centres commerciaux. Les individus peuvent appliquer des méthodes de distanciation sociale en restant à la maison, en limitant les déplacements, en évitant les zones surpeuplées, en utilisant des salutations sans contact et en se distanciant physiquement des autres. [196] De nombreux gouvernements imposent ou recommandent désormais la distanciation sociale dans les régions touchées par l’épidémie.[197]
Des épidémies se sont produites dans les prisons en raison de la surpopulation et de l’incapacité à imposer une distanciation sociale adéquate. [198] [199] Aux États-Unis, la population carcérale vieillit et beaucoup d’entre eux courent un risque élevé de mauvais résultats à cause de la COVID-19 en raison des taux élevés de maladies cardiaques et pulmonaires coexistantes et d’un accès limité à des soins de santé de haute qualité. . [198]
Nettoyage des surfaces
Après avoir été expulsés du corps, les coronavirus peuvent survivre sur des surfaces pendant des heures, voire des jours. Si une personne touche la surface sale, elle peut déposer le virus dans les yeux, le nez ou la bouche où il peut pénétrer dans le corps et provoquer une infection. [200] Les preuves indiquent que le contact avec des surfaces infectées n’est pas le principal moteur de la COVID‐19, [201] [202] [203] conduisant à des recommandations pour des procédures de désinfection optimisées afin d’éviter des problèmes tels que l’augmentation de la résistance aux antimicrobiens par l’utilisation de produits et procédés de nettoyage inappropriés. [204] [205] , donnant un faux sentiment de sécurité contre quelque chose qui se répand principalement dans les airs. [206] [207] Le nettoyage en profondeur et autres assainissements de surface ont été critiqués comme théâtre d’hygiène
La durée de survie du virus dépend considérablement du type de surface, de la température et de l’humidité. [208] Les coronavirus meurent très rapidement lorsqu’ils sont exposés à la lumière UV du soleil . [208] Comme d’autres virus enveloppés, le SRAS-CoV-2 survit le plus longtemps lorsque la température est à température ambiante ou inférieure, et lorsque l’ humidité relative est faible (<50%). [208]
Sur de nombreuses surfaces, y compris le verre, certains types de plastique, l’acier inoxydable et la peau, le virus peut rester infectieux pendant plusieurs jours à l’intérieur à température ambiante, voire environ une semaine dans des conditions idéales. [208] [209] Sur certaines surfaces, y compris le tissu de coton et le cuivre, le virus meurt généralement après quelques heures. [208] Le virus meurt plus rapidement sur les surfaces poreuses que sur les surfaces non poreuses en raison de l’action capillaire dans les pores et de l’évaporation plus rapide des gouttelettes d’aérosol. [210] [203] [208] Cependant, parmi les nombreuses surfaces testées, deux avec les temps de survie les plus longs sont les masques respiratoires N95 et les masques chirurgicaux, qui sont tous deux considérés comme des surfaces poreuses. [208]
Le CDC affirme que dans la plupart des situations, le nettoyage des surfaces avec du savon ou du détergent, et non la désinfection, suffit à réduire le risque de transmission. [211] [212] Le CDC recommande que si un cas de COVID‐19 est suspecté ou confirmé dans un établissement tel qu’un bureau ou une garderie, toutes les zones telles que les bureaux, les salles de bains, les espaces communs, les équipements électroniques partagés tels que les tablettes, les écrans tactiles , les claviers, les télécommandes et les guichets automatiques utilisés par les personnes malades doivent être désinfectés. [213] Les surfaces peuvent être décontaminées avec 62 à 71 % d’ éthanol , 50 à 100 % d’isopropanol, 0,1 % d’hypochlorite de sodium , 0,5 % de peroxyde d’hydrogène, 0,2 à 7,5 % de povidone iodée ou 50 à 200 ppm d’acide hypochloreux.. D’autres solutions, comme le chlorure de bien que les dispositifs populaires nécessitentle chlorure de benzalkonium et le gluconate de chlorhexidine , sont moins efficaces. L’irradiation germicide ultraviolette peut également être utilisée, [188]5 à 10 min d’exposition et peut détériorer certains matériaux avec le temps. [214] Une fiche technique comprenant les substances autorisées à la désinfection dans l’industrie alimentaire (y compris la suspension ou la surface testée, le type de surface, la dilution d’utilisation, les volumes de désinfectant et d’inocuylum) peut être consultée dans le matériel complémentaire de. [204]
Auto-isolement
L’auto-isolement à domicile a été recommandé pour les personnes diagnostiquées avec la COVID‐19 et celles qui soupçonnent qu’elles ont été infectées. Les agences de santé ont publié des instructions détaillées pour un auto-isolement approprié. [215] De nombreux gouvernements ont mandaté ou recommandé l’auto-quarantaine pour des populations entières. Les instructions d’auto-quarantaine les plus strictes ont été données aux personnes appartenant à des groupes à haut risque. [216] Ceux qui ont pu être exposés à une personne atteinte de la COVID‐19 et ceux qui ont récemment voyagé dans un pays ou une région où la transmission est généralisée ont été invités à s’auto-mettre en quarantaine pendant 14 jours à compter de la dernière exposition possible. [217]
Alimentation et mode de vie sains
La Harvard TH Chan School of Public Health recommande une alimentation saine, une activité physique, une gestion du stress psychologique et un sommeil suffisant. [218]
Il a été démontré que le respect constant des directives scientifiques de plus de 150 minutes par semaine d’ exercice ou d’activité physique similaire était associé à un risque d’hospitalisation et de décès dû à la COVID‐19 moindre, même en tenant compte des facteurs de risque probables tels qu’un indice de masse corporelle (IMC) élevé. . [219] [220]
Une méta-analyse, publiée en ligne en octobre 2021, a conclu que “la supplémentation en vitamine D chez les patients positifs pour le SRAS-CoV-2 a le potentiel d’avoir un impact positif sur les patients présentant des symptômes légers et graves”. [221] La plus grande étude observationnelle sur le sujet utilisant des questionnaires en ligne, avec plus de 6 000 participants et un régime posologique proche du RDI , devrait se conclure en juillet 2021. [222] [223] L’un des collaborateurs de l’étude est Synergy Biologics Ltd, un fabricant de suppléments de vitamine D3. [223]
Mesures de contrôle liées aux voyages internationaux
Une revue rapide Cochrane de 2021 a révélé que, sur la base de données probantes de faible certitude, les mesures de contrôle liées aux voyages internationaux, telles que la restriction des voyages transfrontaliers, peuvent aider à contenir la propagation de la COVID‐19. [224] De plus, les mesures de dépistage basées sur les symptômes/l’exposition aux frontières peuvent manquer de nombreux cas positifs. [224] Bien que les mesures de dépistage aux frontières basées sur des tests puissent être plus efficaces, elles pourraient également manquer de nombreux cas positifs si elles ne sont effectuées qu’à l’arrivée sans suivi. L’examen a conclu qu’une quarantaine d’au moins 10 jours peut être bénéfique pour prévenir la propagation de la COVID‐19 et peut être plus efficace si elle est associée à une mesure de contrôle supplémentaire comme le contrôle aux frontières. [224]
Traitement

 Un aperçu des thérapies et des médicaments COVID-19
Un aperçu des thérapies et des médicaments COVID-19
| Cet article doit être mis à jour . ( avril 2022 ) Please help update this article to reflect recent events or newly available information. |
Jusqu’à récemment, il n’existait aucun traitement ou remède spécifique et efficace pour la maladie à coronavirus 2019 (COVID‐19), la maladie causée par le virus SRAS-CoV-2 . [225] [ nécessite une mise à jour ] , [226] mais depuis avril 2022, plusieurs médicaments ont été approuvés dans différents pays. Les patients présentant des symptômes légers à modérés qui appartiennent aux groupes à risque peuvent prendre du Nirmatrelvir/ritonavir (commercialisé sous le nom de Paxlovid) ou du Remdesivir , qui réduisent considérablement le risque de maladie grave ou d’hospitalisation. [227] Aux États-Unis, le plan d’action COVID-19 de l’administration Bidencomprend l’initiative Test to Treat, où les gens peuvent se rendre dans une pharmacie, passer un test COVID et recevoir immédiatement Paxlovid gratuit s’ils sont positifs. [228]
Des vaccins hautement efficaces ont réduit la mortalité liée au SRAS-CoV-2 ; cependant, pour ceux qui attendent d’être vaccinés, ainsi que pour les millions estimés de personnes immunodéprimées qui sont peu susceptibles de répondre de manière robuste à la vaccination, le traitement reste important. [229] La pierre angulaire de la prise en charge de la COVID‐19 a été les soins de soutien , qui comprennent un traitement pour soulager les symptômes , la fluidothérapie , l’apport d’oxygène et le positionnement en décubitus ventral au besoin, ainsi que des médicaments ou des dispositifs pour soutenir d’autres organes vitaux touchés. [230] [231] [232]
La plupart des cas de COVID‐19 sont bénins. Dans ces cas, les soins de soutien comprennent des médicaments tels que le paracétamol ou les AINS pour soulager les symptômes (fièvre, courbatures, toux), un apport adéquat en liquides, du repos et une respiration nasale . [233] [226] [234] [235] Une bonne hygiène personnelle et une alimentation saine sont également recommandées. [236] Les Centers for Disease Control and Prevention (CDC) des États-Unis recommandent à ceux qui soupçonnent d’être porteurs du virus de s’isoler chez eux et de porter un masque facial.[237]
Les personnes atteintes de cas plus graves peuvent avoir besoin d’un traitement à l’hôpital. Chez les personnes à faible taux d’oxygène, l’utilisation de la dexaméthasone , un glucocorticoïde , est fortement recommandée, car elle peut réduire le risque de décès. [238] [239] [240] La ventilation non envahissante et, finalement, l’admission à une unité de soins intensifs pour la ventilation mécanique peuvent être exigées pour soutenir la respiration. [241] L’oxygénation par membrane extracorporelle (ECMO) a été utilisée pour résoudre le problème de l’insuffisance respiratoire, mais ses avantages sont toujours à l’étude. [242] [243]Certains des cas d’évolution grave de la maladie sont causés par une hyper-inflammation systémique, la soi-disant tempête de cytokines . [244]
Pronostic
La gravité de la COVID‐19 varie. La maladie peut suivre une évolution bénigne avec peu ou pas de symptômes, ressemblant à d’autres maladies courantes des voies respiratoires supérieures telles que le rhume . Dans 3 à 4 % des cas (7,4 % pour les plus de 65 ans), les symptômes sont suffisamment graves pour entraîner une hospitalisation. [245] Les cas bénins se rétablissent généralement en deux semaines, tandis que ceux atteints de maladies graves ou critiques peuvent prendre de trois à six semaines pour se rétablir. Parmi ceux qui sont décédés, le délai entre l’apparition des symptômes et le décès a varié de deux à huit semaines. [75] L’ Istituto Superiore di Sanità italien ont rapporté que le délai médian entre le début des symptômes et le décès était de douze jours, dont sept ont été hospitalisés. Cependant, les personnes transférées en unité de soins intensifs avaient un délai médian de dix jours entre l’hospitalisation et le décès. [246] Un temps de prothrombine prolongé et des taux élevés de protéine C-réactive à l’admission à l’hôpital sont associés à une évolution sévère de la COVID‐19 et à un transfert aux soins intensifs. [247] [248]
Certaines études préliminaires suggèrent que 10 à 20 % des personnes atteintes de la COVID‐19 présenteront des symptômes durant plus d’un mois . [249] [250] La majorité de ceux qui ont été admis à l’hôpital avec une maladie grave signalent des problèmes à long terme, notamment de la fatigue et un essoufflement. [251] Le 30 octobre 2020, le chef de l’OMS, Tedros Adhanoma averti que “pour un nombre important de personnes, le virus COVID pose une série d’effets graves à long terme”. Il a décrit le vaste éventail de symptômes de la COVID‐19 qui fluctuent au fil du temps comme « vraiment préoccupant ». Ils vont de la fatigue, de la toux et de l’essoufflement à l’inflammation et aux lésions des principaux organes, y compris les poumons et le cœur, ainsi qu’aux effets neurologiques et psychologiques. Les symptômes se chevauchent souvent et peuvent affecter n’importe quel système du corps. Les personnes infectées ont signalé des épisodes cycliques de fatigue, des maux de tête, des mois d’épuisement complet, des sautes d’humeur et d’autres symptômes. Tedros a donc conclu qu’une stratégie visant à obtenir une immunité collective par infection, plutôt que par vaccination, est “moralement inadmissible et irréalisable”. [252]
En termes de réadmissions à l’hôpital, environ 9 % des 106 000 personnes ont dû revenir pour un traitement hospitalier dans les deux mois suivant leur sortie. La moyenne de réadmission était de huit jours depuis la première visite à l’hôpital. Plusieurs facteurs de risque ont été identifiés comme étant une cause d’admissions multiples dans un établissement hospitalier. Parmi ceux-ci figurent l’âge avancé (plus de 65 ans) et la présence d’une maladie chronique comme le diabète, la MPOC, l’insuffisance cardiaque ou la maladie rénale chronique. [253] [254]
Selon des revues scientifiques, les fumeurs sont plus susceptibles de nécessiter des soins intensifs ou de mourir que les non-fumeurs. [255] [256] Agissant sur les mêmes récepteurs pulmonaires ACE2 affectés par le tabagisme, la pollution de l’air a été corrélée à la maladie. [256] L’exposition à court terme [257] et chronique [258] à la pollution de l’air semble accroître la morbidité et la mortalité liées à la COVID‐19. [259] [260] [261] Les maladies cardiaques et pulmonaires préexistantes [262] ainsi que l’obésité , en particulier en conjonction avec la stéatose hépatique , contribuent à un risque accru de COVID‐19 pour la santé. [256][263] [264] [265]
On suppose également que les personnes immunodéprimées courent un risque plus élevé de tomber gravement malades à cause du SRAS-CoV-2. [266] Une recherche portant sur les infections au COVID‐19 chez les receveurs de greffe de rein hospitalisés a révélé un taux de mortalité de 11 %. [267]
La génétique joue également un rôle important dans la capacité à combattre la maladie. [268] Par exemple, ceux qui ne produisent pas d’ interférons de type I détectables ou qui ne produisent pas d’ auto-anticorps contre ceux-ci peuvent devenir beaucoup plus malades à cause de la COVID‐19. [269] [270] Le dépistage génétique permet de détecter les gènes effecteurs de l’interféron. [271]
Enfants
Alors que les très jeunes enfants ont connu des taux d’infection plus faibles, les enfants plus âgés ont un taux d’infection similaire à celui de la population dans son ensemble. [272] [273] Les enfants sont susceptibles d’avoir des symptômes plus légers et sont moins à risque de maladie grave que les adultes. [274] Le CDC rapporte qu’aux États-Unis, environ un tiers des enfants hospitalisés ont été admis aux soins intensifs, [275] tandis qu’une étude multinationale européenne sur les enfants hospitalisés de juin 2020 a révélé qu’environ 8 % des enfants admis dans un hôpital avaient besoin de soins intensifs. . [276] Quatre des 582 enfants (0,7%) de l’étude européenne sont décédés, mais le taux de mortalité réel peut être “sensiblement inférieur” puisque les cas moins graves qui n’ont pas recherché d’aide médicale n’ont pas été inclus dans l’étude.[277] [278]
Complications

 Mécanismes de la tempête de cytokines SARS-CoV-2 et complications
Mécanismes de la tempête de cytokines SARS-CoV-2 et complications
Les complications peuvent inclure une pneumonie , un syndrome de détresse respiratoire aiguë (SDRA), une défaillance multiviscérale , un choc septique et la mort. [279] [280] [281] [282] Les complications cardiovasculaires peuvent inclure l’insuffisance cardiaque, les arythmies (y compris la fibrillation auriculaire ), l’inflammation cardiaque et la thrombose , en particulier la thromboembolie veineuse . [283] [284] [285] [286] [287] [288] Environ 20 à 30 % des personnes qui se présentent avec la COVID‐19 ont des enzymes hépatiques élevées, ce qui reflète une atteinte hépatique.[289] [165]
Les manifestations neurologiques comprennent les convulsions , les accidents vasculaires cérébraux, l’encéphalite et le syndrome de Guillain-Barré (qui comprend la perte des fonctions motrices ). [290] [291] Suite à l’infection, les enfants peuvent développer un syndrome inflammatoire multisystémique pédiatrique , qui présente des symptômes similaires à la maladie de Kawasaki , qui peut être fatale. [292] [293] Dans de très rares cas, une encéphalopathie aiguë peut survenir, et elle peut être envisagée chez les personnes qui ont reçu un diagnostic de COVID‐19 et dont l’état mental est altéré. [294]
Dans le cas des femmes enceintes, il est important de noter que, selon les Centers for Disease Control and Prevention , les femmes enceintes courent un risque accru de tomber gravement malades à cause de la COVID‐19. [295] En effet, les femmes enceintes atteintes de COVID‐19 semblent plus susceptibles de développer des complications respiratoires et obstétriques pouvant entraîner une fausse couche , un accouchement prématuré et un retard de croissance intra -utérin . [295]
Des infections fongiques telles que l’ aspergillose , la candidose , la cryptococcose et la mucormycose ont été enregistrées chez des patients se remettant de la COVID‐19. [296] [297]
Effets à plus long terme
Certaines premières études suggèrent que 10 à 20 % des personnes atteintes de COVID‐19 présenteront des symptômes durant plus d’un mois. [298] [250] La majorité de ceux qui ont été admis à l’hôpital avec une maladie grave signalent des problèmes à long terme, notamment de la fatigue et un essoufflement. [299] Environ 5 à 10 % des patients admis à l’hôpital évoluent vers une maladie grave ou critique, notamment une pneumonie et une insuffisance respiratoire aiguë. [300]
Par divers mécanismes, les poumons sont les organes les plus touchés par la COVID‐19. [301] Chez les personnes nécessitant une hospitalisation, jusqu’à 98 % des tomodensitogrammes réalisés montrent des anomalies pulmonaires après 28 jours de maladie, même si elles se sont améliorées cliniquement. [302]
Les personnes ayant un âge avancé, une maladie grave, des séjours prolongés aux soins intensifs ou qui fument sont plus susceptibles d’avoir des effets à long terme, y compris la fibrose pulmonaire. [303] Dans l’ensemble, environ un tiers des personnes étudiées après quatre semaines auront des résultats de fibrose pulmonaire ou de fonction pulmonaire réduite telle que mesurée par DLCO , même chez les personnes asymptomatiques, mais avec la suggestion d’une amélioration continue au fil du temps. [301]
Immunité

 Réponse des anticorps humains à l’infection par le SRAS-CoV-2
Réponse des anticorps humains à l’infection par le SRAS-CoV-2
La réponse immunitaire des humains au virus SARS-CoV-2 se produit comme une combinaison de l’ immunité à médiation cellulaire et de la production d’anticorps, [304] comme pour la plupart des autres infections. [305] Les lymphocytes B interagissent avec les lymphocytes T et commencent à se diviser avant la sélection dans le plasmocyte, en partie sur la base de leur affinité pour l’antigène. [306] Étant donné que le SRAS-CoV-2 n’est présent dans la population humaine que depuis décembre 2019, on ne sait toujours pas si l’ immunité est durable chez les personnes qui se remettent de la maladie. [307]La présence d’anticorps neutralisants dans le sang est fortement corrélée à la protection contre l’infection, mais le niveau d’anticorps neutralisants diminue avec le temps. Les personnes atteintes d’une maladie asymptomatique ou bénigne avaient des niveaux indétectables d’anticorps neutralisants deux mois après l’infection. Dans une autre étude, le niveau d’anticorps neutralisants a été multiplié par quatre un à quatre mois après l’apparition des symptômes. Cependant, le manque d’anticorps dans le sang ne signifie pas que les anticorps ne seront pas produits rapidement lors d’une réexposition au SRAS-CoV-2. Les cellules B mémoire spécifiques des protéines de pointe et de nucléocapside du SRAS-CoV-2 durent au moins six mois après l’apparition des symptômes. [307]
La réinfection par la COVID‐19 est possible mais peu fréquente. Le premier cas de réinfection a été documenté en août 2020. [308] Une revue systématique a trouvé 17 cas de réinfection confirmés dans la littérature médicale en mai 2021. [308]
Mortalité
Plusieurs mesures sont couramment utilisées pour quantifier la mortalité. [309] Ces chiffres varient selon la région et au fil du temps et sont influencés par le volume de tests, la qualité du système de santé, les options de traitement, le temps écoulé depuis l’épidémie initiale et les caractéristiques de la population telles que l’âge, le sexe et l’état de santé général. [310]
Le taux de mortalité reflète le nombre de décès au sein d’un groupe démographique spécifique divisé par la population de ce groupe démographique. Par conséquent, le taux de mortalité reflète la prévalence ainsi que la gravité de la maladie au sein d’une population donnée. Les taux de mortalité sont fortement corrélés à l’âge, avec des taux relativement faibles chez les jeunes et des taux relativement élevés chez les personnes âgées. [311] [312] [313] En fait, un facteur pertinent des taux de mortalité est la structure par âge des populations des pays. Par exemple, le taux de létalité du COVID-19 est plus faible en Inde qu’aux États-Unis, car la population plus jeune de l’Inde représente un pourcentage plus élevé qu’aux États-Unis. [314]
Taux de létalité
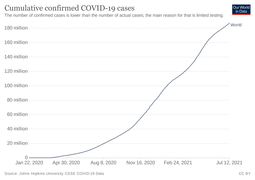
Le taux de létalité (CFR) reflète le nombre de décès divisé par le nombre de cas diagnostiqués dans un intervalle de temps donné. D’après les statistiques de l’Université Johns Hopkins, le ratio mondial décès/cas est de 1,20 % (6 264 097/521 544 771) au 16 mai 2022. [6] Le nombre varie selon les régions. [315] [316]
-
![]()
![]()
Total des cas confirmés au fil du temps
-
![]()
![]()
Nombre total de cas confirmés de COVID‐19 par million de personnes [317]
-
![]()
![]()
Nombre total de décès au fil du temps
-
![]()
![]()
Nombre total de décès confirmés dus au COVID‐19 par million de personnes [318]
Taux de mortalité par infection
Une mesure clé pour évaluer la gravité de la COVID‐19 est le taux de mortalité par infection (IFR), également appelé taux de mortalité par infection ou risque de mortalité par infection . [319] [320] [321] Cette mesure est calculée en divisant le nombre total de décès dus à la maladie par le nombre total d’individus infectés ; par conséquent, contrairement au CFR , l’IFR intègre les infections asymptomatiques et non diagnostiquées ainsi que les cas signalés. [322]
Estimations 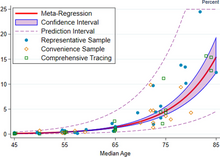
 La ligne rouge montre l’estimation du taux de mortalité par infection (IFR), en pourcentage, en fonction de l’âge. La région ombrée représente l’intervalle de confiance à 95 % pour cette estimation. Les marqueurs désignent des observations spécifiques utilisées dans la méta-analyse. [323]
La ligne rouge montre l’estimation du taux de mortalité par infection (IFR), en pourcentage, en fonction de l’âge. La région ombrée représente l’intervalle de confiance à 95 % pour cette estimation. Les marqueurs désignent des observations spécifiques utilisées dans la méta-analyse. [323] 
 La même relation tracée sur une échelle logarithmique
La même relation tracée sur une échelle logarithmique
Une revue systématique et une méta-analyse de décembre 2020 ont estimé que l’IFR de la population au cours de la première vague de la pandémie était d’environ 0,5 % à 1 % dans de nombreux endroits (dont la France, les Pays-Bas, la Nouvelle-Zélande et le Portugal), de 1 % à 2 % dans d’autres (Australie, Angleterre, Lituanie et Espagne) et a dépassé 2 % en Italie. [323] Cette étude a également révélé que la plupart de ces différences d’IFR reflétaient des différences correspondantes dans la composition par âge de la population et les taux d’infection par âge; en particulier, l’estimation par métarégression de l’IFR est très faible pour les enfants et les jeunes adultes (par exemple, 0,002 % à 10 ans et 0,01 % à 25 ans), mais augmente progressivement à 0,4 % à 55 ans, 1,4 % à 65 ans, 4,6 % à 25 ans. 75 ans et 15 % à 85 ans. [323]Ces résultats ont également été mis en évidence dans un rapport de décembre 2020 publié par l’OMS. [324]
| Tranche d’âge | IFR |
|---|---|
| 0–34 | 0,004 % |
| 35–44 | 0,068 % |
| 45–54 | 0,23 % |
| 55–64 | 0,75 % |
| 65–74 | 2,5 % |
| 75–84 | 8,5 % |
| 85 + | 28,3 % |
Une analyse de ces taux IFR indique que la COVID-19 est dangereuse non seulement pour les personnes âgées, mais aussi pour les adultes d’âge moyen, pour lesquels le taux de mortalité par infection de la COVID-19 est supérieur de deux ordres de grandeur au risque annualisé d’une automobile mortelle accident et bien plus dangereux que la grippe saisonnière. [323]
Estimations antérieures de l’IFR
À un stade précoce de la pandémie, l’Organisation mondiale de la santé a rapporté des estimations d’IFR entre 0,3% et 1%. [325] [326] Le 2 juillet, le scientifique en chef de l’OMS a signalé que l’estimation moyenne de l’IFR présentée lors d’un forum d’experts de l’OMS de deux jours était d’environ 0,6 %. [327] [328] En août, l’OMS a découvert que des études incorporant des données provenant de tests sérologiques étendus en Europe montraient des estimations d’IFR convergeant vers environ 0,5 à 1 %. [329] Des limites inférieures fermes d’IFR ont été établies dans un certain nombre d’endroits tels que New York et Bergame en Italie puisque l’IFR ne peut pas être inférieur au taux de mortalité de la population. (Après un temps suffisant cependant, les gens peuvent être réinfectés). [330]Au 10 juillet, à New York, avec une population de 8,4 millions d’habitants, 23 377 personnes (18 758 confirmées et 4 619 probables) sont décédées du COVID‐19 (0,3 % de la population). [331] Les tests d’anticorps à New York ont suggéré un IFR d’environ 0,9 %, [332] et d’environ 1,4 %. [333] Dans la province de Bergame , 0,6 % de la population est décédée. [334] En septembre 2020, les Centers for Disease Control and Prevention (CDC) des États-Unis ont publié des estimations préliminaires des IFR par âge à des fins de planification de la santé publique. [335]
Différences entre les sexes
| Pourcentage de personnes infectées hospitalisées | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| 0–19 | 20–29 | 30–39 | 40–49 | 50–59 | 60–69 | 70–79 | 80+ | Total | |
| Femelle | 0,1 (0,07–0,2) |
0,5 (0,3–0,8) |
0,9 (0,5–1,5) |
1,3 (0,7–2,1) |
2,6 (1,5–4,2) |
5,1 (2,9–8,3) |
7,8 (4,4–12,8) |
19,3 (10,9–31,6) |
2,6 (1,5–4,3) |
| Homme | 0,2 (0,08–0,2) |
0,6 (0,3–0,9) |
1,2 (0,7–1,9) |
1,6 (0,9–2,6) |
3,2 (1,8–5,2) |
6,7 (3,7–10,9) |
11,0 (6,2–17,9) |
37,6 (21,1–61,3) |
3,3 (1,8–5,3) |
| Total | 0,1 (0,08–0,2) |
0,5 (0,3–0,8) |
1,1 (0,6–1,7) |
1,4 (0,8–2,3) |
2,9 (1,6–4,7) |
5,8 (3,3–9,5) |
9,3 (5,2–15,1) |
26,2 (14,8–42,7) |
2,9 (1,7–4,8) |
| Pourcentage de personnes hospitalisées qui vont à l’unité de soins intensifs | |||||||||
| 0–19 | 20–29 | 30–39 | 40–49 | 50–59 | 60–69 | 70–79 | 80+ | Total | |
| Femelle | 16,7 (14,3–19,3) |
8,7 (7,5–9,9) |
11,9 (10,9–13,0) |
16,6 (15,6–17,7) |
20,7 (19,8–21,6) |
23,1 (22,2–24,0) |
18,7 (18,0–19,5) |
4,2 (4,0–4,5) |
14,3 (13,9–14,7) |
| Homme | 26,9 (23,1–31,1) |
14,0 (12,2–16,0) |
19,2 (17,6–20,9) |
26,9 (25,4–28,4) |
33,4 (32,0–34,8) |
37,3 (36,0–38,6) |
30,2 (29,1–31,3) |
6,8 (6,5–7,2) |
23,1 (22,6–23,6) |
| Total | 22,2 (19,1–25,7) |
11,6 (10,1–13,2) |
15,9 (14,5–17,3) |
22,2 (21,0–23,5) |
27,6 (26,5–28,7) |
30,8 (29,8–31,8) |
24,9 (24,1–25,8) |
5,6 (5,3–5,9) |
19,0 (18,7–19,44) |
| Pourcentage de personnes hospitalisées qui meurent | |||||||||
| 0–19 | 20–29 | 30–39 | 40–49 | 50–59 | 60–69 | 70–79 | 80+ | Total | |
| Femelle | 0,5 (0,2–1,0) |
0,9 (0,5–1,3) |
1,5 (1,2–1,9) |
2,6 (2,3–3,0) |
5,2 (4,8–5,6) |
10,1 (9,5–10,6) |
16,7 (16,0–17,4) |
25,2 (24,4–26,0) |
14,4 (14,0–14,8) |
| Homme | 0,7 (0,3–1,5) |
1,3 (0,8–1,9) |
2,2 (1,7–2,7) |
3,8 (3,3–4,4) |
7,6 (7,0–8,2) |
14,8 (14,1–15,6) |
24,6 (23,7–25,6) |
37,1 (36,1–38,2) |
21,2 (20,8–21,7) |
| Total | 0,6 (0,2–1,3) |
1,1 (0,7–1,6) |
1,9 (1,5–2,3) |
3,3 (2,9–3,8) |
6,5 (6,0–7,0) |
12,6 (12,0–13,2) |
21,0 (20,3–21,7) |
31,6 (30,9–32,4) |
18,1 (17,8–18,4) |
| Pourcentage de personnes infectées qui meurent – taux de mortalité par infection (IFR) | |||||||||
| 0–19 | 20–29 | 30–39 | 40–49 | 50–59 | 60–69 | 70–79 | 80+ | Total | |
| Femelle | 0,001 (<0,001–0,002) |
0,004 (0,002–0,007) |
0,01 (0,007–0,02) |
0,03 (0,02–0,06) |
0,1 (0,08–0,2) |
0,5 (0,3–0,8) |
1,3 (0,7–2,1) |
4,9 (2,7–8,0) |
0,4 (0,2–0,6) |
| Homme | 0,001 (<0,001–0,003) |
0,007 (0,003–0,01) |
0,03 (0,02–0,05) |
0,06 (0,03–0,1) |
0,2 (0,1–0,4) |
1,0 (0,6–1,6) |
2,7 (1,5–1,4) |
14,0 (7,9–22,7) |
0,7 (0,4–1,1) |
| Total | 0,001 (<0,001–0,002) |
0,005 (0,003–0,01) |
0,02 (0,01–0,03) |
0,05 (0,03–0,08) |
0,2 (0,1–0,3) |
0,7 (0,4–1,2) |
1,9 (1,1–3,2) |
8,3 (4,7–13,5) |
0,5 (0,3–0,9) |
| Les nombres entre parenthèses sont des intervalles de crédibilité à 95 % pour les estimations. |
Les taux de létalité de la COVID-19 sont plus élevés chez les hommes que chez les femmes dans la plupart des pays. Cependant, dans quelques pays comme l’Inde, le Népal, le Vietnam et la Slovénie, les cas de décès sont plus élevés chez les femmes que chez les hommes. [314] À l’échelle mondiale, les hommes sont plus susceptibles d’être admis aux soins intensifs et plus susceptibles de mourir. [337] [338] Une méta-analyse a révélé qu’à l’échelle mondiale, les hommes étaient plus susceptibles de contracter la COVID‐19 que les femmes ; il y avait environ 55 hommes et 45 femmes pour 100 infections ( IC : 51,43–56,58). [339]
Le Centre chinois de contrôle et de prévention des maladies a indiqué que le taux de mortalité était de 2,8 % pour les hommes et de 1,7 % pour les femmes. [340] Des examens ultérieurs en juin 2020 ont indiqué qu’il n’y avait pas de différence significative de sensibilité ou de CFR entre les sexes. [341] [342] Un examen reconnaît les différents taux de mortalité chez les hommes chinois, suggérant qu’ils peuvent être attribuables à des choix de mode de vie tels que fumer et boire de l’alcool plutôt qu’à des facteurs génétiques. [343] Le tabagisme, qui dans certains pays comme la Chine est une activité principalement masculine, est une habitude qui contribue à augmenter de manière significative les taux de létalité chez les hommes. [314]Les différences immunologiques basées sur le sexe, la prévalence moindre du tabagisme chez les femmes et les hommes développant des conditions comorbides telles que l’hypertension à un âge plus jeune que les femmes pourraient avoir contribué à la mortalité plus élevée chez les hommes. [344] En Europe, en février 2020, 57 % des personnes infectées étaient des hommes et 72 % des personnes décédées du COVID‐19 étaient des hommes. [345] Depuis avril 2020, le gouvernement américain ne suit pas les données liées au sexe des infections au COVID‐19. [346] La recherche a montré que les maladies virales comme Ebola, le VIH, la grippe et le SRAS affectent différemment les hommes et les femmes. [346]
Différences ethniques
Aux États-Unis, une plus grande proportion de décès dus au COVID-19 est survenue parmi les Afro-Américains et d’autres groupes minoritaires. [347] Les facteurs structurels qui les empêchent de pratiquer la distanciation sociale comprennent leur concentration dans des logements insalubres surpeuplés et dans des professions « essentielles » telles que les épiciers, les employés des transports en commun, les travailleurs de la santé et le personnel d’entretien. Une plus grande prévalence de l’absence d’assurance maladie et de soins pour des affections sous-jacentes telles que le diabète , l’hypertension et les maladies cardiaques augmente également leur risque de décès. [348] Des problèmes similaires affectent les communautés amérindiennes et latino -américaines . [347]D’une part, en République dominicaine, il existe un exemple clair d’inégalité de genre et d’inégalité ethnique. Dans ce territoire latino-américain, il existe une grande inégalité et précarité qui touche particulièrement les femmes dominicaines, avec une plus grande emphase sur celles d’origine haïtienne. [349] Selon une politique de santé américaine à but non lucratif, 34 % des adultes non âgés des Amérindiens et des Autochtones de l’Alaska (AIAN) courent un risque de maladie grave, contre 21 % des adultes blancs non âgés. [350] La source l’attribue à des taux disproportionnellement élevés de nombreux problèmes de santé qui peuvent les exposer à un risque plus élevé ainsi qu’à des conditions de vie comme le manque d’accès à l’eau potable. [351]
Les dirigeants ont appelé à des efforts pour rechercher et remédier aux disparités. [352] Au Royaume-Uni, une plus grande proportion de décès dus au COVID‐19 sont survenus chez un Noir , des Asiatiques et d’autres minorités ethniques. [353] [354] [355] Des impacts plus graves sur les victimes, y compris l’incidence relative de la nécessité d’exigences d’hospitalisation, et la vulnérabilité à la maladie ont été associés via l’analyse de l’ADN pour être exprimés dans des variantes génétiques de la région chromosomique 3, des caractéristiques qui sont associé à l’ héritage néandertalien européen. Cette structure impose de plus grands risques que les personnes touchées développent une forme plus grave de la maladie. [356]Les découvertes sont du professeur Svante Pääbo et des chercheurs qu’il dirige à l’ Institut Max Planck d’anthropologie évolutive et au Karolinska Institutet . [356] On estime que ce mélange de gènes humains et néandertaliens modernes s’est produit il y a environ 50 000 à 60 000 ans en Europe du Sud. [356]
Comorbidités
Les facteurs biologiques (réponse immunitaire) et le comportement général (habitudes) peuvent fortement déterminer les conséquences de la COVID‐19. [314] La plupart des personnes qui meurent de la COVID‐19 ont des affections préexistantes (sous-jacentes) , notamment l’hypertension, le diabète sucré et les maladies cardiovasculaires . [357] Selon les données de mars des États-Unis, 89 % des personnes hospitalisées avaient des conditions préexistantes. [358] L’Istituto Superiore di Sanità italien a signalé que sur 8,8 % des décès pour lesquels des dossiers médicaux étaient disponibles, 96,1 % des personnes présentaient au moins une comorbidité , la personne moyenne ayant 3,4 maladies. [246] Selon ce rapport, les comorbidités les plus courantes sont l’hypertension (66 % des décès), le diabète de type 2 (29,8 % des décès), la cardiopathie ischémique (27,6 % des décès), la fibrillation auriculaire (23,1 % des décès) et l’insuffisance rénale chronique ( 20,2 % des décès).
Selon les Centers for Disease Control and Prevention (CDC), les comorbidités respiratoires les plus critiques sont : l’asthme modéré ou sévère , la MPOC préexistante , la fibrose pulmonaire , la fibrose kystique . [359] Les preuves issues de la méta-analyse de plusieurs documents de recherche de moindre envergure suggèrent également que le tabagisme peut être associé à de moins bons résultats. [360] [361] Lorsqu’une personne ayant des problèmes respiratoires existants est infectée par la COVID‐19, elle peut être plus à risque de présenter des symptômes graves. [362] La COVID‐19 présente également un risque plus élevé pour les personnes qui abusent des opioïdes et et de méthamphétamines , dans la mesure où leur consommation de drogue peut avoir causé des lésions pulmonaires. [363]
En août 2020, le CDC a émis une mise en garde selon laquelle les infections à la tuberculose (TB) pourraient augmenter le risque de maladie grave ou de décès. L’OMS a recommandé que les personnes présentant des symptômes respiratoires soient dépistées pour les deux maladies, car un test positif au COVID-19 ne pouvait pas exclure les co-infections. Certaines projections ont estimé qu’une détection réduite de la tuberculose due à la pandémie pourrait entraîner 6,3 millions de cas de tuberculose supplémentaires et 1,4 million de décès liés à la tuberculose d’ici 2025. [364]
Histoire
On pense que le virus est d’origine animale naturelle, très probablement par le biais d’ une infection contagieuse . [72] [365] [366] Il existe plusieurs théories sur l’ origine du cas index et des enquêtes sur l’origine de la pandémie sont en cours. [367] La phylogénétique estime que le SRAS-CoV-2 est apparu en octobre ou novembre 2019. [368] [369] [370] Une analyse d’algorithme phylogénétique a suggéré que le virus pouvait avoir circulé dans le Guangdong avant Wuhan. [371]Les preuves suggèrent qu’il descend d’un coronavirus qui infecte les chauves-souris sauvages et s’est propagé aux humains par l’intermédiaire d’un hôte sauvage intermédiaire. [372] [373] La possibilité que le virus ait été accidentellement libéré d’un laboratoire fait également l’objet d’un examen de plus en plus actif. [374] Les agences de renseignement américaines ont découvert que le virus n’a pas été développé comme une arme biologique et qu’il est peu probable qu’il ait été génétiquement modifié . [375]
Les premières infections humaines confirmées ont eu lieu à Wuhan , Hubei, Chine. Une étude des 41 premiers cas confirmés de COVID‐19, publiée en janvier 2020 dans The Lancet , a signalé que la première date d’apparition des symptômes était le 1er décembre 2019. [376] [377] [378] Des publications officielles de l’OMS ont rapporté la début des symptômes le 8 décembre 2019. [379] La transmission interhumaine a été confirmée par l’OMS et les autorités chinoises le 20 janvier 2020. [380] [381] Selon des sources officielles chinoises, celles-ci étaient principalement liées au Huanan Seafood Wholesale Market , qui vendait également des animaux vivants. [382] En mai 2020, George Gao, le directeur du CDC, a déclaré que des échantillons d’animaux prélevés sur le marché des fruits de mer avaient été testés négatifs pour le virus, indiquant que le marché était le site d’un événement précoce de super-propagation , mais qu’il n’était pas le site de l’épidémie initiale. [383] Des traces du virus ont été trouvées dans des échantillons d’eaux usées qui ont été prélevés à Milan et à Turin , en Italie, le 18 décembre 2019. [384]
En décembre 2019, la propagation de l’infection était presque entièrement due à la transmission interhumaine. [385] [386] Le nombre de cas de COVID-19 au Hubei a progressivement augmenté, atteignant soixante au 20 décembre [387] et au moins 266 au 31 décembre. [388] Le 24 décembre, l’hôpital central de Wuhan a envoyé un à l’hôpital provincial du Hubei, qui a informé le CDC de Wuhan Jianghan le 27 décembre. [390] Le 30 décembre, un rapport de test adressé à l’hôpital central de Wuhan, de la société CapitalBio Medlab, fait état d’un résultat positif erroné pour le SRAS échantillon de liquide de lavage bronchoalvéolaire (BAL) d’un cas clinique non résolu à la société de séquençage Vision Medicals. Les 27 et 28 décembre, Vision Medicals a informé l’hôpital central de Wuhan et le CDC chinois des résultats du test, montrant un nouveau coronavirus. [389] Un cluster de pneumonies de cause inconnue a été observé le 26 décembre et traité par le médecin Zhang Jixian, obligeant un groupe de médecins de l’hôpital central de Wuhan à alerter leurs collègues et les autorités hospitalières compétentes du résultat. La Commission municipale de la santé de Wuhan a publié un avis à diverses institutions médicales sur “le traitement de la pneumonie de cause inconnue” le soir même. [391] Huit de ces médecins, dont Li Wenliang (punie le 3 janvier), [392] ont ensuite été réprimandés par la police pour avoir répandu de fausses rumeurs et un autre, Ai Fen, a été réprimandée par ses supérieurs pour avoir donné l’alerte. [393]
La Commission municipale de la santé de Wuhan a fait la première annonce publique d’une épidémie de pneumonie de cause inconnue le 31 décembre, confirmant 27 cas [394] [395] [396] – suffisamment pour déclencher une enquête. [397]
Au début de l’épidémie, le nombre de cas doublait environ tous les sept jours et demi. [398] Au début et à la mi-janvier 2020, le virus s’est propagé à d’autres provinces chinoises , aidé par la migration du Nouvel An chinois et Wuhan étant une plaque tournante du transport et un important échangeur ferroviaire. [75] Le 20 janvier, la Chine a signalé près de 140 nouveaux cas en une journée, dont deux personnes à Pékin et une à Shenzhen . [399] Des données officielles ultérieures montrent que 6 174 personnes avaient déjà développé des symptômes à ce moment-là, [400] et d’autres pourraient avoir été infectées. [401] Un reportage dans The Lancetle 24 janvier, indiquait une transmission humaine, recommandait fortement un équipement de protection individuelle pour les agents de santé et déclarait que le dépistage du virus était essentiel en raison de son “potentiel pandémique”. [107] [402] Le 30 janvier, l’OMS a déclaré le COVID-19 une urgence de santé publique de portée internationale . [401] À ce moment-là, l’épidémie s’est propagée par un facteur de 100 à 200 fois. [403]
L’Italie a eu ses premiers cas confirmés le 31 janvier 2020, deux touristes en provenance de Chine. [404] L’Italie a dépassé la Chine en tant que pays avec le plus de décès le 19 mars 2020. [405] Le 26 mars, les États-Unis avaient dépassé la Chine et l’Italie avec le plus grand nombre de cas confirmés au monde. [406] La recherche sur les génomes des coronavirus indique que la majorité des cas de COVID-19 à New York provenaient de voyageurs européens, plutôt que directement de Chine ou de tout autre pays asiatique. [407] De nouveaux tests d’échantillons antérieurs ont trouvé une personne en France qui avait le virus le 27 décembre 2019, [408] [409] et une personne aux États-Unis qui est décédée de la maladie le 6 février 2020.[410]
Les tests RT-PCR d’échantillons d’eaux usées non traitées du Brésil et d’Italie ont suggéré la détection du SRAS-CoV-2 dès novembre et décembre 2019, respectivement, mais les méthodes de ces études sur les eaux usées n’ont pas été optimisées, beaucoup n’ont pas été examinées par des pairs , des détails manquent souvent et il existe un risque de faux positifs en raison d’une contamination ou si un seul gène cible est détecté. [411] Un article de revue de septembre 2020 disait : « La possibilité que l’infection au COVID‐19 se soit déjà propagée en Europe à la fin de l’année dernière est maintenant indiquée par des preuves abondantes, même partiellement circonstancielles », y compris le nombre de cas de pneumonie et radiologie en France et en Italie en novembre et décembre.[412]
Au 1er octobre 2021 [update], Reuters a indiqué qu’il avait estimé que le nombre total de décès dus au COVID‐19 dans le monde avait dépassé les cinq millions. [413]
Désinformation
Après la première épidémie de COVID‐19, la mésinformation et la désinformation concernant l’origine, l’ampleur, la prévention, le traitement et d’autres aspects de la maladie se sont rapidement propagées en ligne. [414] [415] [416]
En septembre 2020, les Centers for Disease Control and Prevention (CDC) des États-Unis ont publié des estimations préliminaires du risque de décès par tranches d’âge aux États-Unis, mais ces estimations ont été largement mal rapportées et mal comprises. [417] [418]
Autres espèces
Les humains semblent être capables de transmettre le virus à certains autres animaux, un type de transmission de maladie appelé zooanthroponose .
Certains animaux de compagnie, en particulier les chats et les furets , peuvent attraper ce virus à partir d’humains infectés. [419] [420] Les symptômes chez les chats comprennent des symptômes respiratoires (comme la toux) et digestifs. [419] Les chats peuvent transmettre le virus à d’autres chats et peuvent transmettre le virus aux humains, mais la transmission du SRAS-CoV-2 de chat à humain n’a pas été prouvée. [419] [421] Par rapport aux chats, les chiens sont moins sensibles à cette infection. [421] Les comportements qui augmentent le risque de transmission incluent embrasser, lécher et caresser l’animal. [421]
Le virus ne semble pas du tout capable d’infecter les porcs , les canards ou les poulets. [419] Les souris , les rats et les lapins, s’ils peuvent être infectés, sont peu susceptibles d’être impliqués dans la propagation du virus. [421]
Les tigres et les lions dans les zoos ont été infectés à la suite d’un contact avec des humains infectés. [421] Comme prévu, les singes et les espèces de grands singes comme les orangs- outans peuvent également être infectés par le virus COVID‐19. [421]
Les visons, qui sont de la même famille que les furets, ont été infectés. [421] Les visons peuvent être asymptomatiques et peuvent également transmettre le virus aux humains. [421] Plusieurs pays ont identifié des animaux infectés dans des élevages de visons . [422] Le Danemark , un important producteur de peaux de vison, a ordonné l’abattage de tous les visons par crainte de mutations virales, [422] à la suite d’une épidémie appelée groupe 5 . Un vaccin pour le vison et d’autres animaux est en cours de recherche. [422]
Rechercher
Des recherches internationales sur les vaccins et les médicaments contre la COVID‐19 sont en cours par des organisations gouvernementales, des groupes universitaires et des chercheurs de l’industrie. [423] [424] Le CDC l’a classé pour exiger un laboratoire de grade BSL3 . [425] Il y a eu beaucoup de recherches sur la COVID‐19, impliquant des processus de recherche accélérés et des raccourcis de publication pour répondre à la demande mondiale. [426]
En décembre 2020 [update], des centaines d’ essais cliniques ont été entrepris, avec des recherches en cours sur tous les continents sauf l’Antarctique . [427] En novembre 2020 [update], plus de 200 traitements possibles avaient jusqu’à présent été étudiés chez l’homme. [428]
Recherche sur la transmission et la prévention
Des recherches de modélisation ont été menées avec plusieurs objectifs, notamment la prédiction de la dynamique de transmission, [429] le diagnostic et le pronostic de l’infection, [430] l’estimation de l’impact des interventions, [431] [432] ou encore l’allocation des ressources. [433] Les études de modélisation sont principalement basées sur des modèles compartimentaux en épidémiologie , [434] estimant le nombre de personnes infectées au fil du temps dans des conditions données. Plusieurs autres types de modèles ont été développés et utilisés pendant la COVID‐19, notamment des modèles de dynamique des fluides computationnelle pour étudier la physique des écoulements de la COVID‐19, [435] modèles de mouvement des foules pour étudier l’exposition des occupants, [436]des modèles basés sur les données de mobilité pour étudier la transmission, [437] ou l’utilisation de modèles macroéconomiques pour évaluer l’impact économique de la pandémie. [438] En outre, des cadres conceptuels issus de la recherche sur la gestion des crises ont été appliqués pour mieux comprendre les effets de la COVID‐19 sur les organisations du monde entier. [439] [440]
Recherche liée au traitement

 Sept cibles médicamenteuses possibles dans le processus de réplication virale et les médicaments
Sept cibles médicamenteuses possibles dans le processus de réplication virale et les médicaments
Les médicaments antiviraux réutilisés constituent la majeure partie de la recherche sur les traitements de la COVID ‐19. [441] [442] D’autres candidats dans les essais comprennent les vasodilatateurs , les corticostéroïdes , les thérapies immunitaires, l’acide lipoïque , le bevacizumab et l’enzyme de conversion de l’angiotensine recombinante 2. 2. [442]
En mars 2020, l’ Organisation mondiale de la santé (OMS) a lancé l’ essai Solidarity pour évaluer les effets thérapeutiques de certains médicaments prometteurs : un médicament expérimental appelé remdesivir ; médicaments antipaludéens chloroquine et hydroxychloroquine; deux médicaments anti-VIH , le lopinavir/ritonavir ; et l’interféron-bêta . [443] [444] Plus de 300 essais cliniques actifs sont en cours en avril 2020. [165]
Les recherches sur les médicaments antipaludiques hydroxychloroquine et chloroquine ont montré qu’ils étaient au mieux inefficaces [445] [446] et qu’ils pouvaient réduire l’activité antivirale du remdesivir. [447] En mai 2020 [update], la France, l’Italie et la Belgique avaient interdit l’utilisation de l’hydroxychloroquine comme traitement contre la COVID‐19.[448]
En juin, les premiers résultats de l’essai randomisé RECOVERY au Royaume-Uni ont montré que la dexaméthasone réduisait la mortalité d’un tiers pour les personnes gravement malades sous ventilateurs et d’un cinquième pour celles recevant de l’oxygène supplémentaire. [449] Parce qu’il s’agit d’un traitement bien testé et largement disponible, il a été bien accueilli par l’OMS, qui est en train de mettre à jour les directives de traitement pour inclure la dexaméthasone et d’autres stéroïdes. [450] [451] Sur la base de ces résultats préliminaires, le traitement à la dexaméthasone a été recommandé par le NIH pour les patients atteints de COVID‐19 qui sont ventilés mécaniquement ou qui ont besoin d’oxygène supplémentaire, mais pas chez les patients atteints de COVID‐19 qui n’ont pas besoin d’oxygène supplémentaire. [452]
En septembre 2020, l’OMS a publié des directives actualisées sur l’utilisation des corticostéroïdes pour la COVID‐19. [453] [454] L’OMS recommande des corticostéroïdes systémiques plutôt que l’absence de corticostéroïdes systémiques pour le traitement des personnes atteintes de COVID‐19 grave et critique (forte recommandation, fondée sur des preuves de certitude modérée). [453] L’OMS suggère de ne pas utiliser de corticostéroïdes dans le traitement des personnes atteintes de COVID‐19 non grave (recommandation conditionnelle, fondée sur des preuves de faible certitude). [453] Les directives mises à jour étaient basées sur une méta-analyse d’essais cliniques de patients COVID-19 gravement malades. [455] [456]
En septembre 2020, l’ Agence européenne des médicaments (EMA) a approuvé l’utilisation de la dexaméthasone chez les adultes et les adolescents à partir de douze ans et pesant au moins 40 kilogrammes (88 lb) qui nécessitent une oxygénothérapie supplémentaire. [457] [458] La dexaméthasone peut être prise par voie orale ou administrée par injection ou perfusion (goutte-à-goutte) dans une veine . [457]
En novembre 2020, la Food and Drug Administration (FDA) des États-Unis a délivré une autorisation d’utilisation d’urgence pour le bamlanivimab, traitement expérimental par anticorps monoclonaux, pour le traitement de la COVID‐19 légère à modérée. [459] Le bamlanivimab est autorisé pour les personnes ayant des résultats positifs aux tests viraux directs du SRAS-CoV-2 qui sont âgées de douze ans et plus pesant au moins 40 kilogrammes (88 lb) et qui présentent un risque élevé d’évolution vers une forme grave de COVID- 19 ou hospitalisation. [459] Cela comprend les personnes âgées de 65 ans ou plus ou qui souffrent de maladies chroniques. [459]
En février 2021, la FDA a délivré une autorisation d’utilisation d’urgence (EUA) pour le bamlanivimab et l’étésevimab administrés ensemble pour le traitement du COVID‐19 léger à modéré chez les personnes de douze ans ou plus pesant au moins 40 kilogrammes (88 lb) dont le test est positif pour le SRAS‐CoV‐2 et qui présentent un risque élevé d’évolution vers une forme grave de COVID‐19. L’utilisation autorisée comprend le traitement des personnes âgées de 65 ans ou plus ou souffrant de certaines maladies chroniques.[460]
En avril 2021, la FDA a révoqué l’autorisation d’utilisation d’urgence (EUA) qui autorisait l’utilisation de la thérapie par anticorps monoclonaux bamlanivimab, lorsqu’elle est administrée seule, pour le traitement de la COVID‐19 légère à modérée chez les adultes et certains patients pédiatriques. [461]
Tempête de cytokines 
 Diverses stratégies thérapeutiques pour cibler la tempête de cytokines
Diverses stratégies thérapeutiques pour cibler la tempête de cytokines
Une tempête de cytokines peut être une complication dans les derniers stades de la COVID-19 sévère. Une tempête de cytokines est une réaction immunitaire potentiellement mortelle dans laquelle une grande quantité de cytokines et de chimiokines pro-inflammatoires est libérée trop rapidement. Une tempête de cytokines peut entraîner un SDRA et une défaillance multiviscérale. [462] Les données recueillies à l’hôpital Jin Yin-tan de Wuhan, en Chine, indiquent que les patients qui ont eu des réponses plus sévères à la COVID‐19 avaient de plus grandes quantités de cytokines et de chimiokines pro-inflammatoires dans leur système que les patients qui avaient des réponses plus douces. Ces niveaux élevés de cytokines et de chimiokines pro-inflammatoires indiquent la présence d’une tempête de cytokines.[463]
Le tocilizumab a été inclus dans les directives de traitement par la Commission nationale chinoise de la santé après la fin d’une petite étude. [464] [465] Il fait l’objet d’un essai non randomisé de phase II au niveau national en Italie après avoir montré des résultats positifs chez des personnes atteintes d’une maladie grave. [466] [467] Combiné avec un test sanguin de ferritine sérique pour identifier une tempête de cytokines (également appelée syndrome de tempête de cytokines, à ne pas confondre avec le syndrome de libération de cytokines), il est destiné à contrer de tels développements, qui seraient la cause de décès chez certaines personnes touchées. [468] Le récepteur de l’ interleukine-6 (IL-6R) antagonistea été approuvé par la FDA pour subir un essai clinique de phase III évaluant son efficacité sur le COVID-19 sur la base d’études de cas rétrospectives pour le traitement du syndrome de libération de cytokines réfractaire aux stéroïdes induit par une cause différente, la thérapie cellulaire CAR T , en 2017. [469 ] Il n’y a aucune preuve randomisée et contrôlée que le tocilizumab est un traitement efficace pour le SRC. Il a été démontré que le tocilizumab prophylactique augmente les taux sériques d’IL-6 en saturant l’IL-6R, en faisant passer l’IL-6 à travers la barrière hémato-encéphalique et en exacerbant la neurotoxicité sans avoir d’effet sur l’incidence du SRC. [470]
Le lenzilumab , un anticorps monoclonal anti-GM-CSF , est protecteur dans les modèles murins du SRC induit par les cellules CAR T et de la neurotoxicité et constitue une option thérapeutique viable en raison de l’augmentation observée des cellules T pathogènes sécrétant du GM-CSF chez les patients hospitalisés atteints de COVID- 19. [471]
Anticorps passifs 
 Vue d’ensemble de l’application et de l’utilisation de la plasmathérapie convalescente
Vue d’ensemble de l’application et de l’utilisation de la plasmathérapie convalescente
Le transfert d’ anticorps purifiés et concentrés produits par le système immunitaire de ceux qui se sont remis de la COVID‐19 à des personnes qui en ont besoin est à l’étude en tant que méthode non vaccinale d’ immunisation passive . [472] [473] La neutralisation virale est le mécanisme d’action prévu par lequel la thérapie passive par anticorps peut assurer la défense contre le SRAS-CoV-2. La protéine de pointe du SRAS-CoV-2 est la principale cible des anticorps neutralisants. [474] Au 8 août 2020, huit anticorps neutralisants ciblant la protéine de pointe du SRAS-CoV-2 sont entrés dans les études cliniques. [475]Il a été proposé que la sélection d’anticorps neutralisants larges contre le SRAS-CoV-2 et le SRAS-CoV pourrait être utile pour traiter non seulement le COVID-19, mais également les futures infections à CoV liées au SRAS. [474][472]Cependant, d’autres mécanismes, tels que la cytotoxicité cellulaire ou la phagocytose dépendante des anticorps , peuvent être possibles. [472] D’autres formes de thérapie passive par anticorps, par exemple l’utilisation d’anticorps monoclonaux fabriqués, sont en cours de développement.
L’utilisation d’anticorps passifs pour traiter les personnes atteintes de COVID-19 actif est également à l’étude. Cela implique la production de sérum de convalescence , qui consiste en la partie liquide du sang des personnes qui se sont remises de l’infection et contient des anticorps spécifiques à ce virus, qui est ensuite administré aux patients actifs. [472] Cette stratégie a été essayée pour le SRAS avec des résultats non concluants. [472] Une revue Cochrane mise à jour en mai 2021 a trouvé des preuves de haute certitude que, pour le traitement des personnes atteintes de COVID-19 modéré à sévère, le plasma convalescent ne réduisait pas la mortalité ni n’apportait d’amélioration des symptômes. [473]L’innocuité de l’administration de plasma convalescent aux personnes atteintes de COVID-19 continue d’être incertaine et les résultats différents mesurés dans différentes études limitent leur utilisation pour déterminer l’efficacité. [473]
Bioéthique
Depuis le déclenchement de la pandémie de COVID‐19, les chercheurs ont exploré la bioéthique , l’économie normative et les théories politiques des politiques de santé liées à la crise de santé publique. [476] Les universitaires ont souligné la détresse morale des travailleurs de la santé, l’éthique de la distribution de ressources de santé rares telles que les ventilateurs, [477] et la justice mondiale des diplomaties vaccinales. [ citation nécessaire ] Les inégalités socio-économiques entre les genres, [478] races, [479] groupes handicapés, [480] communautés, [481] régions, pays,[482] et les continents ont également attiré l’attention du milieu universitaire et du grand public.
Effet sur d’autres maladies et le commerce de la pharmacie
Il y a eu un rapport [483] le 3 mars 2021, selon lequel la distanciation sociale et le port courant de masques chirurgicaux et similaires comme précaution courante contre le COVID‐19 ont provoqué une baisse du taux de propagation du rhume et de la grippe .
Voir également
- Les maladies à coronavirus , un groupe de syndromes étroitement liés
- Maladie X , un terme de l’OMS
- Loi de la virulence déclinante – Revendication de l’épidémiologiste Theobald Smith
- Théorie de la virulence – Théorie du biologiste Paul W. Ewald
Références
- ^ “Covid-19” . Dictionnaire anglais Oxford (éd. En ligne). Presse universitaire d’Oxford . avril 2020 . Récupéré le 15 avril 2020 . (Abonnement ou adhésion à une institution participante requise.)
- ^ “Symptômes du coronavirus” . Centres américains de contrôle et de prévention des maladies (CDC) . 13 mai 2020. Archivé de l’original le 17 juin 2020 . Récupéré le 18 juin 2020 .
- ^ “Q&R sur les coronavirus (COVID-19)” . Organisation mondiale de la santé (OMS). 17 avril 2020. Archivé de l’original le 14 mai 2020 . Récupéré le 14 mai 2020 .
- ^ Talic, S; Shah, S; Sauvage, H; Gasevic, D; Maharaj, A ; Ademi, Z; Li, X; Xu, W; Mesa-Eguiagaray, I; Rostron, J; Théodoratou, E (17 novembre 2021). “Efficacité des mesures de santé publique pour réduire l’incidence de la transmission du covid-19, du SRAS-CoV-2 et de la mortalité du covid-19 : examen systématique et méta-analyse”. BMJ (Clinical Research Ed.) . 375 : e068302. doi : 10.1136/bmj-2021-068302 (inactif le 25 mars 2022). ISSN 1756-1833 . PMID 34789505 . {{cite journal}}: CS1 maint: DOI inactive as of March 2022 (link)
- ^ “Vaccins COVID-19” . Organisation mondiale de la santé (OMS) . Récupéré le 3 mars 2021 .
- ^ un bc “Le tableau de bord COVID -19 par le Centre pour la Science et l’Ingénierie des Systèmes (CSSE) à l’Université Johns Hopkins (JHU)” . ArcGIS . Université John Hopkins . Récupéré le 16 mai 2022 .
- ^ Page J, Hinshaw D, McKay B (26 février 2021). “Dans Hunt for Covid-19 Origin, Patient Zero Points to Second Wuhan Market – L’homme avec la première infection confirmée du nouveau coronavirus a déclaré à l’équipe de l’OMS que ses parents y avaient fait leurs courses” . Le Wall StreetJournal . Récupéré le 27 février 2021 .
- ^ Zimmer C (26 février 2021). “La vie secrète d’un coronavirus – Une bulle de gènes huileuse de 100 nanomètres de large a tué plus de deux millions de personnes et remodelé le monde. Les scientifiques ne savent pas trop quoi en penser” . Le New York Times . ISSN 0362-4331 . Archivé de l’original le 28 décembre 2021 . Récupéré le 28 février 2021 .
- ^ Islam MA (avril 2021). “Prévalence et caractéristiques de la fièvre chez les patients adultes et pédiatriques atteints de la maladie à coronavirus 2019 (COVID-19) : Une revue systématique et une méta-analyse de 17515 patients” . PLOS ONE . 16 (4) : e0249788. Bibcode : 2021PLoSO..1649788I . doi : 10.1371/journal.pone.0249788 . PMC 8023501 . PMID 33822812 .
- ^ Islam MA (novembre 2020). “Prévalence des maux de tête chez les patients atteints de la maladie à coronavirus 2019 (COVID-19) : examen systématique et méta-analyse de 14 275 patients” . Frontières en Neurologie . 11 : 562634. doi : 10.3389/fneur.2020.562634 . PMC 7728918 . PMID 33329305 .
- ^ Saniasiaya J, Islam MA (avril 2021). “Prévalence du dysfonctionnement olfactif dans la maladie à coronavirus 2019 (COVID-19) : une méta-analyse de 27 492 patients” . Le Laryngoscope . 131 (4): 865–878. doi : 10.1002/lary.29286 . ISSN 0023-852X . PMC 7753439 . PMID 33219539 .
- ^ Saniasiaya J, Islam MA (novembre 2020). « Prévalence et caractéristiques des troubles du goût dans les cas de COVID-19 : une méta-analyse de 29 349 patients ». Oto-rhino-laryngologie – Chirurgie cervico-faciale . 165 (1): 33–42. doi : 10.1177/0194599820981018 . PMID 33320033 . S2CID 229174644 .
- ^ Agyeman AA, Chin KL, Landersdorfer CB, Liew D, Ofori-Asenso R (août 2020). “Dysfonctionnement de l’odorat et du goût chez les patients atteints de COVID-19 : une revue systématique et une méta-analyse” . Mayo Clin. Proc . 95 (8): 1621-1631. doi : 10.1016/j.mayocp.2020.05.030 . PMC 7275152 . PMID 32753137 .
- ^ Oran DP, Topol EJ (janvier 2021). “La proportion d’infections par le SRAS-CoV-2 asymptomatiques : un examen systématique” . Annales de médecine interne . 174 (5) : M20-6976. doi : 10.7326/M20-6976 . PMC 7839426 . PMID 33481642 .
- ^ “Conseils cliniques provisoires pour la gestion des patients atteints d’une maladie à coronavirus confirmée (COVID-19)” . Centres américains de contrôle et de prévention des maladies (CDC) . 6 avril 2020. Archivé de l’original le 2 mars 2020 . Récupéré le 19 avril 2020 .
- ^ un b CDC (11 février 2020). “Conditions post-COVID” . Centres américains de contrôle et de prévention des maladies (CDC) . Récupéré le 12 juillet 2021 .
- ^ CDC (11 février 2020). “Maladie à coronavirus 2019 (COVID-19)” . Centres américains de contrôle et de prévention des maladies (CDC) . Récupéré le 6 décembre 2020 .
- ^ “Questions cliniques sur COVID-19 : Questions et réponses” . Centres américains de contrôle et de prévention des maladies (CDC) . 17 novembre 2021 . Récupéré le 25 janvier 2022 .
- ^ “2ème cas américain de coronavirus de Wuhan confirmé” . NPR.org . NPR . Récupéré le 4 avril 2020 .
- ^ McNeil Jr DG (2 février 2020). “Le coronavirus de Wuhan ressemble de plus en plus à une pandémie, disent les experts” . Le New York Times . ISSN 0362-4331 . Archivé de l’original le 2 février 2020 . Récupéré le 4 avril 2020 .
- ^ Griffiths J. “Les décès dus au coronavirus de Wuhan augmentent à nouveau alors que l’épidémie ne montre aucun signe de ralentissement” . CNN . Récupéré le 4 avril 2020 .
- ^ Jiang S, Xia S, Ying T, Lu L (mai 2020). “Un nouveau coronavirus (2019-nCoV) provoquant un syndrome respiratoire associé à la pneumonie” . Immunologie cellulaire et moléculaire . 17 (5): 554. doi : 10.1038/s41423-020-0372-4 . PMC 7091741 . PMID 32024976 .
- ^ Chan JF, Yuan S, Kok KH, To KK, Chu H, Yang J, et al. (février 2020). “Un cluster familial de pneumonie associé au nouveau coronavirus 2019 indiquant une transmission de personne à personne : une étude d’un cluster familial” . Lancette . 395 (10223): 514-523. doi : 10.1016/S0140-6736(20)30154-9 . PMC 7159286 . PMID 31986261 .
- ^ Shablovsky S (septembre 2017). “L’héritage de la grippe espagnole” . Sciences . 357 (6357): 1245. Bibcode : 2017Sci…357.1245S . doi : 10.1126/science.aao4093 . ISSN 0036-8075 . S2CID 44116811 .
- ^ “Arrêtez la stigmatisation du coronavirus maintenant” . Nature . 7 avril 2020. p. 165. doi : 10.1038/d41586-020-01009-0 . Récupéré le 16 avril 2020 .
- ^ “Rapport de situation sur le nouveau coronavirus (2019-nCoV) – 1” (PDF) . Organisation mondiale de la santé (OMS) . 21 janvier 2020.
- ^ “Rapport de situation sur le nouveau coronavirus (2019-nCoV) – 10” (PDF) . Organisation mondiale de la santé (OMS) . 30 janvier 2020.
- ^ “Nouveau coronavirus nommé” Covid-19 “: QUI” . Aujourd’hui . Singapour. Archivé de l’original le 21 mars 2020 . Récupéré le 11 février 2020 .
- ^ “Le coronavirus propage le racisme contre – et parmi – les Chinois de souche” . L’Économiste . 17 février 2020. Archivé de l’original le 17 février 2020 . Récupéré le 17 février 2020 .
- ^ Meilleures pratiques de l’Organisation mondiale de la santé pour la dénomination des nouvelles maladies infectieuses humaines (PDF) (Rapport). Organisation mondiale de la santé (OMS). Mai 2015. hdl : 10665/163636 .
- ^ un b “Nommer la maladie à coronavirus (COVID-19) et le virus qui la cause” . Organisation mondiale de la santé (OMS) . Archivé de l’original le 28 février 2020 . Récupéré le 13 mars 2020 .
- ^ Maladie à coronavirus 2019 (COVID-19) dans l’UE/EEE et au Royaume-Uni – huitième mise à jour (PDF) (Rapport). ECDC. Archivé (PDF) de l’original le 14 mars 2020 . Récupéré le 19 avril 2020 .
- ^ Gover AR, Harper SB, Langton L (juillet 2020). “Crime de haine anti-asiatique pendant la pandémie de COVID-19 : Exploration de la reproduction des inégalités” . Journal américain de justice pénale . 45 (4): 647–667. doi : 10.1007/s12103-020-09545-1 . PMC 7364747 . PMID 32837171 .
- ^ “Symptômes du coronavirus” . Centres américains de contrôle et de prévention des maladies de contrôle et de prévention des maladies (CDC) . 22 février 2021. Archivé de l’original le 4 mars 2021 . Récupéré le 4 mars 2021 .
- ^ Grant MC, Geoghegan L, Arbyn M, Mohammed Z, McGuinness L, Clarke EL, Wade RG (23 juin 2020). “La prévalence des symptômes chez 24 410 adultes infectés par le nouveau coronavirus (SRAS-CoV-2 ; COVID-19) : une revue systématique et une méta-analyse de 148 études de 9 pays” . PLOS ONE . 15 (6) : e0234765. Bibcode : 2020PLoSO..1534765G . doi : 10.1371/journal.pone.0234765 . PMC 7310678 . PMID 32574165 . S2CID 220046286 .
- ^ Pardhan, Shahina; Vaughan, Megan; Zhang, Jufen; Smith, Lee; Chichger, Havovi (1er novembre 2020). “Les yeux endoloris comme symptôme oculaire le plus important ressenti par les personnes atteintes de COVID-19 : une comparaison entre les états pré-COVID-19 et pendant les états COVID-19” . Ophtalmologie ouverte BMJ . 5 (1) : e000632. doi : 10.1136/bmjophth-2020-000632 . ISSN 2397-3269 . PMID 32253246 .
- ^ “Orteils COVID, éruptions cutanées : comment le coronavirus peut affecter votre peau” . www.aad.org . Récupéré le 20 mars 2022 .
- ^ un b “Les caractéristiques cliniques de COVID-19” . Centre européen de prévention et de contrôle des maladies . Récupéré le 29 décembre 2020 .
- ^ Paderno A, Mattavelli D, Rampinelli V, Grammatica A, Raffetti E, Tomasoni M, et al. (Décembre 2020). “Résultats olfactifs et gustatifs dans COVID-19 : une évaluation prospective chez des sujets non hospitalisés” . Oto-rhino-laryngologie – Chirurgie cervico-faciale . 163 (6): 1144–1149. doi : 10.1177/0194599820939538 . PMC 7331108 . PMID 32600175 .
- ^ Chabot AB, Huntwork MP (September 2021). “Turmeric as a Possible Treatment for COVID-19-Induced Anosmia and Ageusia”. Cureus. 13 (9): e17829. doi:10.7759/cureus.17829. PMC 8502749. PMID 34660038.
- ^ Niazkar HR, Zibaee B, Nasimi A, Bahri N (July 2020). “The neurological manifestations of COVID-19: a review article”. Neurological Sciences. 41 (7): 1667–1671. doi:10.1007/s10072-020-04486-3. PMC 7262683. PMID 32483687.
- ^ “Interim Clinical Guidance for Management of Patients with Confirmed Coronavirus Disease (COVID-19)”. U.S. Centers for Disease Control and Prevention (CDC). 6 April 2020. Archived from the original on 2 March 2020. Retrieved 19 April 2020.
- ^ Multiple sources:
- Oran DP, Topol EJ (January 2021). “The Proportion of SARS-CoV-2 Infections That Are Asymptomatic : A Systematic Review”. Annals of Internal Medicine. 174 (5): 655–662. doi:10.7326/M20-6976. PMC 7839426. PMID 33481642.
- “Transmission of COVID-19”. European Centre for Disease Prevention and Control. Retrieved 6 December 2020.
- Nogrady B (November 2020). “What the data say about asymptomatic COVID infections”. Nature. 587 (7835): 534–535. Bibcode:2020Natur.587..534N. doi:10.1038/d41586-020-03141-3. PMID 33214725.
- ^ a b Gao Z, Xu Y, Sun C, Wang X, Guo Y, Qiu S, Ma K (February 2021). “A systematic review of asymptomatic infections with COVID-19”. Journal of Microbiology, Immunology, and Infection = Wei Mian Yu Gan Ran Za Zhi. 54 (1): 12–16. doi:10.1016/j.jmii.2020.05.001. ISSN 1684-1182. PMC 7227597. PMID 32425996.
- ^ Oran, Daniel P., and Eric J. Topol. “Prevalence of Asymptomatic SARS-CoV-2 Infection : A Narrative Review.” Annals of Internal Medicine. vol. 173,5 (2020): 362-367. doi:10.7326/M20-3012 PMID 32491919 Retrieved 14 January 2021.
- ^ Lai CC, Liu YH, Wang CY, Wang YH, Hsueh SC, Yen MY, et al. (June 2020). “Asymptomatic carrier state, acute respiratory disease, and pneumonia due to severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2): Facts and myths”. Journal of Microbiology, Immunology, and Infection = Wei Mian Yu Gan Ran Za Zhi. 53 (3): 404–412. doi:10.1016/j.jmii.2020.02.012. PMC 7128959. PMID 32173241.
- ^ a b Furukawa NW, Brooks JT, Sobel J (July 2020). “Evidence Supporting Transmission of Severe Acute Respiratory Syndrome Coronavirus 2 While Presymptomatic or Asymptomatic”. Emerging Infectious Diseases. 26 (7). doi:10.3201/eid2607.201595. PMC 7323549. PMID 32364890.
- ^ a b Gandhi RT, Lynch JB, Del Rio C (October 2020). “Mild or Moderate Covid-19”. The New England Journal of Medicine. 383 (18): 1757–1766. doi:10.1056/NEJMcp2009249. PMID 32329974.
- ^ Byrne, Andrew William; McEvoy, David; Collins, Aine B.; Hunt, Kevin; Casey, Miriam; Barber, Ann; Butler, Francis; Griffin, John; Lane, Elizabeth A.; McAloon, Conor; O’Brien, Kirsty (1 August 2020). “Inferred duration of infectious period of SARS-CoV-2: rapid scoping review and analysis of available evidence for asymptomatic and symptomatic COVID-19 cases”. BMJ Open. 10 (8): e039856. doi:10.1136/bmjopen-2020-039856. ISSN 2044-6055. PMID 32759252.
- ^ Wiersinga WJ, Rhodes A, Cheng AC, Peacock SJ, Prescott HC (August 2020). “Pathophysiology, Transmission, Diagnosis, and Treatment of Coronavirus Disease 2019 (COVID-19): A Review”. JAMA. 324 (8): 782–793. doi:10.1001/jama.2020.12839. PMID 32648899. S2CID 220465311.
- ^ “Half of young adults with COVID-19 have persistent symptoms after 6 months”. medicalxpress.com. Retrieved 10 July 2021.
- ^ Blomberg B, Mohn KG, Brokstad KA, Zhou F, Linchausen DW, Hansen BA, et al. (June 2021). “Long COVID in a prospective cohort of home-isolated patients”. Nature Medicine. 27 (9): 1607–1613. doi:10.1038/s41591-021-01433-3. PMC 8440190. PMID 34163090. S2CID 235625772.
- ^ CDC (11 February 2020). “COVID-19 and Your Health”. Centers for Disease Control and Prevention. Retrieved 23 January 2021.
- ^ Hu B, Guo H, Zhou P, Shi ZL (March 2021). “Characteristics of SARS-CoV-2 and COVID-19″. Nature Reviews. Microbiology. 19 (3): 141–154. doi:10.1038/s41579-020-00459-7. PMC 7537588. PMID 33024307.
- ^ a b Wang CC, Prather KA, Sznitman J, Jimenez JL, Lakdawala SS, Tufekci Z, Marr LC (August 2021). “Airborne transmission of respiratory viruses”. Science. 373 (6558). Bibcode:2021Sci…373…..W. doi:10.1126/science.abd9149. PMID 34446582.
- ^ Greenhalgh T, Jimenez JL, Prather KA, Tufekci Z, Fisman D, Schooley R (May 2021). “Ten scientific reasons in support of airborne transmission of SARS-CoV-2“. Lancet. 397 (10285): 1603–1605. doi:10.1016/s0140-6736(21)00869-2. PMC 8049599. PMID 33865497.
- ^ Bourouiba L (13 July 2021). “Fluid Dynamics of Respiratory Infectious Diseases”. Annual Review of Biomedical Engineering. 23 (1): 547–577. doi:10.1146/annurev-bioeng-111820-025044. hdl:1721.1/131115. PMID 34255991. S2CID 235823756. Retrieved 7 September 2021.
- ^ Stadnytskyi, Valentyn; Bax, Christina E.; Bax, Adriaan; Anfinrud, Philip (2 June 2020). “The airborne lifetime of small speech droplets and their potential importance in SARS-CoV-2 transmission”. Proceedings of the National Academy of Sciences. 117 (22): 11875–11877. doi:10.1073/pnas.2006874117. PMC 7275719. PMID 32404416.
- ^ Miller SL, Nazaroff WW, Jimenez JL, Boerstra A, Buonanno G, Dancer SJ, et al. (March 2021). “Transmission of SARS-CoV-2 by inhalation of respiratory aerosol in the Skagit Valley Chorale superspreading event”. Indoor Air. 31 (2): 314–323. doi:10.1111/ina.12751. PMC 7537089. PMID 32979298.
- ^ He, Xi; Lau, Eric H. Y.; Wu, Peng; Deng, Xilong; Wang, Jian; Hao, Xinxin; Lau, Yiu Chung; Wong, Jessica Y.; Guan, Yujuan; Tan, Xinghua; Mo, Xiaoneng; Chen, Yanqing; Liao, Baolin; Chen, Weilie; Hu, Fengyu; Zhang, Qing; Zhong, Mingqiu; Wu, Yanrong; Zhao, Lingzhai; Zhang, Fuchun; Cowling, Benjamin J.; Li, Fang; Leung, Gabriel M. (September 2020). “Author Correction: Temporal dynamics in viral shedding and transmissibility of COVID-19”. Nature Medicine. 26 (9): 1491–1493. doi:10.1038/s41591-020-1016-z.
- ^ a b c d Communicable Diseases Network Australia. “Coronavirus Disease 2019 (COVID-19): CDNA National Guidelines for Public Health Units”. 5.1. Communicable Diseases Network Australia/Australian Government Department of Health.
- ^ “Clinical Questions about COVID-19: Questions and Answers”. Centers for Disease Control and Prevention. 4 March 2021.
- ^ “Scientific Brief: SARS-CoV-2 Transmission”. Centers for Disease Control and Prevention. 7 May 2021. Retrieved 8 May 2021.
- ^ “Coronavirus disease (COVID-19): How is it transmitted?”. World Health Organization. 30 April 2021.
- ^ a b c d e • “COVID-19: epidemiology, virology and clinical features”. GOV.UK. Retrieved 18 October 2020.
• Communicable Diseases Network Australia. “Coronavirus Disease 2019 (COVID-19) – CDNA Guidelines for Public Health Units”. Version 4.4. Australian Government Department of Health. Retrieved 17 May 2021.{{cite web}}: CS1 maint: url-status (link)
• Public Health Agency of Canada (3 November 2020). “COVID-19: Main modes of transmission”. aem. Retrieved 18 May 2021.
• “Transmission of COVID-19”. European Centre for Disease Prevention and Control. Retrieved 18 May 2021.
• Meyerowitz EA, Richterman A, Gandhi RT, Sax PE (January 2021). “Transmission of SARS-CoV-2: A Review of Viral, Host, and Environmental Factors”. Annals of Internal Medicine. 174 (1): 69–79. doi:10.7326/M20-5008. ISSN 0003-4819. PMC 7505025. PMID 32941052. - ^ a b c Tang JW, Marr LC, Li Y, Dancer SJ (April 2021). “Covid-19 has redefined airborne transmission”. BMJ. 373: n913. doi:10.1136/bmj.n913. PMID 33853842.
- ^ a b Morawska L, Allen J, Bahnfleth W, Bluyssen PM, Boerstra A, Buonanno G, et al. (May 2021). “A paradigm shift to combat indoor respiratory infection” (PDF). Science. 372 (6543): 689–691. Bibcode:2021Sci…372..689M. doi:10.1126/science.abg2025. PMID 33986171. S2CID 234487289.
- ^ a b Meyerowitz EA, Richterman A, Gandhi RT, Sax PE (January 2021). “Transmission of SARS-CoV-2: A Review of Viral, Host, and Environmental Factors”. Annals of Internal Medicine. 174 (1): 69–79. doi:10.7326/M20-5008. ISSN 0003-4819. PMC 7505025. PMID 32941052.
- ^ CDC (11 February 2020). “Healthcare Workers”. Centers for Disease Control and Prevention. Retrieved 29 March 2022.
- ^ Liu T, Gong D, Xiao J, Hu J, He G, Rong Z, Ma W (October 2020). “Cluster infections play important roles in the rapid evolution of COVID-19 transmission: A systematic review”. International Journal of Infectious Diseases. 99: 374–380. doi:10.1016/j.ijid.2020.07.073. PMC 7405860. PMID 32768702.
- ^ “Outbreak of severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2): increased transmission beyond China – fourth update” (PDF). European Centre for Disease Prevention and Control. 14 February 2020. Retrieved 8 March 2020.
- ^ a b Andersen KG, Rambaut A, Lipkin WI, Holmes EC, Garry RF (April 2020). “The proximal origin of SARS-CoV-2“. Nature Medicine. 26 (4): 450–452. doi:10.1038/s41591-020-0820-9. PMC 7095063. PMID 32284615.
- ^ Gibbens S (18 March 2020). “Why soap is preferable to bleach in the fight against coronavirus”. National Geographic. Archived from the original on 2 April 2020. Retrieved 2 April 2020.
- ^ Zhu N, Zhang D, Wang W, Li X, Yang B, Song J, et al. (February 2020). “A Novel Coronavirus from Patients with Pneumonia in China, 2019”. The New England Journal of Medicine. 382 (8): 727–733. doi:10.1056/NEJMoa2001017. PMC 7092803. PMID 31978945.
- ^ a b c Report of the WHO-China Joint Mission on Coronavirus Disease 2019 (COVID-19) (PDF) (Report). World Health Organization (WHO). February 2020. Archived (PDF) from the original on 29 February 2020. Retrieved 21 March 2020.
- ^ “Report of the WHO-China Joint Mission on Coronavirus Disease 2019 (COVID-19)”. World Health Organization (WHO). Retrieved 25 January 2022.
- ^ Rathore JS, Ghosh C (August 2020). “Severe acute respiratory syndrome coronavirus-2 (SARS-CoV-2), a newly emerged pathogen: an overview”. Pathogens and Disease. 78 (6). doi:10.1093/femspd/ftaa042. OCLC 823140442. PMC 7499575. PMID 32840560.
- ^ Thomas S (19 October 2020). “The Structure of the Membrane Protein of SARS-CoV-2 Resembles the Sugar Transporter SemiSWEET”. Pathogens & Immunity. 5 (1): 342–363. doi:10.20411/pai.v5i1.377. PMC 7608487. PMID 33154981.
- ^ Koyama T, Platt D, Parida L (July 2020). “Variant analysis of SARS-CoV-2 genomes”. Bulletin of the World Health Organization. 98 (7): 495–504. doi:10.2471/BLT.20.253591. PMC 7375210. PMID 32742035. We detected in total 65776 variants with 5775 distinct variants.
- ^ a b Rambaut A, Holmes EC, O’Toole Á, Hill V, McCrone JT, Ruis C, et al. (November 2020). “A dynamic nomenclature proposal for SARS-CoV-2 lineages to assist genomic epidemiology”. Nature Microbiology. 5 (11): 1403–1407. doi:10.1038/s41564-020-0770-5. PMC 7610519. PMID 32669681.
- ^ “Tracking SARS-CoV-2 variants”. World Health Organization. 1 July 2021. Retrieved 5 July 2021.
- ^ Alm E, Broberg EK, Connor T, Hodcroft EB, Komissarov AB, Maurer-Stroh S, et al. (August 2020). “Geographical and temporal distribution of SARS-CoV-2 clades in the WHO European Region, January to June 2020″. Euro Surveillance. 25 (32). doi:10.2807/1560-7917.ES.2020.25.32.2001410. PMC 7427299. PMID 32794443.
- ^ “PANGO lineages”. cov-lineages.org. Archived from the original on 10 May 2021. Retrieved 9 May 2021.
- ^ Lauring AS, Hodcroft EB (February 2021). “Genetic Variants of SARS-CoV-2-What Do They Mean?”. JAMA. 325 (6): 529–531. doi:10.1001/jama.2020.27124. PMID 33404586. S2CID 230783233. Retrieved 22 October 2021.
- ^ Abdool Karim SS, de Oliveira T (May 2021). “New SARS-CoV-2 Variants – Clinical, Public Health, and Vaccine Implications”. The New England Journal of Medicine. Massachusetts Medical Society. 384 (19): 1866–1868. doi:10.1056/nejmc2100362. ISSN 0028-4793. PMC 8008749. PMID 33761203.
- ^ Mallapaty S (November 2020). “COVID mink analysis shows mutations are not dangerous – yet”. Nature. 587 (7834): 340–341. Bibcode:2020Natur.587..340M. doi:10.1038/d41586-020-03218-z. PMID 33188367. S2CID 226947606.
- ^ Larsen HD, Fonager J, Lomholt FK, Dalby T, Benedetti G, Kristensen B, et al. (February 2021). “Preliminary report of an outbreak of SARS-CoV-2 in mink and mink farmers associated with community spread, Denmark, June to November 2020″. Euro Surveillance. 26 (5): 2100009. doi:10.2807/1560-7917.ES.2021.26.5.210009. PMC 7863232. PMID 33541485. As at 1 February 2021, we assess that the cluster 5 variant is no longer circulating among humans in Denmark.
- ^ “New COVID-19 Variants”. U.S. Centers for Disease Control and Prevention (CDC). 28 June 2021 [First published 11 February 2020]. Retrieved 15 July 2021.
- ^ “COVID-19 Weekly Epidemiological Update Edition 69”. World Health Organization (WHO). 7 December 2021.
- ^ “Classification of Omicron (B.1.1.529): SARS-CoV-2 Variant of Concern”. World Health Organization (WHO). Retrieved 9 December 2021.
- ^ Harrison AG, Lin T, Wang P (December 2020). “Mechanisms of SARS-CoV-2 Transmission and Pathogenesis”. Trends in Immunology. 41 (12): 1100–1115. doi:10.1016/j.it.2020.10.004. PMC 7556779. PMID 33132005.
- ^ Verdecchia P, Cavallini C, Spanevello A, Angeli F (June 2020). “The pivotal link between ACE2 deficiency and SARS-CoV-2 infection”. European Journal of Internal Medicine. 76: 14–20. doi:10.1016/j.ejim.2020.04.037. PMC 7167588. PMID 32336612.
- ^ Letko M, Marzi A, Munster V (April 2020). “Functional assessment of cell entry and receptor usage for SARS-CoV-2 and other lineage B betacoronaviruses”. Nature Microbiology. 5 (4): 562–569. doi:10.1038/s41564-020-0688-y. PMC 7095430. PMID 32094589.
- ^ Marik PE, Iglesias J, Varon J, Kory P (1 January 2021). “A scoping review of the pathophysiology of COVID-19”. International Journal of Immunopathology and Pharmacology. 35: 20587384211048026. doi:10.1177/20587384211048026. PMC 8477699. PMID 34569339.
- ^ a b Meunier N, Briand L, Jacquin-Piques A, Brondel L, Pénicaud L (June 2020). “COVID 19-Induced Smell and Taste Impairments: Putative Impact on Physiology”. Frontiers in Physiology. 11: 625110. doi:10.3389/fphys.2020.625110. PMC 7870487. PMID 33574768.
- ^ Juan IG, et al. (2021). “Central and peripheral nervous system involvement by COVID-19: a systematic review of the pathophysiology, clinical manifestations, neuropathology, neuroimaging, electrophysiology, and cerebrospinal fluid findings”. BMC Infectious Diseases. 21 (1): 515. doi:10.1186/s12879-021-06185-6. PMC 8170436. PMID 34078305.
- ^ a b Pezzini A, Padovani A (November 2020). “Lifting the mask on neurological manifestations of COVID-19”. Nature Reviews. Neurology. 16 (11): 636–644. doi:10.1038/s41582-020-0398-3. PMC 7444680. PMID 32839585.
- ^ Li YC, Bai WZ, Hashikawa T (June 2020). “The neuroinvasive potential of SARS-CoV2 may play a role in the respiratory failure of COVID-19 patients”. Journal of Medical Virology. 92 (6): 552–555. doi:10.1002/jmv.25728. PMC 7228394. PMID 32104915.
- ^ Baig AM, Khaleeq A, Ali U, Syeda H (April 2020). “Evidence of the COVID-19 Virus Targeting the CNS: Tissue Distribution, Host-Virus Interaction, and Proposed Neurotropic Mechanisms”. ACS Chemical Neuroscience. 11 (7): 995–998. doi:10.1021/acschemneuro.0c00122. PMC 7094171. PMID 32167747.
- ^ Yavarpour-Bali H, Ghasemi-Kasman M (September 2020). “Update on neurological manifestations of COVID-19”. Life Sciences. 257: 118063. doi:10.1016/j.lfs.2020.118063. PMC 7346808. PMID 32652139.
- ^ Covid can shrink brain and damage its tissue, finds research The Guardian
- ^ Scans reveal how Covid may change the brain BBC
- ^ “Even mild Covid is linked to brain damage months after illness, scans show”. NBC News.
- ^ Gu J, Han B, Wang J (May 2020). “COVID-19: Gastrointestinal Manifestations and Potential Fecal-Oral Transmission”. Gastroenterology. 158 (6): 1518–1519. doi:10.1053/j.gastro.2020.02.054. PMC 7130192. PMID 32142785.
- ^ Mönkemüller K, Fry L, Rickes S (May 2020). “COVID-19, coronavirus, SARS-CoV-2 and the small bowel”. Revista Espanola de Enfermedades Digestivas. 112 (5): 383–388. doi:10.17235/reed.2020.7137/2020. PMID 32343593. S2CID 216645754.
- ^ a b c Zheng YY, Ma YT, Zhang JY, Xie X (May 2020). “COVID-19 and the cardiovascular system”. Nature Reviews. Cardiology. 17 (5): 259–260. doi:10.1038/s41569-020-0360-5. PMC 7095524. PMID 32139904.
- ^ a b c Huang C, Wang Y, Li X, Ren L, Zhao J, Hu Y, et al. (February 2020). “Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China”. Lancet. 395 (10223): 497–506. doi:10.1016/S0140-6736(20)30183-5. PMC 7159299. PMID 31986264.
- ^ “Coronavirus disease 2019 (COVID-19): Myocardial infarction and other coronary artery disease issues”. UpToDate. Retrieved 28 September 2020.
- ^ Turner AJ, Hiscox JA, Hooper NM (June 2004). “ACE2: from vasopeptidase to SARS virus receptor”. Trends in Pharmacological Sciences. 25 (6): 291–4. doi:10.1016/j.tips.2004.04.001. PMC 7119032. PMID 15165741.
- ^ Abou-Ismail MY, Diamond A, Kapoor S, Arafah Y, Nayak L (October 2020). “The hypercoagulable state in COVID-19: Incidence, pathophysiology, and management”. Thrombosis Research. Elsevier BV. 194: 101–115. doi:10.1016/j.thromres.2020.06.029. PMC 7305763. PMID 32788101.
- ^ a b Wadman M (April 2020). “How does coronavirus kill? Clinicians trace a ferocious rampage through the body, from brain to toes”. Science. doi:10.1126/science.abc3208.
- ^ “NIH study uncovers blood vessel damage and inflammation in COVID-19 patients’ brains but no infection”. National Institutes of Health (NIH). 30 December 2020. Retrieved 17 January 2021.
- ^ Celine T (8 January 2021). “COVID-19’s Severe Damage to Brain Tissues Found Through Studying Autopsies”. Science Times. Retrieved 17 January 2021.
- ^ Lee MH, Perl DP, Nair G, Li W, Maric D, Murray H, et al. (February 2021). “Microvascular Injury in the Brains of Patients with Covid-19”. The New England Journal of Medicine. 384 (5): 481–483. doi:10.1056/nejmc2033369. PMC 7787217. PMID 33378608.
- ^ “How a COVID-19 infection changes blood cells in the long run”. phys.org. Retrieved 10 July 2021.
- ^ Kubánková M, Hohberger B, Hoffmanns J, Fürst J, Herrmann M, Guck J, Kräter M (July 2021). “Physical phenotype of blood cells is altered in COVID-19”. Biophysical Journal. 120 (14): 2838–2847. Bibcode:2021BpJ…120.2838K. doi:10.1016/j.bpj.2021.05.025. PMC 8169220. PMID 34087216.
- ^ “Coronavirus: Kidney Damage Caused by COVID-19”. Johns Hopkins Medicine. 14 May 2020. Retrieved 25 January 2022.
- ^ a b c d e f g h Eketunde AO, Mellacheruvu SP, Oreoluwa P (July 2020). “A Review of Postmortem Findings in Patients With COVID-19”. Cureus. Cureus, Inc. 12 (7): e9438. doi:10.7759/cureus.9438. PMC 7451084. PMID 32864262. S2CID 221352704.
- ^ Zhang C, Wu Z, Li JW, Zhao H, Wang GQ (May 2020). “Cytokine release syndrome in severe COVID-19: interleukin-6 receptor antagonist tocilizumab may be the key to reduce mortality”. International Journal of Antimicrobial Agents. 55 (5): 105954. doi:10.1016/j.ijantimicag.2020.105954. PMC 7118634. PMID 32234467.
- ^ Gómez-Rial J, Rivero-Calle I, Salas A, Martinón-Torres F (2020). “Role of Monocytes/Macrophages in Covid-19 Pathogenesis: Implications for Therapy”. Infection and Drug Resistance. 13: 2485–2493. doi:10.2147/IDR.S258639. PMC 7383015. PMID 32801787.
- ^ Dai L, Gao GF (February 2021). “Viral targets for vaccines against COVID-19”. Nature Reviews. Immunology. 21 (2): 73–82. doi:10.1038/s41577-020-00480-0. ISSN 1474-1733. PMC 7747004. PMID 33340022.
- ^ a b Boopathi S, Poma AB, Kolandaivel P (April 2020). “Novel 2019 coronavirus structure, mechanism of action, antiviral drug promises and rule out against its treatment”. Journal of Biomolecular Structure & Dynamics. 39 (9): 3409–3418. doi:10.1080/07391102.2020.1758788. PMC 7196923. PMID 32306836.
- ^ Kai H, Kai M (July 2020). “Interactions of coronaviruses with ACE2, angiotensin II, and RAS inhibitors-lessons from available evidence and insights into COVID-19”. Hypertension Research. 43 (7): 648–654. doi:10.1038/s41440-020-0455-8. PMC 7184165. PMID 32341442.
- ^ Chen HX, Chen ZH, Shen HH (October 2020). “[Structure of SARS-CoV-2 and treatment of COVID-19]”. Sheng Li Xue Bao. 72 (5): 617–630. PMID 33106832.
- ^ Jeyanathan M, Afkhami S, Smaill F, Miller MS, Lichty BD, Xing Z (4 September 2020). “Immunological considerations for COVID-19 vaccine strategies”. Nature Reviews Immunology. 20 (10): 615–632. doi:10.1038/s41577-020-00434-6. ISSN 1474-1741. PMC 7472682. PMID 32887954.
- ^ Zhang Q, Ju B, Ge J, Chan JF, Cheng L, Wang R, et al. (July 2021). “Potent and protective IGHV3-53/3-66 public antibodies and their shared escape mutant on the spike of SARS-CoV-2“. Nature Communications. 12 (1): 4210. Bibcode:2021NatCo..12.4210Z. doi:10.1038/s41467-021-24514-w. PMC 8270942. PMID 34244522. S2CID 235786394.
- ^ Soy M, Keser G, Atagündüz P, Tabak F, Atagündüz I, Kayhan S (July 2020). “Cytokine storm in COVID-19: pathogenesis and overview of anti-inflammatory agents used in treatment”. Clinical Rheumatology. 39 (7): 2085–2094. doi:10.1007/s10067-020-05190-5. PMC 7260446. PMID 32474885.
- ^ Quirch M, Lee J, Rehman S (August 2020). “Hazards of the Cytokine Storm and Cytokine-Targeted Therapy in Patients With COVID-19: Review”. Journal of Medical Internet Research. 22 (8): e20193. doi:10.2196/20193. PMC 7428145. PMID 32707537.
- ^ Bhaskar S, Sinha A, Banach M, Mittoo S, Weissert R, Kass JS, et al. (2020). “Cytokine Storm in COVID-19-Immunopathological Mechanisms, Clinical Considerations, and Therapeutic Approaches: The REPROGRAM Consortium Position Paper”. Frontiers in Immunology. 11: 1648. doi:10.3389/fimmu.2020.01648. PMC 7365905. PMID 32754159.
- ^ a b c d e f Wastnedge EA, Reynolds RM, van Boeckel SR, Stock SJ, Denison FC, Maybin JA, Critchley HO (January 2021). “Pregnancy and COVID-19”. Physiological Reviews. 101 (1): 303–318. doi:10.1152/physrev.00024.2020. PMC 7686875. PMID 32969772.
- ^ Campbell D (10 October 2021). “One in six most critically ill NHS Covid patients are unvaccinated pregnant women”. The Guardian. Retrieved 25 January 2022.
- ^ a b c d Li C, Zhao C, Bao J, Tang B, Wang Y, Gu B (November 2020). “Laboratory diagnosis of coronavirus disease-2019 (COVID-19)”. Clinica Chimica Acta; International Journal of Clinical Chemistry. 510: 35–46. doi:10.1016/j.cca.2020.06.045. PMC 7329657. PMID 32621814.
- ^ a b Ai T, Yang Z, Hou H, Zhan C, Chen C, Lv W, et al. (August 2020). “Correlation of Chest CT and RT-PCR Testing for Coronavirus Disease 2019 (COVID-19) in China: A Report of 1014 Cases”. Radiology. 296 (2): E32–E40. doi:10.1148/radiol.2020200642. PMC 7233399. PMID 32101510.
- ^ a b c d Salehi S, Abedi A, Balakrishnan S, Gholamrezanezhad A (July 2020). “Coronavirus Disease 2019 (COVID-19): A Systematic Review of Imaging Findings in 919 Patients”. AJR. American Journal of Roentgenology. 215 (1): 87–93. doi:10.2214/AJR.20.23034. PMID 32174129.
- ^ “2019 Novel Coronavirus (2019-nCoV) Situation Summary”. U.S. Centers for Disease Control and Prevention (CDC). 30 January 2020. Archived from the original on 26 January 2020. Retrieved 30 January 2020.
- ^ “Coronavirus disease (COVID-19) technical guidance: Laboratory testing for 2019-nCoV in humans”. World Health Organization (WHO). Archived from the original on 15 March 2020. Retrieved 14 March 2020.
- ^ Bullard J, Dust K, Funk D, Strong JE, Alexander D, Garnett L, et al. (December 2020). “Predicting Infectious Severe Acute Respiratory Syndrome Coronavirus 2 From Diagnostic Samples”. Clinical Infectious Diseases. 71 (10): 2663–2666. doi:10.1093/cid/ciaa638. PMC 7314198. PMID 32442256.
- ^ “Interim Guidelines for Collecting, Handling, and Testing Clinical Specimens from Persons for Coronavirus Disease 2019 (COVID-19)”. U.S. Centers for Disease Control and Prevention (CDC). 11 February 2020. Archived from the original on 4 March 2020. Retrieved 26 March 2020.
- ^ “Real-Time RT-PCR Panel for Detection 2019-nCoV”. U.S. Centers for Disease Control and Prevention (CDC). 29 January 2020. Archived from the original on 30 January 2020. Retrieved 1 February 2020.
- ^ “Laboratory testing for 2019 novel coronavirus (2019-nCoV) in suspected human cases”. World Health Organization (WHO). Archived from the original on 17 March 2020. Retrieved 13 March 2020.
- ^ “NHS staff will be first to get new coronavirus antibody test, medical chief promises”. The Independent. 14 May 2020. Retrieved 14 May 2020.
- ^ Heneghan C, Jefferson T (1 September 2020). “Virological characterization of COVID-19 patients that test re-positive for SARS-CoV-2 by RT-PCR”. CEBM. Retrieved 19 September 2020.
- ^ Lu J, Peng J, Xiong Q, Liu Z, Lin H, Tan X, et al. (September 2020). “Clinical, immunological and virological characterization of COVID-19 patients that test re-positive for SARS-CoV-2 by RT-PCR”. EBioMedicine. 59: 102960. doi:10.1016/j.ebiom.2020.102960. PMC 7444471. PMID 32853988.
- ^ Spencer E, Jefferson T, Brassey J, Heneghan C (11 September 2020). “When is Covid, Covid?”. The Centre for Evidence-Based Medicine. Retrieved 19 September 2020.
- ^ “SARS-CoV-2 RNA testing: assurance of positive results during periods of low prevalence”. GOV.UK. Retrieved 19 September 2020.
- ^ “ACR Recommendations for the use of Chest Radiography and Computed Tomography (CT) for Suspected COVID-19 Infection”. American College of Radiology. 22 March 2020. Archived from the original on 28 March 2020.
- ^ Pormohammad A, Ghorbani S, Khatami A, Razizadeh MH, Alborzi E, Zarei M, et al. (October 2020). “Comparison of influenza type A and B with COVID-19: A global systematic review and meta-analysis on clinical, laboratory and radiographic findings”. Reviews in Medical Virology. 31 (3): e2179. doi:10.1002/rmv.2179. PMC 7646051. PMID 33035373. S2CID 222255245.
- ^ Lee EY, Ng MY, Khong PL (April 2020). “COVID-19 pneumonia: what has CT taught us?”. The Lancet. Infectious Diseases. 20 (4): 384–385. doi:10.1016/S1473-3099(20)30134-1. PMC 7128449. PMID 32105641.
- ^ a b Li Y, Xia L (June 2020). “Coronavirus Disease 2019 (COVID-19): Role of Chest CT in Diagnosis and Management”. AJR. American Journal of Roentgenology. 214 (6): 1280–1286. doi:10.2214/AJR.20.22954. PMID 32130038. S2CID 212416282.
- ^ “COVID-19 Database”. Società Italiana di Radiologia Medica e Interventistica (in Italian). Retrieved 11 March 2020.
- ^ “ICD-10 Version:2019”. World Health Organization (WHO). 2019. Archived from the original on 31 March 2020. Retrieved 31 March 2020. U07.2 – COVID-19, virus not identified – COVID-19 NOS – Use this code when COVID-19 is diagnosed clinically or epidemiologically but laboratory testing is inconclusive or not available. Use additional code, if desired, to identify pneumonia or other manifestations
- ^ Giani M, Seminati D, Lucchini A, Foti G, Pagni F (May 2020). “Exuberant Plasmocytosis in Bronchoalveolar Lavage Specimen of the First Patient Requiring Extracorporeal Membrane Oxygenation for SARS-CoV-2 in Europe”. Journal of Thoracic Oncology. 15 (5): e65–e66. doi:10.1016/j.jtho.2020.03.008. PMC 7118681. PMID 32194247.
- ^ Lillicrap D (April 2020). “Disseminated intravascular coagulation in patients with 2019-nCoV pneumonia”. Journal of Thrombosis and Haemostasis. 18 (4): 786–787. doi:10.1111/jth.14781. PMC 7166410. PMID 32212240.
- ^ Mitra A, Dwyre DM, Schivo M, Thompson GR, Cohen SH, Ku N, Graff JP (August 2020). “Leukoerythroblastic reaction in a patient with COVID-19 infection”. American Journal of Hematology. 95 (8): 999–1000. doi:10.1002/ajh.25793. PMC 7228283. PMID 32212392.
- ^ a b c d e f Satturwar S, Fowkes M, Farver C, Wilson AM, Eccher A, Girolami I, et al. (May 2021). “Postmortem Findings Associated With SARS-CoV-2: Systematic Review and Meta-analysis”. The American Journal of Surgical Pathology. 45 (5): 587–603. doi:10.1097/PAS.0000000000001650. PMC 8132567. PMID 33481385. S2CID 231679276.
- ^ Maier BF, Brockmann D (May 2020). “Effective containment explains subexponential growth in recent confirmed COVID-19 cases in China”. Science. 368 (6492): 742–746. arXiv:2002.07572. Bibcode:2020Sci…368..742M. doi:10.1126/science.abb4557. PMC 7164388. PMID 32269067. (“… initial exponential growth expected for an unconstrained outbreak.”)
- ^ “Viral Load Exposure Factors”. ReallyCorrect.com.
- ^ “Recommendation Regarding the Use of Cloth Face Coverings, Especially in Areas of Significant Community-Based Transmission”. U.S. Centers for Disease Control and Prevention (CDC). 28 June 2020.
- ^ “Scientific Brief: SARS-CoV-2 and Potential Airborne Transmission”. COVID-19 Published Science and Research. U.S. Centers for Disease Control and Prevention (CDC). 11 February 2020. Retrieved 30 October 2020.
- ^ Centers for Disease Control and Prevention (5 April 2020). “What to Do if You Are Sick”. U.S. Centers for Disease Control and Prevention (CDC). Archived from the original on 14 February 2020. Retrieved 24 April 2020.
- ^ “Coronavirus Disease 2019 (COVID-19) – Prevention & Treatment”. U.S. Centers for Disease Control and Prevention (CDC). 10 March 2020. Archived from the original on 11 March 2020. Retrieved 11 March 2020.
- ^ “UK medicines regulator gives approval for first UK COVID-19 vaccine”. Medicines and Healthcare Products Regulatory Agency, Government of the UK. 2 December 2020. Retrieved 2 December 2020.
- ^ Mueller B (2 December 2020). “U.K. Approves Pfizer Coronavirus Vaccine, a First in the West”. The New York Times. Archived from the original on 2 December 2020. Retrieved 2 December 2020.
- ^ “COVID-19 Treatment Guidelines”. nih.gov. National Institutes of Health. Retrieved 21 April 2020.
- ^ a b c Sanders JM, Monogue ML, Jodlowski TZ, Cutrell JB (May 2020). “Pharmacologic Treatments for Coronavirus Disease 2019 (COVID-19): A Review”. JAMA. 323 (18): 1824–1836. doi:10.1001/jama.2020.6019. PMID 32282022.
- ^ a b Anderson RM, Heesterbeek H, Klinkenberg D, Hollingsworth TD (March 2020). “How will country-based mitigation measures influence the course of the COVID-19 epidemic?”. Lancet. 395 (10228): 931–934. doi:10.1016/S0140-6736(20)30567-5. PMC 7158572. PMID 32164834. A key issue for epidemiologists is helping policy makers decide the main objectives of mitigation – e.g. minimising morbidity and associated mortality, avoiding an epidemic peak that overwhelms health-care services, keeping the effects on the economy within manageable levels, and flattening the epidemic curve to wait for vaccine development and manufacture on scale and antiviral drug therapies.
- ^ Wiles S (14 March 2020). “After ‘Flatten the Curve’, we must now ‘Stop the Spread’. Here’s what that means”. The Spinoff. Archived from the original on 26 March 2020. Retrieved 13 March 2020.
- ^ Li YD, Chi WY, Su JH, Ferrall L, Hung CF, Wu TC (December 2020). “Coronavirus vaccine development: from SARS and MERS to COVID-19”. Journal of Biomedical Science. 27 (1): 104. doi:10.1186/s12929-020-00695-2. PMC 7749790. PMID 33341119.
- ^ Subbarao K (July 2021). “The success of SARS-CoV-2 vaccines and challenges ahead”. Cell Host & Microbe. 29 (7): 1111–1123. doi:10.1016/j.chom.2021.06.016. PMC 8279572. PMID 34265245.
- ^ Padilla TB (24 February 2021). “No one is safe unless everyone is safe”. BusinessWorld. Retrieved 24 February 2021.
- ^ Vergano D (5 June 2021). “COVID-19 Vaccines Work Way Better Than We Had Ever Expected. Scientists Are Still Figuring Out Why”. BuzzFeed News. Retrieved 24 June 2021.
- ^ Mallapaty S, Callaway E, Kozlov M, Ledford H, Pickrell J, Van Noorden R (December 2021). “How COVID vaccines shaped 2021 in eight powerful charts”. Nature. 600 (7890): 580–583. Bibcode:2021Natur.600..580M. doi:10.1038/d41586-021-03686-x. PMID 34916666. S2CID 245262732.
- ^ Beaumont P (18 November 2020). “Covid-19 vaccine: who are countries prioritising for first doses?”. The Guardian. ISSN 0261-3077. Retrieved 26 December 2020.
- ^ Richie H, Ortiz-Ospina E, Beltekian D, Methieu E, Hasell J, Macdonald B, et al. (5 March 2020). “Coronavirus (COVID-19) Vaccinations – Statistics and Research”. Our World in Data. Retrieved 7 February 2021.
- ^ Mullard A (November 2020). “How COVID vaccines are being divvied up around the world”. Nature. doi:10.1038/d41586-020-03370-6. PMID 33257891. S2CID 227246811.
- ^ So AD, Woo J (December 2020). “Reserving coronavirus disease 2019 vaccines for global access: cross sectional analysis”. BMJ. 371: m4750. doi:10.1136/bmj.m4750. PMC 7735431. PMID 33323376.
- ^ Hotez PJ, Bottazzi ME (January 2022). “Whole Inactivated Virus and Protein-Based COVID-19 Vaccines”. Annual Review of Medicine. 73 (1): 55–64. doi:10.1146/annurev-med-042420-113212. PMID 34637324.
- ^ Ye Y, Zhang Q, Wei X, Cao Z, Yuan H, Zeng DD (February 2022). “Equitable access to COVID-19 vaccines makes a life-saving difference to all countries”. Nature Human Behaviour. 6 (2): 207–216. doi:10.1038/s41562-022-01289-8.
- ^ “Wear masks in public says WHO, in update of COVID-19 advice”. Reuters. 5 June 2020. Retrieved 3 July 2020.
- ^ a b c “Recommendation Regarding the Use of Cloth Face Coverings, Especially in Areas of Significant Community-Based Transmission”. U.S. Centers for Disease Control and Prevention (CDC). 11 February 2020. Retrieved 17 April 2020.
- ^ a b “Using face masks in the community – Technical Report” (PDF). ECDC. 8 April 2020.
- ^ “Scientific Brief: Community Use of Cloth Masks to Control the Spread of SARS-CoV-2“. U.S. Centers for Disease Control and Prevention (CDC). 10 November 2020.
- ^ Greenhalgh T, Schmid MB, Czypionka T, Bassler D, Gruer L (April 2020). “Face masks for the public during the covid-19 crisis”. BMJ. 369: m1435. doi:10.1136/bmj.m1435. PMID 32273267. S2CID 215516381.
- ^ “Caring for Someone Sick at Home”. U.S. Centers for Disease Control and Prevention (CDC). 11 February 2020. Retrieved 3 July 2020.
- ^ “Using Personal Protective Equipment (PPE)”. U.S. Centers for Disease Control and Prevention (CDC). 11 June 2020. Retrieved 4 July 2020.
- ^ a b c CDC (11 February 2020). “Scientific Brief: SARS-CoV-2 Transmission”. U.S. Centers for Disease Control and Prevention (CDC). Retrieved 10 May 2021.
- ^ “Transmission of COVID-19”. www.ecdc.europa.eu. 7 September 2020. Retrieved 14 October 2020.
- ^ a b National Center for Immunization and Respiratory Diseases (NCIRD) (9 July 2020). “COVID-19 Employer Information for Office Buildings”. U.S. Centers for Disease Control and Prevention (CDC). Retrieved 9 July 2020.
- ^ World Health Organization (29 October 2020). WHO’s Science in 5 on COVID-19 – Ventilation. Retrieved 2 November 2020 – via YouTube.
- ^ Somsen GA, van Rijn C, Kooij S, Bem RA, Bonn D (July 2020). “Small droplet aerosols in poorly ventilated spaces and SARS-CoV-2 transmission”. The Lancet. Respiratory Medicine. Elsesier. 8 (7): 658–659. doi:10.1016/S2213-2600(20)30245-9. PMC 7255254. PMID 32473123.
- ^ Lipinski T, Ahmad D, Serey N, Jouhara H (1 November 2020). “Review of ventilation strategies to reduce the risk of disease transmission in high occupancy buildings”. International Journal of Thermofluids. 7–8: 100045. doi:10.1016/j.ijft.2020.100045. ISSN 2666-2027. S2CID 221642242.
- ^ “Social distancing: what you need to do – Coronavirus (COVID-19)”. nhs.uk. 2 June 2020. Retrieved 18 August 2020.
- ^ “Advice for the public on COVID-19 – World Health Organization”. World Health Organization (WHO). Retrieved 18 August 2020.
- ^ “COVID-19 and Your Health”. U.S. Centers for Disease Control and Prevention (CDC). 11 February 2020. Retrieved 23 March 2021. To prevent the spread of germs, including COVID-19, CDC recommends washing hands with soap and water whenever possible because it reduces the amount of many types of germs and chemicals on hands. But if soap and water are not readily available, using a hand sanitizer with at least 60% alcohol can help you avoid getting sick and spreading germs to others.
- ^ “WHO-recommended handrub formulations”. WHO Guidelines on Hand Hygiene in Health Care: First Global Patient Safety Challenge Clean Care Is Safer Care. World Health Organization (WHO). 19 March 2009. Retrieved 19 March 2020.
- ^ Nussbaumer-Streit, Barbara; Mayr, Verena; Dobrescu, Andreea Iulia; Chapman, Andrea; Persad, Emma; Klerings, Irma; Wagner, Gernot; Siebert, Uwe; Ledinger, Dominic; Zachariah, Casey; Gartlehner, Gerald (15 September 2020). “Quarantine alone or in combination with other public health measures to control COVID-19: a rapid review”. The Cochrane Database of Systematic Reviews. 2020 (9): CD013574. doi:10.1002/14651858.CD013574.pub2. ISSN 1469-493X. PMC 8133397. PMID 33959956.
- ^ Qian M, Jiang J (May 2020). “COVID-19 and social distancing”. Zeitschrift für Gesundheitswissenschaften = Journal of Public Health. 30 (1): 259–261. doi:10.1007/s10389-020-01321-z. PMC 7247774. PMID 32837835.
- ^ a b Hawks L, Woolhandler S, McCormick D (August 2020). “COVID-19 in Prisons and Jails in the United States”. JAMA Internal Medicine. 180 (8): 1041–1042. doi:10.1001/jamainternmed.2020.1856. PMID 32343355.
- ^ Waldstein D (6 May 2020). “To Fight Virus in Prisons, C.D.C. Suggests More Screenings”. The New York Times. Archived from the original on 7 May 2020. Retrieved 14 May 2020.
- ^ “How COVID-19 Spreads”. U.S. Centers for Disease Control and Prevention (CDC). 18 September 2020. Archived from the original on 19 September 2020. Retrieved 20 September 2020.
- ^ Goldman E (August 2020). “Exaggerated risk of transmission of COVID-19 by fomites”. The Lancet. Infectious Diseases. 20 (8): 892–893. doi:10.1016/S1473-3099(20)30561-2. PMC 7333993. PMID 32628907.
- ^ Weixel N (5 April 2021). “CDC says risk of COVID-19 transmission on surfaces 1 in 10,000”. TheHill. Retrieved 19 December 2021.
- ^ a b “Science Brief: SARS-CoV-2 and Surface (Fomite) Transmission for Indoor Community Environments”. U.S. Centers for Disease Control and Prevention (CDC). 5 April 2021. Archived from the original on 5 April 2021.
- ^ a b Pedreira A, Taşkın Y, García MR (January 2021). “A Critical Review of Disinfection Processes to Control SARS-CoV-2 Transmission in the Food Industry”. Foods. 10 (2): 283. doi:10.3390/foods10020283. PMC 7911259. PMID 33572531. S2CID 231900820.
- ^ Rezasoltani S, Yadegar A, Hatami B, Asadzadeh Aghdaei H, Zali MR (2020). “Antimicrobial Resistance as a Hidden Menace Lurking Behind the COVID-19 Outbreak: The Global Impacts of Too Much Hygiene on AMR”. Frontiers in Microbiology. 11: 590683. doi:10.3389/fmicb.2020.590683. PMC 7769770. PMID 33384670.
- ^ Thompson D (8 February 2021). “Hygiene Theater Is Still a Huge Waste of Time”. The Atlantic. Retrieved 27 February 2021.
- ^ Thompson D (27 July 2020). “Hygiene Theater Is a Huge Waste of Time”. The Atlantic. Retrieved 27 February 2021.
- ^ a b c d e f g Bueckert M, Gupta R, Gupta A, Garg M, Mazumder A (November 2020). “Infectivity of SARS-CoV-2 and Other Coronaviruses on Dry Surfaces: Potential for Indirect Transmission”. Materials. 13 (22): 5211. Bibcode:2020Mate…13.5211B. doi:10.3390/ma13225211. PMC 7698891. PMID 33218120.
- ^ Bhardwaj R, Agrawal A (November 2020). “How coronavirus survives for days on surfaces”. Physics of Fluids. 32 (11): 111706. Bibcode:2020PhFl…32k1706B. doi:10.1063/5.0033306. PMC 7713872. PMID 33281435.
- ^ Chatterjee S, Murallidharan JS, Agrawal A, Bhardwaj R (February 2021). “Why coronavirus survives longer on impermeable than porous surfaces”. Physics of Fluids. 33 (2): 021701. Bibcode:2021PhFl…33b1701C. doi:10.1063/5.0037924. PMC 7978145. PMID 33746485.
- ^ CDC (11 February 2020). “Coronavirus Disease 2019 (COVID-19)”. U.S. Centers for Disease Control and Prevention (CDC). Retrieved 12 April 2021.
- ^ Anthes E (8 April 2021). “Has the Era of Overzealous Cleaning Finally Come to an End?”. The New York Times. Archived from the original on 28 December 2021. Retrieved 12 April 2021.
- ^ “Interim Recommendations for US Community Facilities with Suspected/Confirmed Coronavirus Disease 2019”. U.S. Centers for Disease Control and Prevention (CDC). 11 February 2020. Retrieved 4 April 2020.
- ^ “Yes, UV phone sanitizers work. That doesn’t mean you need one”. The Washington Post. 16 February 2021. Retrieved 29 April 2022.
- ^ Patiño-Lugo DF, Vélez M, Velásquez Salazar P, Vera-Giraldo CY, Vélez V, Marín IC, et al. (June 2020). “Non-pharmaceutical interventions for containment, mitigation and suppression of COVID-19 infection”. Colombia Medica. 51 (2): e4266. doi:10.25100/cm.v51i2.4266. PMC 7518730. PMID 33012884.
- ^ “COVID-19 Informational Resources for High-Risk Groups | Keeping Education ACTIVE | Partnership to Fight Chronic Disease”. fightchronicdisease.org. Retrieved 31 May 2020.
- ^ “Quarantine and Isolation”. U.S. Centers for Disease Control and Prevention (CDC). 29 July 2021. Retrieved 12 August 2021.
- ^ “Food safety, nutrition, and wellness during COVID-19”. The Nutrition Source. Harvard T.H. Chan School of Public Health. 29 May 2020. Retrieved 8 November 2020.
- ^ Reynolds G (14 April 2021). “Regular Exercise May Help Protect Against Severe COVID”. The New York Times. Archived from the original on 28 December 2021. Retrieved 10 May 2021.
- ^ Sallis R, Young DR, Tartof SY, Sallis JF, Sall J, Li Q, et al. (April 2021). “Physical inactivity is associated with a higher risk for severe COVID-19 outcomes: a study in 48 440 adult patients”. British Journal of Sports Medicine. 55 (19): 1099–1105. doi:10.1136/bjsports-2021-104080. PMC 8050880. PMID 33849909.
- ^ Szarpak L, Filipiak KJ, Gasecka A, Gawel W, Koziel D, Jaguszewski MJ, et al. (October 2021). “Vitamin D supplementation to treat SARS-CoV-2 positive patients. Evidence from meta-analysis”. Cardiology Journal. 29 (2): 188–196. doi:10.5603/CJ.a2021.0122. PMID 34642923. S2CID 238746984.
- ^ “Trial to test if Vitamin D protects against Covid”. BBC News. 13 October 2020. Retrieved 10 November 2020.
- ^ a b “Trial of Vitamin D to Reduce Risk and Severity of COVID-19 and Other Acute Respiratory Infections – Full Text View – ClinicalTrials.gov”. clinicaltrials.gov. Retrieved 10 November 2020.
- ^ a b c Burns J, Movsisyan A, Stratil JM, Biallas RL, Coenen M, Emmert-Fees KM, et al. (Cochrane Public Health Group) (March 2021). “International travel-related control measures to contain the COVID-19 pandemic: a rapid review”. The Cochrane Database of Systematic Reviews. 2021 (3): CD013717. doi:10.1002/14651858.CD013717.pub2. PMC 8406796. PMID 33763851. S2CID 232356197.
- ^ Siemieniuk RA, Bartoszko JJ, Ge L, Zeraatkar D, Izcovich A, Kum E, et al. (July 2020). “Drug treatments for covid-19: living systematic review and network meta-analysis”. BMJ. 370: m2980. doi:10.1136/bmj.m2980. PMC 7390912. PMID 32732190.
- ^ a b “Coronavirus”. WebMD. Archived from the original on 1 February 2020. Retrieved 1 February 2020.
- ^ “COVID Treatment Guidelines: Clinical Management Summary”. NIH Coronavirus Disease 2019 (COVID-19) Treatment Guidelines. 8 April 2022. Retrieved 19 April 2022.
- ^ Wise, Jeff (17 April 2022). “What Happened to Paxlovid, the COVID Wonder Drug?”. Intelligencer. Retrieved 19 April 2022.
- ^ Tao K, Tzou PL, Nouhin J, Bonilla H, Jagannathan P, Shafer RW (July 2021). “SARS-CoV-2 Antiviral Therapy”. Clinical Microbiology Reviews. 34 (4): e0010921. doi:10.1128/CMR.00109-21. PMC 8404831. PMID 34319150. S2CID 236472654.
- ^ Fisher D, Heymann D (February 2020). “Q&A: The novel coronavirus outbreak causing COVID-19”. BMC Medicine. 18 (1): 57. doi:10.1186/s12916-020-01533-w. PMC 7047369. PMID 32106852.
- ^ Liu K, Fang YY, Deng Y, Liu W, Wang MF, Ma JP, et al. (May 2020). “Clinical characteristics of novel coronavirus cases in tertiary hospitals in Hubei Province”. Chinese Medical Journal. 133 (9): 1025–1031. doi:10.1097/CM9.0000000000000744. PMC 7147277. PMID 32044814.
- ^ Wang T, Du Z, Zhu F, Cao Z, An Y, Gao Y, Jiang B (March 2020). “Comorbidities and multi-organ injuries in the treatment of COVID-19”. Lancet. Elsevier BV. 395 (10228): e52. doi:10.1016/s0140-6736(20)30558-4. PMC 7270177. PMID 32171074.
- ^ Wang Y, Wang Y, Chen Y, Qin Q (March 2020). “Unique epidemiological and clinical features of the emerging 2019 novel coronavirus pneumonia (COVID-19) implicate special control measures”. Journal of Medical Virology. 92 (6): 568–576. doi:10.1002/jmv.25748. PMC 7228347. PMID 32134116.
- ^ Martel J, Ko YF, Young JD, Ojcius DM (May 2020). “Could nasal breathing help to mitigate the severity of COVID-19”. Microbes and Infection. 22 (4–5): 168–171. doi:10.1016/j.micinf.2020.05.002. PMC 7200356. PMID 32387333.
- ^ “Coronavirus recovery: breathing exercises”. www.hopkinsmedicine.org. Johns Hopkins Medicine. Retrieved 30 July 2020.
- ^ Wang L, Wang Y, Ye D, Liu Q (March 2020). “Review of the 2019 novel coronavirus (SARS-CoV-2) based on current evidence”. International Journal of Antimicrobial Agents. 55 (6): 105948. doi:10.1016/j.ijantimicag.2020.105948. PMC 7156162. PMID 32201353.
- ^ U.S. Centers for Disease Control and Prevention (5 April 2020). “What to Do if You Are Sick”. U.S. Centers for Disease Control and Prevention (CDC). Archived from the original on 14 February 2020. Retrieved 24 April 2020.
- ^ “Update to living WHO guideline on drugs for covid-19”. BMJ (Clinical Research Ed.). 371: m4475. November 2020. doi:10.1136/bmj.m4475. ISSN 1756-1833. PMID 33214213. S2CID 227059995.
- ^ “Q&A: Dexamethasone and COVID-19”. World Health Organization (WHO). Retrieved 11 July 2020.
- ^ “Home”. National COVID-19 Clinical Evidence Taskforce. Retrieved 11 July 2020.
- ^ “COVID-19 Treatment Guidelines”. www.nih.gov. National Institutes of Health. Retrieved 18 January 2021.
- ^ Guan WJ, Ni ZY, Hu Y, Liang WH, Ou CQ, He JX, et al. (April 2020). “Clinical Characteristics of Coronavirus Disease 2019 in China”. The New England Journal of Medicine. Massachusetts Medical Society. 382 (18): 1708–1720. doi:10.1056/nejmoa2002032. PMC 7092819. PMID 32109013.
- ^ Henry BM (April 2020). “COVID-19, ECMO, and lymphopenia: a word of caution”. The Lancet. Respiratory Medicine. Elsevier BV. 8 (4): e24. doi:10.1016/s2213-2600(20)30119-3. PMC 7118650. PMID 32178774.
- ^ Kim JS, Lee JY, Yang JW, Lee KH, Effenberger M, Szpirt W, et al. (2021). “Immunopathogenesis and treatment of cytokine storm in COVID-19”. Theranostics. 11 (1): 316–329. doi:10.7150/thno.49713. PMC 7681075. PMID 33391477.
- ^ Doshi P (October 2020). “Will covid-19 vaccines save lives? Current trials aren’t designed to tell us”. BMJ. 371: m4037. doi:10.1136/bmj.m4037. PMID 33087398. S2CID 224817161.
- ^ a b Palmieri L, Andrianou X, Barbariol P, Bella A, Bellino S, Benelli E, et al. (22 July 2020). Characteristics of SARS-CoV-2 patients dying in Italy Report based on available data on July 22nd, 2020 (PDF) (Report). Istituto Superiore di Sanità. Retrieved 4 October 2020.
- ^ Baranovskii DS, Klabukov ID, Krasilnikova OA, Nikogosov DA, Polekhina NV, Baranovskaia DR, et al. (December 1975). “Letter: Acid secretion by gastric mucous membrane”. The American Journal of Physiology. 229 (6): 21–25. doi:10.1080/03007995.2020.1853510. PMC 7738209. PMID 33210948. S2CID 227065216.
- ^ Christensen B, Favaloro EJ, Lippi G, Van Cott EM (October 2020). “Hematology Laboratory Abnormalities in Patients with Coronavirus Disease 2019 (COVID-19)”. Seminars in Thrombosis and Hemostasis. 46 (7): 845–849. doi:10.1055/s-0040-1715458. PMC 7645834. PMID 32877961.
- ^ “Living with Covid19”. NIHR Themed Reviews. National Institute for Health Research. 15 October 2020. doi:10.3310/themedreview_41169.
- ^ a b “How long does COVID-19 last?”. UK COVID Symptom Study. 6 June 2020. Retrieved 15 October 2020.
- ^ “Summary of COVID-19 Long Term Health Effects: Emerging evidence and Ongoing Investigation” (PDF). University of Washington. 1 September 2020. Archived from the original (PDF) on 18 December 2020. Retrieved 15 October 2020.
- ^ “Long-term symptoms of COVID-19 ‘really concerning’, says WHO chief”. UN News. 30 October 2020. Retrieved 7 March 2021.
- ^ “Coronavirus disease 2019 (COVID-19) – Prognosis”. BMJ. Retrieved 15 November 2020.
- ^ Lavery AM, Preston LE, Ko JY, Chevinsky JR, DeSisto CL, Pennington AF, et al. (November 2020). “Characteristics of Hospitalized COVID-19 Patients Discharged and Experiencing Same-Hospital Readmission – United States, March-August 2020”. MMWR. Morbidity and Mortality Weekly Report. 69 (45): 1695–1699. doi:10.15585/mmwr.mm6945e2. PMC 7660660. PMID 33180754.
- ^ Vardavas CI, Nikitara K (March 2020). “COVID-19 and smoking: A systematic review of the evidence”. Tobacco Induced Diseases. 18: 20. doi:10.18332/tid/119324. PMC 7083240. PMID 32206052.
- ^ a b c Engin AB, Engin ED, Engin A (August 2020). “Two important controversial risk factors in SARS-CoV-2 infection: Obesity and smoking”. Environmental Toxicology and Pharmacology. 78: 103411. doi:10.1016/j.etap.2020.103411. PMC 7227557. PMID 32422280.
- ^ Setti L, Passarini F, De Gennaro G, Barbieri P, Licen S, Perrone MG, et al. (September 2020). “Potential role of particulate matter in the spreading of COVID-19 in Northern Italy: first observational study based on initial epidemic diffusion”. BMJ Open. 10 (9): e039338. doi:10.1136/bmjopen-2020-039338. PMC 7517216. PMID 32973066.
- ^ Wu X, Nethery RC, Sabath MB, Braun D, Dominici F (November 2020). “Air pollution and COVID-19 mortality in the United States: Strengths and limitations of an ecological regression analysis”. Science Advances. 6 (45): eabd4049. Bibcode:2020SciA….6.4049W. doi:10.1126/sciadv.abd4049. PMC 7673673. PMID 33148655.
- ^ Pansini R, Fornacca D (June 2021). “Early Spread of COVID-19 in the Air-Polluted Regions of Eight Severely Affected Countries”. Atmosphere. 12 (6): 795. Bibcode:2021Atmos..12..795P. doi:10.3390/atmos12060795.
- ^ Comunian S, Dongo D, Milani C, Palestini P (June 2020). “Air Pollution and Covid-19: The Role of Particulate Matter in the Spread and Increase of Covid-19’s Morbidity and Mortality”. International Journal of Environmental Research and Public Health. 17 (12): 4487. doi:10.3390/ijerph17124487. PMC 7345938. PMID 32580440.
- ^ Domingo JL, Marquès M, Rovira J (September 2020). “Influence of airborne transmission of SARS-CoV-2 on COVID-19 pandemic. A review”. Environmental Research. 188: 109861. Bibcode:2020ER….188j9861D. doi:10.1016/j.envres.2020.109861. PMC 7309850. PMID 32718835.
- ^ “COVID-19: Who’s at higher risk of serious symptoms?”. Mayo Clinic.
- ^ Tamara A, Tahapary DL (July 2020). “Obesity as a predictor for a poor prognosis of COVID-19: A systematic review”. Diabetes & Metabolic Syndrome. 14 (4): 655–659. doi:10.1016/j.dsx.2020.05.020. PMC 7217103. PMID 32438328.
- ^ Petrakis D, Margină D, Tsarouhas K, Tekos F, Stan M, Nikitovic D, et al. (July 2020). “Obesity – A risk factor for increased COVID-19, severity and lethality (Review)”. Molecular Medicine Reports. 22 (1): 9–19. doi:10.3892/mmr.2020.11127. PMC 7248467. PMID 32377709.
- ^ Roca-Fernández A, Dennis A, Nicholls R, McGonigle J, Kelly M, Banerjee R, et al. (29 March 2021). “Hepatic Steatosis, Rather Than Underlying Obesity, Increases the Risk of Infection and Hospitalization for COVID-19”. Frontiers in Medicine. 8: 636637. doi:10.3389/fmed.2021.636637. ISSN 2296-858X. PMC 8039134. PMID 33855033.
- ^ “Coronavirus Disease 2019 (COVID-19)”. U.S. Centers for Disease Control and Prevention (CDC). 11 February 2020.
- ^ Devresse A, Belkhir L, Vo B, Ghaye B, Scohy A, Kabamba B, et al. (November 2020). “COVID-19 Infection in Kidney Transplant Recipients: A Single-Center Case Series of 22 Cases From Belgium”. Kidney Medicine. 2 (4): 459–466. doi:10.1016/j.xkme.2020.06.001. PMC 7295531. PMID 32775986.
- ^ Shelton JF, Shastri AJ, Ye C, Weldon CH, Filshtein-Sonmez T, Coker D, et al. (April 2021). “Trans-ancestry analysis reveals genetic and nongenetic associations with COVID-19 susceptibility and severity”. Nature Genetics. 53 (6): 801–808. doi:10.1038/s41588-021-00854-7. PMID 33888907. S2CID 233372385.
- ^ Wallis C. “One in Seven Dire COVID Cases May Result from a Faulty Immune Response”. Scientific American.
- ^ Bastard P, Rosen LB, Zhang Q, Michailidis E, Hoffmann HH, Zhang Y, et al. (October 2020). “Autoantibodies against type I IFNs in patients with life-threatening COVID-19”. Science. 370 (6515): eabd4585. doi:10.1126/science.abd4585. PMC 7857397. PMID 32972996. S2CID 221914095.
- ^ Fusco DN, Brisac C, John SP, Huang YW, Chin CR, Xie T, et al. (June 2013). “A genetic screen identifies interferon-α effector genes required to suppress hepatitis C virus replication”. Gastroenterology. 144 (7): 1438–49, 1449.e1-9. doi:10.1053/j.gastro.2013.02.026. PMC 3665646. PMID 23462180.
- ^ “COVID-19 in children and the role of school settings in transmission – first update”. European Centre for Disease Prevention and Control. 23 December 2020. Retrieved 6 April 2021.
- ^ “Estimated Disease Burden of COVID-19”. U.S. Centers for Disease Control and Prevention (CDC). 11 February 2020. Retrieved 6 April 2021.
- ^ Reardon S (2 September 2021). “Why don’t kids tend to get as sick from Covid-19?”. Knowable Magazine. doi:10.1146/knowable-090121-1. S2CID 239653475. Retrieved 7 September 2021.
- ^ “Information for Pediatric Healthcare Providers”. U.S. Centers for Disease Control and Prevention (CDC). 11 February 2020. Retrieved 6 April 2021.
- ^ Götzinger F, Santiago-García B, Noguera-Julián A, Lanaspa M, Lancella L, Calò Carducci FI, et al. (September 2020). “COVID-19 in children and adolescents in Europe: a multinational, multicentre cohort study”. The Lancet. Child & Adolescent Health. 4 (9): 653–661. doi:10.1016/S2352-4642(20)30177-2. PMC 7316447. PMID 32593339.
- ^ Fang L, Karakiulakis G, Roth M (April 2020). “Are patients with hypertension and diabetes mellitus at increased risk for COVID-19 infection?”. The Lancet. Respiratory Medicine. 8 (4): e21. doi:10.1016/S0140-6736(20)30311-1. PMC 7118626. PMID 32171062.
- ^ “Coronavirus Disease 2019 (COVID-19)”. U.S. Centers for Disease Control and Prevention (CDC). 11 February 2020. Archived from the original on 2 March 2020. Retrieved 2 March 2020.
- ^ Hui DS, I Azhar E, Madani TA, Ntoumi F, Kock R, Dar O, et al. (February 2020). “The continuing 2019-nCoV epidemic threat of novel coronaviruses to global health – The latest 2019 novel coronavirus outbreak in Wuhan, China”. International Journal of Infectious Diseases. 91: 264–266. doi:10.1016/j.ijid.2020.01.009. PMC 7128332. PMID 31953166.
- ^ Murthy S, Gomersall CD, Fowler RA (April 2020). “Care for Critically Ill Patients With COVID-19”. JAMA. 323 (15): 1499–1500. doi:10.1001/jama.2020.3633. PMID 32159735.
- ^ Cascella M, Rajnik M, Cuomo A, Dulebohn SC, Di Napoli R (2020). “Features, Evaluation and Treatment Coronavirus (COVID-19)”. StatPearls. Treasure Island (FL): StatPearls Publishing. PMID 32150360. Retrieved 18 March 2020.
- ^ Heymann DL, Shindo N, et al. (WHO Scientific and Technical Advisory Group for Infectious Hazards) (February 2020). “COVID-19: what is next for public health?”. Lancet. 395 (10224): 542–545. doi:10.1016/s0140-6736(20)30374-3. PMC 7138015. PMID 32061313.
- ^ Romiti GF, Corica B, Lip GY, Proietti M (June 2021). “Prevalence and Impact of Atrial Fibrillation in Hospitalized Patients with COVID-19: A Systematic Review and Meta-Analysis”. Journal of Clinical Medicine. 10 (11): 2490. doi:10.3390/jcm10112490. PMC 8200114. PMID 34199857.
- ^ Wen W, Zhang H, Zhou M, Cheng Y, Ye L, Chen J, et al. (November 2020). “Arrhythmia in patients with severe coronavirus disease (COVID-19): a meta-analysis”. European Review for Medical and Pharmacological Sciences. 24 (21): 11395–11401. doi:10.26355/eurrev_202011_23632. PMID 33215461. S2CID 227077132.
- ^ Long B, Brady WJ, Koyfman A, Gottlieb M (July 2020). “Cardiovascular complications in COVID-19”. The American Journal of Emergency Medicine. 38 (7): 1504–1507. doi:10.1016/j.ajem.2020.04.048. PMC 7165109. PMID 32317203.
- ^ Puntmann VO, Carerj ML, Wieters I, Fahim M, Arendt C, Hoffmann J, et al. (November 2020). “Outcomes of Cardiovascular Magnetic Resonance Imaging in Patients Recently Recovered From Coronavirus Disease 2019 (COVID-19)”. JAMA Cardiology. 5 (11): 1265–1273. doi:10.1001/jamacardio.2020.3557. PMC 7385689. PMID 32730619.
- ^ Lindner D, Fitzek A, Bräuninger H, Aleshcheva G, Edler C, Meissner K, et al. (November 2020). “Association of Cardiac Infection With SARS-CoV-2 in Confirmed COVID-19 Autopsy Cases”. JAMA Cardiology. 5 (11): 1281–1285. doi:10.1001/jamacardio.2020.3551. PMC 7385672. PMID 32730555.
- ^ Siripanthong B, Nazarian S, Muser D, Deo R, Santangeli P, Khanji MY, et al. (September 2020). “Recognizing COVID-19-related myocarditis: The possible pathophysiology and proposed guideline for diagnosis and management”. Heart Rhythm. 17 (9): 1463–1471. doi:10.1016/j.hrthm.2020.05.001. PMC 7199677. PMID 32387246.
- ^ Xu L, Liu J, Lu M, Yang D, Zheng X (May 2020). “Liver injury during highly pathogenic human coronavirus infections”. Liver International. 40 (5): 998–1004. doi:10.1111/liv.14435. PMC 7228361. PMID 32170806.
- ^ Carod-Artal FJ (May 2020). “Neurological complications of coronavirus and COVID-19”. Revista de Neurología. 70 (9): 311–322. doi:10.33588/rn.7009.2020179. PMID 32329044. S2CID 226200547.
- ^ Toscano G, Palmerini F, Ravaglia S, Ruiz L, Invernizzi P, Cuzzoni MG, et al. (June 2020). “Guillain-Barré Syndrome Associated with SARS-CoV-2“. The New England Journal of Medicine. 382 (26): 2574–2576. doi:10.1056/NEJMc2009191. PMC 7182017. PMID 32302082.
- ^ “Multisystem inflammatory syndrome in children and adolescents temporally related to COVID-19”. World Health Organization (WHO). 15 May 2020. Retrieved 20 May 2020.
- ^ HAN Archive – 00432. U.S. Centers for Disease Control and Prevention (CDC) (Report). 15 May 2020. Retrieved 20 May 2020.
- ^ Poyiadji N, Shahin G, Noujaim D, Stone M, Patel S, Griffith B (August 2020). “COVID-19-associated Acute Hemorrhagic Necrotizing Encephalopathy: Imaging Features”. Radiology. 296 (2): E119–E120. doi:10.1148/radiol.2020201187. PMC 7233386. PMID 32228363.
- ^ a b Córdoba-Vives S, Peñaranda G (April 2020). “COVID-19 y Embarazo”. Medical Journal of Costa Rica (in Spanish): 629. Archived from the original on 18 June 2021. Retrieved 14 February 2022.
- ^ Das S, Dhar S (July 2021). “Mucormycosis Following COVID-19 Infections: an Insight”. The Indian Journal of Surgery: 1–2. doi:10.1007/s12262-021-03028-1. PMC 8270771. PMID 34276145. S2CID 235782159.
- ^ Baruah C, Devi P, Deka B, Sharma DK (June 2021). “Mucormycosis and Aspergillosis have been Linked to Covid-19-Related Fungal Infections in India”. Advancements in Case Studies. 3 (1). doi:10.31031/AICS.2021.03.000555. ISSN 2639-0531. S2CID 244678882 – via ResearchGate.
- ^ “Living with Covid19”. NIHR Themed Review. National Institute for Health Research. 15 October 2020. doi:10.3310/themedreview_41169. S2CID 241034526.
- ^ “Summary of COVID-19 Long Term Health Effects: Emerging evidence and Ongoing Investigation” (PDF). University of Washington. 1 September 2020. Retrieved 15 October 2020.
- ^ Huang C, Wang Y, Li X, Ren L, Zhao J, Hu Y, et al. (February 2020). “Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China”. Lancet. 395 (10223): 497–506. doi:10.1016/S0140-6736(20)30183-5. PMC 7159299. PMID 31986264.
- ^ a b Torres-Castro R, Vasconcello-Castillo L, Alsina-Restoy X, Solis-Navarro L, Burgos F, Puppo H, Vilaró J (November 2020). “Respiratory function in patients post-infection by COVID-19: a systematic review and meta-analysis”. Pulmonology. Elsevier BV. 27 (4): 328–337. doi:10.1016/j.pulmoe.2020.10.013. PMC 7687368. PMID 33262076. S2CID 227162748.
- ^ Shaw B, Daskareh M, Gholamrezanezhad A (January 2021). “The lingering manifestations of COVID-19 during and after convalescence: update on long-term pulmonary consequences of coronavirus disease 2019 (COVID-19)”. La Radiologia Medica. 126 (1): 40–46. doi:10.1007/s11547-020-01295-8. PMC 7529085. PMID 33006087.
- ^ Zhao YM, Shang YM, Song WB, Li QQ, Xie H, Xu QF, et al. (August 2020). “Follow-up study of the pulmonary function and related physiological characteristics of COVID-19 survivors three months after recovery”. EClinicalMedicine. 25: 100463. doi:10.1016/j.ijtb.2020.11.003. PMC 7654356. PMID 32838236.
- ^ “Immune responses and correlates of protective immunity against SARS-CoV-2“. European Centre for Disease Prevention and Control. 18 May 2021. Retrieved 3 June 2021.
- ^ Vabret N, Britton GJ, Gruber C, Hegde S, Kim J, Kuksin M, et al. (June 2020). “Immunology of COVID-19: Current State of the Science”. Immunity. 52 (6): 910–941. doi:10.1016/j.immuni.2020.05.002. PMC 7200337. PMID 32505227.
- ^ Wang Z, Muecksch F, Schaefer-Babajew D, Finkin S, Viant C, Gaebler C, et al. (July 2021). “Naturally enhanced neutralizing breadth against SARS-CoV-2 one year after infection”. Nature. 595 (7867): 426–431. Bibcode:2021Natur.595..426W. doi:10.1038/s41586-021-03696-9. PMC 8277577. PMID 34126625.
- ^ a b Cohen JI, Burbelo PD (December 2020). “Reinfection with SARS-CoV-2: Implications for Vaccines”. Clinical Infectious Diseases. 73 (11): e4223–e4228. doi:10.1093/cid/ciaa1866. PMC 7799323. PMID 33338197. S2CID 229323810.
- ^ a b Wang J, Kaperak C, Sato T, Sakuraba A (August 2021). “COVID-19 reinfection: a rapid systematic review of case reports and case series”. Journal of Investigative Medicine. 69 (6): 1253–1255. doi:10.1136/jim-2021-001853. ISSN 1081-5589. PMID 34006572. S2CID 234773697.
- ^ Centers for Disease Control and Prevention (May 2012). “Lesson 3: Measures of Risk Section 3: Mortality Frequency Measures”. Principles of Epidemiology in Public Health Practice (Third ed.). U.S. Centers for Disease Control and Prevention (CDC). No. SS1978. Archived from the original on 28 February 2020. Retrieved 28 March 2020.
- ^ Ritchie H, Roser M (25 March 2020). Chivers T (ed.). “What do we know about the risk of dying from COVID-19?”. Our World in Data. Archived from the original on 28 March 2020. Retrieved 28 March 2020.
- ^ Castagnoli R, Votto M, Licari A, Brambilla I, Bruno R, Perlini S, et al. (September 2020). “Severe Acute Respiratory Syndrome Coronavirus 2 (SARS-CoV-2) Infection in Children and Adolescents: A Systematic Review”. JAMA Pediatrics. 174 (9): 882–889. doi:10.1001/jamapediatrics.2020.1467. PMID 32320004.
- ^ Lu X, Zhang L, Du H, Zhang J, Li YY, Qu J, et al. (April 2020). “SARS-CoV-2 Infection in Children”. The New England Journal of Medicine. Massachusetts Medical Society. 382 (17): 1663–1665. doi:10.1056/nejmc2005073. PMC 7121177. PMID 32187458.
- ^ Dong Y, Mo X, Hu Y, Qi X, Jiang F, Jiang Z, Tong S (June 2020). “Epidemiology of COVID-19 Among Children in China”. Pediatrics. 145 (6): e20200702. doi:10.1542/peds.2020-0702. PMID 32179660. S2CID 219118986.
- ^ a b c d Dehingia N (2021). “Sex differences in COVID-19 case fatality: do we know enough?”. The Lancet. Global Health. 9 (1): e14–e15. doi:10.1016/S2214-109X(20)30464-2. PMC 7834645. PMID 33160453.
- ^ Lazzerini M, Putoto G (May 2020). “COVID-19 in Italy: momentous decisions and many uncertainties”. The Lancet. Global Health. 8 (5): e641–e642. doi:10.1016/S2214-109X(20)30110-8. PMC 7104294. PMID 32199072.
- ^ Ritchie H, Ortiz-Ospina E, Beltekian D, Mathieu E, Hasell J, MacDonald B, et al. (5 March 2020). “What do we know about the risk of dying from COVID-19?”. Our World in Data. Archived from the original on 28 March 2020. Retrieved 28 March 2020.
- ^ “Total confirmed cases of COVID-19 per million people”. Our World in Data. Archived from the original on 19 March 2020. Retrieved 10 April 2020.[needs update]
- ^ “Cumulative confirmed COVID-19 deaths per million people”. Our World in Data.
- ^ Mallapaty S (June 2020). “How deadly is the coronavirus? Scientists are close to an answer”. Nature. 582 (7813): 467–468. Bibcode:2020Natur.582..467M. doi:10.1038/d41586-020-01738-2. PMID 32546810. S2CID 219726496.
- ^ Alwan NA, Burgess RA, Ashworth S, Beale R, Bhadelia N, Bogaert D, et al. (October 2020). “Scientific consensus on the COVID-19 pandemic: we need to act now”. Lancet. 396 (10260): e71–e72. doi:10.1016/S0140-6736(20)32153-X. PMC 7557300. PMID 33069277.
- ^ Meyerowitz-Katz G, Merone L (December 2020). “A systematic review and meta-analysis of published research data on COVID-19 infection fatality rates”. International Journal of Infectious Diseases. 101: 138–148. doi:10.1016/j.ijid.2020.09.1464. PMC 7524446. PMID 33007452.
- ^ Zhang D, Hu M, Ji Q (October 2020). “Financial markets under the global pandemic of COVID-19”. Finance Research Letters. 36: 101528. Bibcode:2020CSFX….500043D. doi:10.1016/j.csfx.2020.100043. PMC 7402242. PMID 32837360.
- ^ a b c d e Levin AT, Hanage WP, Owusu-Boaitey N, Cochran KB, Walsh SP, Meyerowitz-Katz G (December 2020). “Assessing the age specificity of infection fatality rates for COVID-19: systematic review, meta-analysis, and public policy implications”. European Journal of Epidemiology. 35 (12): 1123–1138. doi:10.1007/s10654-020-00698-1. PMC 7721859. PMID 33289900.
![CC-BY icon.svg]() Text was copied from this source, which is available under a Creative Commons Attribution 4.0 International License.
Text was copied from this source, which is available under a Creative Commons Attribution 4.0 International License. - ^ World Health Organization (22 December 2020). “Background paper on Covid-19 disease and vaccines: prepared by the Strategic Advisory Group of Experts (SAGE) on immunization working group on COVID-19 vaccines”. World Health Organization. hdl:10665/338095.
- ^ “Coronavirus disease 2019 (COVID-19) Situation Report – 30” (PDF). 19 February 2020. Retrieved 3 June 2020.
- ^ “Coronavirus disease 2019 (COVID-19) Situation Report – 31” (PDF). 20 February 2020. Retrieved 23 April 2020.
- ^ McNeil Jr DG (4 July 2020). “The Pandemic’s Big Mystery: How Deadly Is the Coronavirus? – Even with more than 500,000 dead worldwide, scientists are struggling to learn how often the virus kills. Here’s why”. The New York Times. Archived from the original on 4 July 2020. Retrieved 6 July 2020.
- ^ “Global Research and Innovation Forum on COVID-19: Virtual Press Conference” (PDF). World Health Organization. 2 July 2020.
- ^ “Estimating mortality from COVID-19”. World Health Organization (WHO). Retrieved 21 September 2020.
- ^ Shaffer C (23 October 2021). “Covid-19 still rife in Iran”. New Scientist. 252 (3357): 10–11. Bibcode:2021NewSc.252…10S. doi:10.1016/S0262-4079(21)01865-0. ISSN 0262-4079. PMC 8536311. PMID 34720322.
- ^ “COVID-19: Data”. City of New York.
- ^ Wilson L (May 2020). “SARS-CoV-2, COVID-19, Infection Fatality Rate (IFR) Implied by the Serology, Antibody, Testing in New York City”. SSRN 3590771.
- ^ Yang W, Kandula S, Huynh M, Greene SK, Van Wye G, Li W, et al. (February 2021). “Estimating the infection-fatality risk of SARS-CoV-2 in New York City during the spring 2020 pandemic wave: a model-based analysis”. The Lancet. Infectious Diseases. 21 (2): 203–212. doi:10.1016/s1473-3099(20)30769-6. PMC 7572090. PMID 33091374.
- ^ Modi C (21 April 2020). “How deadly is COVID-19? Data Science offers answers from Italy mortality data”. Medium. Retrieved 23 April 2020.
- ^ “Coronavirus Disease 2019 (COVID-19)”. U.S. Centers for Disease Control and Prevention (CDC). 10 September 2020. Retrieved 9 December 2020.
- ^ Salje H, Tran Kiem C, Lefrancq N, Courtejoie N, Bosetti P, Paireau J, et al. (July 2020). “Estimating the burden of SARS-CoV-2 in France”. Science. 369 (6500): 208–211. Bibcode:2020Sci…369..208S. doi:10.1126/science.abc3517. PMC 7223792. PMID 32404476.
- ^ McIntosh K (April 2021). “Covid 19 Clinical Features”. UpToDate. Retrieved 12 May 2021.
- ^ Peckham H, de Gruijter NM, Raine C, Radziszewska A, Ciurtin C, Wedderburn LR, et al. (December 2020). “Male sex identified by global COVID-19 meta-analysis as a risk factor for death and ITU admission”. Nature Communications. 11 (1): 6317. Bibcode:2020NatCo..11.6317P. doi:10.1038/s41467-020-19741-6. PMC 7726563. PMID 33298944.
- ^ Abate BB, Kassie AM, Kassaw MW, Aragie TG, Masresha SA (October 2020). “Sex difference in coronavirus disease (COVID-19): a systematic review and meta-analysis”. BMJ Open. 10 (10): e040129. doi:10.1136/bmjopen-2020-040129. PMC 7539579. PMID 33028563.
- ^ “The Epidemiological Characteristics of an Outbreak of 2019 Novel Coronavirus Diseases (COVID-19)”. China CDC Weekly. 2 (8): 113–122. February 2020. doi:10.46234/ccdcw2020.032. ISSN 2096-7071. Retrieved 15 June 2020.
- ^ Hu Y, Sun J, Dai Z, Deng H, Li X, Huang Q, et al. (June 2020). “Prevalence and severity of corona virus disease 2019 (COVID-19): A systematic review and meta-analysis”. Journal of Clinical Virology. 127: 104371. doi:10.1016/j.jcv.2020.104371. PMC 7195434. PMID 32315817.
- ^ Fu L, Wang B, Yuan T, Chen X, Ao Y, Fitzpatrick T, et al. (June 2020). “Clinical characteristics of coronavirus disease 2019 (COVID-19) in China: A systematic review and meta-analysis”. The Journal of Infection. 80 (6): 656–665. doi:10.1016/j.jinf.2020.03.041. PMC 7151416. PMID 32283155.
- ^ Yuki K, Fujiogi M, Koutsogiannaki S (June 2020). “COVID-19 pathophysiology: A review”. Clinical Immunology. 215: 108427. doi:10.1016/j.clim.2020.108427. PMC 7169933. PMID 32325252. S2CID 216028003.
- ^ Rabin RC (20 March 2020). “In Italy, Coronavirus Takes a Higher Toll on Men”. The New York Times. Archived from the original on 20 March 2020. Retrieved 7 April 2020.
- ^ “COVID-19 weekly surveillance report”. World Health Organization (WHO). Archived from the original on 15 March 2020. Retrieved 7 April 2020.
- ^ a b Gupta AH (3 April 2020). “Does Covid-19 Hit Women and Men Differently? U.S. Isn’t Keeping Track”. The New York Times. Archived from the original on 3 April 2020. Retrieved 7 April 2020.
- ^ a b Dorn AV, Cooney RE, Sabin ML (April 2020). “COVID-19 exacerbating inequalities in the US”. Lancet. 395 (10232): 1243–1244. doi:10.1016/S0140-6736(20)30893-X. PMC 7162639. PMID 32305087.
- ^ Adams ML, Katz DL, Grandpre J (August 2020). “Population-Based Estimates of Chronic Conditions Affecting Risk for Complications from Coronavirus Disease, United States”. Emerging Infectious Diseases. 26 (8): 1831–1833. doi:10.3201/eid2608.200679. PMC 7392427. PMID 32324118.
- ^ Batthyány K (13 October 2020). “Coronavirus y Desigualdades preexistentes: Género y Cuidados”. CLACSO (Consejo Latinoamericano de Ciencias Sociales). Retrieved 22 April 2021.
- ^ “COVID-19 Presents Significant Risks for American Indian and Alaska Native People”. 14 May 2020.
- ^ “COVID-19 Presents Significant Risks for American Indian and Alaska Native People”. 14 May 2020.
- ^ Laurencin CT, McClinton A (June 2020). “The COVID-19 Pandemic: a Call to Action to Identify and Address Racial and Ethnic Disparities”. Journal of Racial and Ethnic Health Disparities. 7 (3): 398–402. doi:10.1007/s40615-020-00756-0. PMC 7166096. PMID 32306369.
- ^ “How coronavirus deaths in the UK compare by race and ethnicity”. The Independent. 9 June 2020. Retrieved 10 June 2020.
- ^ “Emerging findings on the impact of COVID-19 on black and minority ethnic people”. The Health Foundation. Retrieved 10 June 2020.
- ^ Butcher B, Massey J (9 June 2020). “Why are more BAME people dying from coronavirus?”. BBC News. Retrieved 10 June 2020.
- ^ a b c “The ancient Neanderthal hand in severe COVID-19”. ScienceDaily. 30 September 2020. Retrieved 13 December 2020.
- ^ “WHO Director-General’s statement on the advice of the IHR Emergency Committee on Novel Coronavirus”. World Health Organization (WHO).
- ^ Garg S, Kim L, Whitaker M, O’Halloran A, Cummings C, Holstein R, et al. (April 2020). “Hospitalization Rates and Characteristics of Patients Hospitalized with Laboratory-Confirmed Coronavirus Disease 2019 – COVID-NET, 14 States, March 1-30, 2020”. MMWR. Morbidity and Mortality Weekly Report. 69 (15): 458–464. doi:10.15585/mmwr.mm6915e3. PMC 7755063. PMID 32298251.
- ^ “Coronavirus Disease 2019 (COVID-19)”. U.S. Centers for Disease Control and Prevention (CDC). 11 February 2020. Retrieved 19 June 2020.
- ^ Zhao Q, Meng M, Kumar R, Wu Y, Huang J, Lian N, et al. (October 2020). “The impact of COPD and smoking history on the severity of COVID-19: A systemic review and meta-analysis”. Journal of Medical Virology. 92 (10): 1915–1921. doi:10.1002/jmv.25889. PMC 7262275. PMID 32293753.
- ^ “Smoking and COVID-19”. World Health Organization (WHO). Retrieved 19 June 2020.
- ^ “Coronavirus Disease 2019 (COVID-19)”. U.S. Centers for Disease Control and Prevention (CDC). 11 February 2020. Retrieved 4 May 2020.
- ^ DeRobertis J (3 May 2020). “People who use drugs are more vulnerable to coronavirus. Here’s what clinics are doing to help”. The Advocate (Louisiana). Retrieved 4 May 2020.
- ^ “Coronavirus Disease 2019 (COVID-19)”. U.S. Centers for Disease Control and Prevention (CDC). 11 February 2020.
- ^ Frutos R, Gavotte L, Devaux CA (November 2021). “Understanding the origin of COVID-19 requires to change the paradigm on zoonotic emergence from the spillover to the circulation model”. Infection, Genetics and Evolution. 95: 104812. doi:10.1016/j.meegid.2021.104812. PMC 7969828. PMID 33744401.
- ^ Holmes EC, Goldstein SA, Rasmussen AL, Robertson DL, Crits-Christoph A, Wertheim JO, et al. (September 2021). “The origins of SARS-CoV-2: A critical review”. Cell. 184 (19): 4848–4856. doi:10.1016/j.cell.2021.08.017. PMC 8373617. PMID 34480864.
- ^ Duarte F (24 February 2020). “As the cases of coronavirus increase in China and around the world, the hunt is on to identify “patient zero””. BBC News. Retrieved 22 March 2020.
- ^ Li X, Zai J, Zhao Q, Nie Q, Li Y, Foley BT, Chaillon A (June 2020). “Evolutionary history, potential intermediate animal host, and cross-species analyses of SARS-CoV-2“. Journal of Medical Virology. 92 (6): 602–611. doi:10.1002/jmv.25731. PMC 7228310. PMID 32104911.
- ^ Andersen KG, Rambaut A, Lipkin WI, Holmes EC, Garry RF (April 2020). “The proximal origin of SARS-CoV-2“. Nature Medicine. 26 (4): 450–452. doi:10.1038/s41591-020-0820-9. PMC 7095063. PMID 32284615.
- ^ van Dorp L, Acman M, Richard D, Shaw LP, Ford CE, Ormond L, et al. (September 2020). “Emergence of genomic diversity and recurrent mutations in SARS-CoV-2“. Infection, Genetics and Evolution. 83: 104351. doi:10.1016/j.meegid.2020.104351. PMC 7199730. PMID 32387564.
- ^ Grose TK (13 May 2020). “Did the Coronavirus Originate Outside of Wuhan?”. U.S. News & World Report.
- ^ Shield C (26 March 2020). “Coronavirus: From bats to pangolins, how do viruses reach us?”. Deutsche Welle. Retrieved 1 December 2020.
- ^ “WHO Points To Wildlife Farms In Southern China As Likely Source Of Pandemic”. NPR. 15 March 2021.
- ^ Wolf ZB (25 May 2021). “Analysis: Why scientists are suddenly more interested in the lab-leak theory of Covid’s origin”. CNN. Retrieved 26 May 2021.
- ^ Maxmen A (September 2021). “US COVID origins report: researchers pleased with scientific approach”. Nature. 597 (7875): 159–160. Bibcode:2021Natur.597..159M. doi:10.1038/d41586-021-02366-0. PMID 34465917. S2CID 237373547.
- ^ Wu YC, Chen CS, Chan YJ (March 2020). “The outbreak of COVID-19: An overview”. Journal of the Chinese Medical Association. 83 (3): 217–220. doi:10.1097/JCMA.0000000000000270. PMC 7153464. PMID 32134861.
- ^ Wang C, Horby PW, Hayden FG, Gao GF (February 2020). “A novel coronavirus outbreak of global health concern”. Lancet. 395 (10223): 470–473. doi:10.1016/S0140-6736(20)30185-9. PMC 7135038. PMID 31986257.
- ^ Cohen J (January 2020). “Wuhan seafood market may not be source of novel virus spreading globally”. Science. doi:10.1126/science.abb0611.
- ^ “Novel Coronavirus – China”. World Health Organization (WHO). 12 January 2020. Archived from the original on 14 January 2020.
- ^ Kessler G (17 April 2020). “Trump’s false claim that the WHO said the coronavirus was ‘not communicable'”. The Washington Post. Archived from the original on 17 April 2020. Retrieved 17 April 2020.
- ^ Kuo L (21 January 2020). “China confirms human-to-human transmission of coronavirus”. The Guardian. Retrieved 18 April 2020.
- ^ Epidemiology Working Group For Ncip Epidemic Response; Chinese Center for Disease Control Prevention (February 2020). “[The epidemiological characteristics of an outbreak of 2019 novel coronavirus diseases (COVID-19) in China]”. Zhonghua Liu Xing Bing Xue Za Zhi = Zhonghua Liuxingbingxue Zazhi (in Chinese). 41 (2): 145–151. doi:10.3760/cma.j.issn.0254-6450.2020.02.003. PMID 32064853. S2CID 211133882.
- ^ Areddy JT (26 May 2020). “China Rules Out Animal Market and Lab as Coronavirus Origin”. The Wall Street Journal. Retrieved 29 May 2020.
- ^ Kelland K (19 June 2020). “Italy sewage study suggests COVID-19 was there in December 2019”. Reuters. Retrieved 23 June 2020.
- ^ Yanping Z, et al. (The Novel Coronavirus Pneumonia Emergency Response Epidemiology Team) (February 2020). “The Epidemiological Characteristics of an Outbreak of 2019 Novel Coronavirus Diseases (COVID-19) – China, 2020”. China CDC Weekly. Chinese Center for Disease Control and Prevention. 2 (8): 113–122. doi:10.46234/ccdcw2020.032. PMC 8392929. PMID 34594836. Archived from the original on 19 February 2020. Retrieved 18 March 2020.
- ^ Heymann DL, Shindo N (February 2020). “COVID-19: what is next for public health?”. Lancet. 395 (10224): 542–545. doi:10.1016/S0140-6736(20)30374-3. PMC 7138015. PMID 32061313.
- ^ Bryner J (14 March 2020). “1st known case of coronavirus traced back to November in China”. livescience.com. Retrieved 31 May 2020.
- ^ Canadian Politics (8 April 2020). “The birth of a pandemic: How COVID-19 went from Wuhan to Toronto | National Post”. National Post. Retrieved 31 May 2020.
- ^ 高昱 (26 February 2020). “独家 | 新冠病毒基因测序溯源:警报是何时拉响的” [Exclusive | Tracing the New Coronavirus gene sequencing: when did the alarm sound]. Caixin (in Chinese). Archived from the original on 27 February 2020. Retrieved 1 March 2020.
- ^ 路子康. “最早上报疫情的她,怎样发现这种不一样的肺炎”. 中国网新闻 (in Chinese (China)). 北京. Archived from the original on 2 March 2020. Retrieved 11 February 2020.
- ^ “Undiagnosed pneumonia – China (HU): RFI”. ProMED Mail. ProMED. Retrieved 7 May 2020.
- ^ “‘Hero who told the truth’: Chinese rage over coronavirus death of whistleblower doctor”. The Guardian. 7 February 2020.
- ^ Kuo L (11 March 2020). “Coronavirus: Wuhan doctor speaks out against authorities”. The Guardian. London.
- ^ “Novel Coronavirus”. World Health Organization (WHO). Archived from the original on 2 February 2020. Retrieved 6 February 2020.
- ^ “武汉现不明原因肺炎 官方确认属实:已经做好隔离”. Xinhua Net 新華網. 31 December 2019. Retrieved 31 March 2020.
- ^ 武汉市卫健委关于当前我市肺炎疫情的情况通报. WJW.Wuhan.gov.cn (in Chinese). Wuhan Municipal Health Commission. 31 December 2019. Archived from the original on 9 January 2020. Retrieved 8 February 2020.
- ^ “Mystery pneumonia virus probed in China”. BBC News. 3 January 2020. Archived from the original on 5 January 2020. Retrieved 29 January 2020.
- ^ Li Q, Guan X, Wu P, Wang X, Zhou L, Tong Y, et al. (March 2020). “Early Transmission Dynamics in Wuhan, China, of Novel Coronavirus-Infected Pneumonia”. The New England Journal of Medicine. 382 (13): 1199–1207. doi:10.1056/NEJMoa2001316. PMC 7121484. PMID 31995857.
- ^ “China confirms sharp rise in cases of SARS-like virus across the country”. 20 January 2020. Archived from the original on 20 January 2020. Retrieved 20 January 2020.
- ^ The Novel Coronavirus Pneumonia Emergency Response Epidemiology Team (February 2020). “The Epidemiological Characteristics of an Outbreak of 2019 Novel Coronavirus Diseases (COVID-19) – China, 2020”. China CDC Weekly. 2 (8): 113–122. doi:10.46234/ccdcw2020.032. PMC 8392929. PMID 34594836. Retrieved 18 March 2020.
- ^ a b “Flattery and foot dragging: China’s influence over the WHO under scrutiny”. The Globe and Mail. 25 April 2020.
- ^ Horton R (18 March 2020). “Scientists have been sounding the alarm on coronavirus for months. Why did Britain fail to act?”. The Guardian. Retrieved 23 April 2020.
- ^ “China delayed releasing coronavirus info, frustrating WHO”. Associated Press. 2 June 2020. Retrieved 3 June 2020.
- ^ “Coronavirus: Primi due casi in Italia” [Coronavirus: First two cases in Italy]. Corriere della sera (in Italian). 31 January 2020. Retrieved 31 January 2020.
- ^ “Coronavirus: Number of COVID-19 deaths in Italy surpasses China as total reaches 3,405”. Sky News. Retrieved 7 May 2020.
- ^ McNeil Jr DG (26 March 2020). “The U.S. Now Leads the World in Confirmed Coronavirus Cases”. The New York Times. Archived from the original on 26 March 2020. Retrieved 27 March 2020.
- ^ “Studies Show N.Y. Outbreak Originated in Europe”. The New York Times. 8 April 2020. Archived from the original on 8 April 2020.
- ^ Irish J (4 May 2020). Lough RM, Graff P (eds.). “After retesting samples, French hospital discovers COVID-19 case from December”. Reuters. Retrieved 4 May 2020.
- ^ Deslandes A, Berti V, Tandjaoui-Lambotte Y, Alloui C, Carbonnelle E, Zahar JR, et al. (June 2020). “SARS-CoV-2 was already spreading in France in late December 2019″. International Journal of Antimicrobial Agents. 55 (6): 106006. doi:10.1016/j.ijantimicag.2020.106006. PMC 7196402. PMID 32371096.
- ^ “2 died with coronavirus weeks before 1st U.S. virus death”. PBS NewsHour. 22 April 2020. Retrieved 23 April 2020.
- ^ Michael-Kordatou I, Karaolia P, Fatta-Kassinos D (October 2020). “Sewage analysis as a tool for the COVID-19 pandemic response and management: the urgent need for optimised protocols for SARS-CoV-2 detection and quantification”. Journal of Environmental Chemical Engineering. 8 (5): 104306. doi:10.1016/j.jece.2020.104306. PMC 7384408. PMID 32834990.
- ^ Platto S, Xue T, Carafoli E (September 2020). “COVID19: an announced pandemic”. Cell Death & Disease. 11 (9): 799. doi:10.1038/s41419-020-02995-9. PMC 7513903. PMID 32973152.
- ^ Kavya B, Abraham R (3 October 2021). Shumaker L, Wardell J (eds.). “Global COVID-19 deaths hit 5 million as Delta variant sweeps the world”. Reuters – via www.reuters.com.
- ^ “China coronavirus: Misinformation spreads online about origin and scale”. BBC News. 30 January 2020. Archived from the original on 4 February 2020. Retrieved 10 February 2020.
- ^ Taylor J (31 January 2020). “Bat soup, dodgy cures and ‘diseasology’: the spread of coronavirus misinformation”. The Guardian. Archived from the original on 2 February 2020. Retrieved 3 February 2020.
- ^ “Here’s A Running List Of Disinformation Spreading About The Coronavirus”. Buzzfeed News. Archived from the original on 6 February 2020. Retrieved 8 February 2020.
- ^ “Coronavirus Disease 2019 (COVID-19)”. U.S. Centers for Disease Control and Prevention (CDC). 11 February 2020. Retrieved 10 October 2020.
- ^ “Misleading claim circulates online about infection fatality ratio of Covid-19 in the US”. Fact Check. 8 October 2020. Retrieved 10 October 2020.
- ^ a b c d Kampf G, Brüggemann Y, Kaba HE, Steinmann J, Pfaender S, Scheithauer S, Steinmann E (December 2020). “Potential sources, modes of transmission and effectiveness of prevention measures against SARS-CoV-2“. The Journal of Hospital Infection. 106 (4): 678–697. doi:10.1016/j.jhin.2020.09.022. PMC 7500278. PMID 32956786.
- ^ Shi J, Wen Z, Zhong G, Yang H, Wang C, Huang B, et al. (May 2020). “Susceptibility of ferrets, cats, dogs, and other domesticated animals to SARS-coronavirus 2”. Science. 368 (6494): 1016–1020. doi:10.1126/science.abb7015. PMC 7164390. PMID 32269068.
- ^ a b c d e f g h Salajegheh Tazerji S, Magalhães Duarte P, Rahimi P, Shahabinejad F, Dhakal S, Singh Malik Y, et al. (September 2020). “Transmission of severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2) to animals: an updated review”. Journal of Translational Medicine. 18 (1): 358. doi:10.1186/s12967-020-02534-2. PMC 7503431. PMID 32957995.
- ^ a b c Gorman J (22 January 2021). “The Coronavirus Kills Mink, So They Too May Get a Vaccine”. The New York Times. ISSN 0362-4331. Archived from the original on 28 December 2021. Retrieved 24 February 2021.
- ^ Dhama K, Sharun K, Tiwari R, Dadar M, Malik YS, Singh KP, Chaicumpa W (June 2020). “COVID-19, an emerging coronavirus infection: advances and prospects in designing and developing vaccines, immunotherapeutics, and therapeutics”. Human Vaccines & Immunotherapeutics. 16 (6): 1232–1238. doi:10.1080/21645515.2020.1735227. PMC 7103671. PMID 32186952.
- ^ Zhang L, Liu Y (May 2020). “Potential interventions for novel coronavirus in China: A systematic review”. Journal of Medical Virology. 92 (5): 479–490. doi:10.1002/jmv.25707. PMC 7166986. PMID 32052466.
- ^ “Interim Laboratory Biosafety Guidelines for Handling and Processing Specimens Associated with Coronavirus Disease 2019 (COVID-19)”. Coronavirus Disease 2019 (COVID-19) Lab Biosafety Guidelines. U.S. Centers for Disease Control and Prevention (CDC). 11 February 2020. Retrieved 1 April 2020.
- ^ Aristovnik A, Ravšelj D, Umek L (November 2020). “A Bibliometric Analysis of COVID-19 across Science and Social Science Research Landscape”. Sustainability. 12 (21): 9132. doi:10.3390/su12219132.
- ^ Kupferschmidt, Kai (3 December 2020). “First-of-its-kind African trial tests common drugs to prevent severe COVID-19”. Science. doi:10.1126/science.abf9987. Retrieved 8 March 2022.
- ^ Reardon S (13 November 2020). “For COVID Drugs, Months of Frantic Development Lead to Few Outright Successes”. Scientific American. Retrieved 10 December 2020.
- ^ Kucharski AJ, Russell TW, Diamond C, Liu Y, Edmunds J, Funk S, Eggo RM (May 2020). “Early dynamics of transmission and control of COVID-19: a mathematical modelling study”. The Lancet. Infectious Diseases. 20 (5): 553–558. doi:10.1016/S1473-3099(20)30144-4. PMC 7158569. PMID 32171059.
- ^ “Update to living systematic review on prediction models for diagnosis and prognosis of covid-19”. BMJ (Clinical Research Ed.). 372: n236. 3 February 2021. doi:10.1136/bmj.n236. ISSN 1756-1833. PMID 33536183. S2CID 231775762.
- ^ Giordano G, Blanchini F, Bruno R, Colaneri P, Di Filippo A, Di Matteo A, Colaneri M (June 2020). “Modelling the COVID-19 epidemic and implementation of population-wide interventions in Italy”. Nature Medicine. 26 (6): 855–860. arXiv:2003.09861. doi:10.1038/s41591-020-0883-7. PMC 7175834. PMID 32322102.
- ^ Prem K, Liu Y, Russell TW, Kucharski AJ, Eggo RM, Davies N, et al. (May 2020). “The effect of control strategies to reduce social mixing on outcomes of the COVID-19 epidemic in Wuhan, China: a modelling study”. The Lancet. Public Health. 5 (5): e261–e270. doi:10.1016/S2468-2667(20)30073-6. PMC 7158905. PMID 32220655.
- ^ Emanuel EJ, Persad G, Upshur R, Thome B, Parker M, Glickman A, et al. (May 2020). “Fair Allocation of Scarce Medical Resources in the Time of Covid-19”. The New England Journal of Medicine. 382 (21): 2049–2055. doi:10.1056/NEJMsb2005114. PMID 32202722.
- ^ Kermack WO, McKendrick AG (1927). “A contribution to the mathematical theory of epidemics”. Proceedings of the Royal Society of London. Series A, Containing Papers of a Mathematical and Physical Character. 115 (772): 700–721. Bibcode:1927RSPSA.115..700K. doi:10.1098/rspa.1927.0118.
- ^ Mittal R, Ni R, Seo JH (2020). “The flow physics of COVID-19”. Journal of Fluid Mechanics. 894: –2. arXiv:2004.09354. Bibcode:2020JFM…894F…2M. doi:10.1017/jfm.2020.330.
- ^ Ronchi E, Lovreglio R (October 2020). “EXPOSED: An occupant exposure model for confined spaces to retrofit crowd models during a pandemic”. Safety Science. 130: 104834. arXiv:2005.04007. doi:10.1016/j.ssci.2020.104834. PMC 7373681. PMID 32834509.
- ^ Badr HS, Du H, Marshall M, Dong E, Squire MM, Gardner LM (November 2020). “Association between mobility patterns and COVID-19 transmission in the USA: a mathematical modelling study”. The Lancet Infectious Diseases. 20 (11): 1247–1254. doi:10.1016/S1473-3099(20)30553-3. PMC 7329287. PMID 32621869.
- ^ McKibbin W, Roshen F (2020). “The global macroeconomic impacts of COVID-19: Seven scenarios” (PDF). CAMA Working Paper. doi:10.2139/ssrn.3547729. S2CID 216307705.
- ^ Bundy J, Pfarrer MD, Short CE, Coombs WT (July 2017). “Crises and crisis management: Integration, interpretation, and research development”. Journal of Management. 43 (6): 1661–92. doi:10.1177/0149206316680030. S2CID 152223772.
- ^ Kraus S, Clauss T, Breier M, Gast J, Zardini A, Tiberius V (2020). “The economics of COVID-19: initial empirical evidence on how family firms in five European countries cope with the corona crisis”. International Journal of Entrepreneurial Behavior & Research. 26 (5): 1067–1092. doi:10.1108/IJEBR-04-2020-0214. ISSN 1355-2554. S2CID 219144929.
- ^ “COVID-19 treatment and vaccine tracker” (PDF). Milken Institute. 21 April 2020. Retrieved 21 April 2020.
- ^ a b Koch S, Pong W (13 March 2020). “First up for COVID-19: nearly 30 clinical readouts before end of April”. BioCentury Inc. Retrieved 1 April 2020.
- ^ Kupferschmidt K, Cohen J (March 2020). “WHO launches global megatrial of the four most promising coronavirus treatments”. Science. doi:10.1126/science.abb8497.
- ^ “UN health chief announces global ‘solidarity trial’ to jumpstart search for COVID-19 treatment”. UN News. 18 March 2020. Archived from the original on 23 March 2020. Retrieved 23 March 2020.
- ^ “Citing safety concerns, the W.H.O. paused tests of a drug Trump said he had taken”. The New York Times. 26 May 2020. Archived from the original on 26 May 2020.
- ^ “Hydroxychloroquine does not benefit adults hospitalized with COVID-19”. National Institutes of Health (NIH) (Press release). 9 November 2020. Retrieved 9 November 2020.
![Public Domain]() This article incorporates text from this source, which is in the public domain .
This article incorporates text from this source, which is in the public domain . - ^ “Coronavirus (COVID-19) Update: FDA Warns of Newly Discovered Potential Drug Interaction That May Reduce Effectiveness of a COVID-19 Treatment Authorized for Emergency Use”. U.S. Food and Drug Administration (FDA) (Press release). 15 June 2020. Retrieved 15 June 2020.
![Public Domain]() This article incorporates text from this source, which is in the public domain .
This article incorporates text from this source, which is in the public domain . - ^ “France bans use of hydroxychloroquine, drug touted by Trump, in coronavirus patients”. CBS News. 27 May 2020.
- ^ Boseley S (16 June 202). “Recovery trial for Covid-19 treatments: what we know so far”. The Guardian. Retrieved 21 June 2020.
- ^ “WHO welcomes preliminary results about dexamethasone use in treating critically ill COVID-19 patients”. World Health Organization (WHO) (Press release). 16 June 2020. Retrieved 21 June 2020.
- ^ “Q&A: Dexamethasone and COVID-19”. World Health Organization (WHO) (Press release). Retrieved 12 July 2020.
- ^ “Corticosteroids”. COVID-19 Treatment Guidelines. National Institutes of Health. Retrieved 12 July 2020.
- ^ a b c World Health Organization (2020). Corticosteroids for COVID-19: living guidance, 2 September 2020 (Report). hdl:10665/334125. WHO/2019-nCoV/Corticosteroids/2020.1.
- ^ “WHO updates clinical care guidance with corticosteroid recommendations”. World Health Organization (WHO). Retrieved 25 January 2022.
- ^ Sterne JA, Murthy S, Diaz JV, Slutsky AS, Villar J, Angus DC, et al. (The WHO Rapid Evidence Appraisal for COVID-19 Therapies (REACT) Working Group) (October 2020). “Association Between Administration of Systemic Corticosteroids and Mortality Among Critically Ill Patients With COVID-19: A Meta-analysis”. JAMA. 324 (13): 1330–1341. doi:10.1001/jama.2020.17023. PMC 7489434. PMID 32876694. S2CID 221467783.
- ^ Prescott HC, Rice TW (October 2020). “Corticosteroids in COVID-19 ARDS: Evidence and Hope During the Pandemic”. JAMA. 324 (13): 1292–1295. doi:10.1001/jama.2020.16747. PMID 32876693. S2CID 221468015.
- ^ a b “EMA endorses use of dexamethasone in COVID-19 patients on oxygen or mechanical ventilation”. European Medicines Agency (EMA) (Press release). 18 September 2020. Retrieved 21 September 2020. Text was copied from this source which is European Medicines Agency. Reproduction is authorized provided the source is acknowledged.
- ^ Dexamethasone in hospitalised patients with COVID-19 (PDF) (Report). European Medicines Agency. 17 September 2020.
- ^ a b c “Coronavirus (COVID-19) Update: FDA Authorizes Monoclonal Antibody for Treatment of COVID-19”. U.S. Food and Drug Administration (FDA) (Press release). 9 November 2020. Retrieved 9 November 2020.
![Public Domain]() This article incorporates text from this source, which is in the public domain .
This article incorporates text from this source, which is in the public domain . - ^ “FDA Authorizes Monoclonal Antibodies for Treatment of COVID-19”. U.S. Food and Drug Administration (FDA) (Press release). 10 February 2021. Retrieved 9 February 2021.
![Public Domain]() This article incorporates text from this source, which is in the public domain .
This article incorporates text from this source, which is in the public domain . - ^ “Coronavirus (COVID-19) Update: FDA Revokes Emergency Use Authorization for Monoclonal Antibody Bamlanivimab”. U.S. Food and Drug Administration (FDA) (Press release). 16 April 2021. Retrieved 16 April 2021.
![Public Domain]() This article incorporates text from this source, which is in the public domain .
This article incorporates text from this source, which is in the public domain . - ^ Li X, Geng M, Peng Y, Meng L, Lu S (April 2020). “Molecular immune pathogenesis and diagnosis of COVID-19”. Journal of Pharmaceutical Analysis. 10 (2): 102–108. doi:10.1016/j.jpha.2020.03.001. PMC 7104082. PMID 32282863.
- ^ Zhao Z, Wei Y, Tao C (January 2021). “An enlightening role for cytokine storm in coronavirus infection”. Clinical Immunology. 222: 108615. doi:10.1016/j.clim.2020.108615. PMC 7583583. PMID 33203513.
- ^ Liu R, Miller J (3 March 2020). “China approves use of Roche drug in battle against coronavirus complications”. Reuters. Archived from the original on 12 March 2020. Retrieved 14 March 2020.
- ^ Xu X, Han M, Li T, Sun W, Wang D, Fu B, et al. (May 2020). “Effective treatment of severe COVID-19 patients with tocilizumab”. Proceedings of the National Academy of Sciences of the United States of America. 117 (20): 10970–10975. doi:10.1073/pnas.2005615117. PMC 7245089. PMID 32350134.
- ^ Ovadia D, Agenzia Z. “COVID-19 – Italy launches an independent trial on tocilizumab”. Univadis from Medscape. Aptus Health. Retrieved 22 April 2020.
- ^ “Tocilizumab in COVID-19 Pneumonia (TOCIVID-19) (TOCIVID-19)”. clinicaltrials.gov. Retrieved 22 April 2020.
- ^ Various sources:
- “How doctors can potentially significantly reduce the number of deaths from Covid-19”. Vox. 12 March 2020. Archived from the original on 19 March 2020. Retrieved 14 March 2020.
- Ruan Q, Yang K, Wang W, Jiang L, Song J (May 2020). “Clinical predictors of mortality due to COVID-19 based on an analysis of data of 150 patients from Wuhan, China”. Intensive Care Medicine. 46 (5): 846–848. doi:10.1007/s00134-020-05991-x. PMC 7080116. PMID 32125452.
- Mehta P, McAuley DF, Brown M, Sanchez E, Tattersall RS, Manson JJ (March 2020). “COVID-19: consider cytokine storm syndromes and immunosuppression”. Lancet. 395 (10229): 1033–1034. doi:10.1016/S0140-6736(20)30628-0. PMC 7270045. PMID 32192578.
- ^ Slater H (26 March 2020). “FDA Approves Phase III Clinical Trial of Tocilizumab for COVID-19 Pneumonia”. cancernetwork.com. Cancer Network. Retrieved 22 April 2020.
- ^ Locke FL, Neelapu SS, Bartlett NL, Lekakis LJ, Jacobson CA, Braunschweig I, et al. (2017). “Preliminary Results of Prophylactic Tocilizumab after Axicabtageneciloleucel (axi-cel; KTE-C19) Treatment for Patients with Refractory, Aggressive Non-Hodgkin Lymphoma (NHL)”. Blood. 130 (Supplement 1): 1547. doi:10.1182/blood.V130.Suppl_1.1547.1547 (inactive 28 February 2022).{{cite journal}}: CS1 maint: DOI inactive as of February 2022 (link)
- ^ Sterner RM, Sakemura R, Cox MJ, Yang N, Khadka RH, Forsman CL, et al. (February 2019). “GM-CSF inhibition reduces cytokine release syndrome and neuroinflammation but enhances CAR T cell function in xenografts”. Blood. 133 (7): 697–709. doi:10.1182/blood-2018-10-881722. PMC 6376281. PMID 30463995.
- ^ a b c d e Casadevall A, Pirofski LA (April 2020). “The convalescent sera option for containing COVID-19”. The Journal of Clinical Investigation. 130 (4): 1545–1548. doi:10.1172/JCI138003. PMC 7108922. PMID 32167489.
- ^ a b c Piechotta V, Iannizzi C, Chai KL, Valk SJ, Kimber C, Dorando E, et al. (May 2021). “Convalescent plasma or hyperimmune immunoglobulin for people with COVID-19: a living systematic review”. The Cochrane Database of Systematic Reviews. 2021 (5): CD013600. doi:10.1002/14651858.CD013600.pub4. PMC 8135693. PMID 34013969.
- ^ a b Ho M (April 2020). “Perspectives on the development of neutralizing antibodies against SARS-CoV-2“. Antibody Therapeutics. 3 (2): 109–114. doi:10.1093/abt/tbaa009. PMC 7291920. PMID 32566896.
- ^ Yang L, Liu W, Yu X, Wu M, Reichert JM, Ho M (July 2020). “COVID-19 antibody therapeutics tracker: a global online database of antibody therapeutics for the prevention and treatment of COVID-19”. Antibody Therapeutics. 3 (3): 205–212. doi:10.1093/abt/tbaa020. PMC 7454247. PMID 33215063.
- ^ Maccaro A, Piaggio D, Pagliara S, Pecchia L (June 2021). “The role of ethics in science: a systematic literature review from the first wave of COVID-19”. Health and Technology. 11 (5): 1063–1071. doi:10.1007/s12553-021-00570-6. ISSN 2190-7188. PMC 8175060. PMID 34104626.
- ^ McGuire AL, Aulisio MP, Davis FD, Erwin C, Harter TD, Jagsi R, et al. (July 2020). “Ethical Challenges Arising in the COVID-19 Pandemic: An Overview from the Association of Bioethics Program Directors (ABPD) Task Force”. The American Journal of Bioethics. 20 (7): 15–27. doi:10.1080/15265161.2020.1764138. PMID 32511078. S2CID 219552665.
- ^ Wenham C, Smith J, Morgan R (March 2020). “COVID-19: the gendered impacts of the outbreak”. Lancet. 395 (10227): 846–848. doi:10.1016/S0140-6736(20)30526-2. PMC 7124625. PMID 32151325.
- ^ Tolchin B, Hull SC, Kraschel K (October 2020). “Triage and justice in an unjust pandemic: ethical allocation of scarce medical resources in the setting of racial and socioeconomic disparities”. Journal of Medical Ethics. 47 (3): 200–202. doi:10.1136/medethics-2020-106457. PMID 33067315. S2CID 223558059.
- ^ Sabatello M, Burke TB, McDonald KE, Appelbaum PS (October 2020). “Disability, Ethics, and Health Care in the COVID-19 Pandemic”. American Journal of Public Health. 110 (10): 1523–1527. doi:10.2105/AJPH.2020.305837. PMC 7483109. PMID 32816541.
- ^ Chin T, Kahn R, Li R, Chen JT, Krieger N, Buckee CO, et al. (September 2020). “US-county level variation in intersecting individual, household and community characteristics relevant to COVID-19 and planning an equitable response: a cross-sectional analysis”. BMJ Open. 10 (9): e039886. doi:10.1136/bmjopen-2020-039886. PMC 7467554. PMID 32873684.
- ^ Elgar FJ, Stefaniak A, Wohl MJ (October 2020). “The trouble with trust: Time-series analysis of social capital, income inequality, and COVID-19 deaths in 84 countries”. Social Science & Medicine. 263: 113365. doi:10.1016/j.socscimed.2020.113365. PMC 7492158. PMID 32981770.
- ^ Uttley H (2 March 2021). “Pandemic sends demand for cold and flu remedies to record low”. The Telegraph. Archived from the original on 10 January 2022. Retrieved 28 March 2021.
Further reading
- Erola Pairo-Castineira; Sara Clohisey; Lucija Klarić; et al. (11 December 2020). “Genetic mechanisms of critical illness in Covid-19”. Nature. doi:10.1038/S41586-020-03065-Y. ISSN 1476-4687. PMID 33307546. Wikidata Q104287299. Scholia Q104287299.
- “Progress report on the coronavirus pandemic”. Nature. 584 (7821): 325. 1 August 2020. doi:10.1038/D41586-020-02414-1. ISSN 1476-4687. PMID 32814893. Wikidata Q98568681.
- COVID-19 infection prevention and control measures for primary care, including general practitioner practices, dental clinics and pharmacy settings: first update. European Centre for Disease Prevention and Control (ECDC) (Report). October 2020.
External links
| Scholia has a profile for COVID-19 (Q84263196). |
Health agencies
- Coronavirus disease (COVID‐19) Facts by the World Health Organization (WHO)
- Coronavirus 2019 (COVID-19) by the US Centers for Disease Control and Prevention (CDC)
- Coronavirus (COVID‐19) by the UK National Health Service (NHS)
Directories
- Coronavirus Resource Center at the Center for Inquiry
- COVID-19 at Curlie
- COVID‐19 Resource Directory on OpenMD
- COVID‐19 Information on FireMountain.net
Medical journals
- Coronavirus Disease 2019 (COVID‐19) by JAMA
- BMJ’s Coronavirus (covid‐19) Hub by the BMJ
- Novel Coronavirus Information Center by Elsevier
- COVID‐19 Resource Centre by The Lancet
- Coronavirus (COVID‐19) Research Highlights by Springer Nature
- Coronavirus (Covid‐19) by The New England Journal of Medicine
- Covid‐19: Novel Coronavirus by Wiley Publishing
Treatment guidelines
- “JHMI Clinical Recommendations for Available Pharmacologic Therapies for COVID-19” (PDF). Johns Hopkins Medicine.
- “Bouncing Back From COVID-19: Your Guide to Restoring Movement” (PDF). Johns Hopkins Medicine.
- “Guidelines on the Treatment and Management of Patients with COVID-19”. Infectious Diseases Society of America.
- “Coronavirus Disease 2019 (COVID-19) Treatment Guidelines” (PDF). National Institutes of Health.
- World Health Organization (2022). Therapeutics and COVID-19: living guideline, 14 January 2022 (Report). hdl:10665/351006. WHO/2019-nCoV/therapeutics/2022.1.
- NHS England and NHS Improvement. National Guidance for post-COVID syndrome assessment clinics (Report).
Portals: ![]() Medicine
Medicine ![]() Viruses COVID-19 at Wikipedia’s sister projects:
Viruses COVID-19 at Wikipedia’s sister projects: ![]() Media from Commons
Media from Commons ![]() News from Wikinews
News from Wikinews ![]() Quotations from Wikiquote
Quotations from Wikiquote ![]() Resources from Wikiversity
Resources from Wikiversity ![]() Data from Wikidata
Data from Wikidata