Syndromes d’Ehlers-Danlos
Les syndromes d’Ehlers-Danlos (EDS) sont un groupe de treize troubles génétiques du tissu conjonctif qui figurent dans la classification actuelle, avec un quatorzième type découvert en 2018. [1] Les symptômes peuvent inclure des articulations lâches , des douleurs articulaires , une peau veloutée extensible et des anomalies formation de cicatrice . [1] Ceux-ci peuvent être remarqués à la naissance ou dans la petite enfance. [2] Les complications peuvent inclure une dissection aortique , des dislocations articulaires , une scoliose , des douleurs chroniques ou une arthrose précoce . [1] [3]
| Syndromes d’Ehlers-Danlos (EDS) | |
|---|---|
 |
|
| Individu avec EDS affichant une hyperélasticité cutanée | |
| Prononciation |
|
| Spécialité | Génétique médicale , rhumatologie |
| Les symptômes | Articulations trop flexibles, peau qui s’étire, formation anormale de cicatrices [1] |
| Complications | Dissection aortique , Luxations articulaires , arthrose [1] |
| Début habituel | Enfance ou adolescence selon le type. [2] |
| Durée | À vie [3] |
| Les types | Hypermobile, classique, vasculaire , cyphoscoliose, arthrocalasie, dermatosparaxis, syndrome de la cornée fragile, autres [4] |
| causes | Génétique [1] |
| Facteurs de risque | Antécédents familiaux [1] |
| Méthode diagnostique | Tests génétiques , examen physique [3] |
| Diagnostic différentiel | Syndrome de Marfan , syndrome de la cutis laxa , syndrome d’hypermobilité articulaire familiale , [3] syndrome de Loeys-Dietz , trouble du spectre de l’hypermobilité |
| Traitement | Soutien [5] |
| Pronostic | Dépend du trouble spécifique [3] |
| La fréquence | 1 sur 5 000 [1] |
L’EDS se produit en raison de variations de plus de 19 gènes présents à la naissance. [1] Le gène spécifique affecté détermine le type d’EDS. [1] Certains cas résultent d’une nouvelle variation survenant au cours du développement précoce, tandis que d’autres sont hérités de manière autosomique dominante ou récessive . [1] En règle générale, ces variations entraînent des défauts dans la structure ou le traitement de la protéine collagène . [1]
Le diagnostic est souvent basé sur les symptômes et confirmé par des tests génétiques ou une biopsie cutanée , [3] mais les personnes peuvent initialement être mal diagnostiquées avec une hypocondrie , une dépression ou un syndrome de fatigue chronique . [3]
Aucun remède n’est actuellement connu [5] et le traitement est de nature symptomatique . [3] La physiothérapie et les attelles peuvent aider à renforcer les muscles et à soutenir les articulations. [3] Alors que certaines formes d’EDS entraînent une espérance de vie normale , celles qui affectent les vaisseaux sanguins la diminuent généralement. [5]
Le type hypermobile d’EDS (hEDS) affecte au moins une personne sur 5 000 dans le monde ; [1] [6] d’autres types se produisent à des fréquences plus basses. [7] [8] Le pronostic dépend du trouble spécifique. [3] La mobilité excessive a été décrite pour la première fois par Hippocrate en 400 av. [9] Les syndromes portent le nom de deux médecins, Edvard Ehlers et Henri-Alexandre Danlos , qui les ont décrits au tournant du XXe siècle. [dix]
Signes et symptômes
Ce groupe de troubles affecte les tissus conjonctifs dans tout le corps, les symptômes étant le plus souvent présents dans les articulations, la peau et les vaisseaux sanguins. Cependant, comme le tissu conjonctif se trouve dans tout le corps, l’EDS peut entraîner une série d’impacts inattendus avec n’importe quel degré de gravité, et la condition ne se limite pas aux articulations, à la peau et aux vaisseaux sanguins. [11] Les effets peuvent aller d’articulations légèrement lâches à des complications cardiovasculaires potentiellement mortelles . [12] En raison de la diversité des sous-types au sein de la famille EDS, les symptômes peuvent varier considérablement entre les personnes diagnostiquées avec EDS. [13]
Musculo-squelettique
Les symptômes musculo-squelettiques comprennent des articulations hyperflexibles qui sont instables et sujettes à l’ entorse , à la luxation , à la subluxation et à l’ Hyperextension . [3] [10] Il peut y avoir un début précoce d’ arthrose avancée , [14] une maladie articulaire dégénérative chronique, [14] une déformation en col de cygne des doigts, [15] et une déformation en boutonnière des doigts. Une déchirure des tendons ou des muscles peut survenir. [16] Déformations de la colonne vertébrale, telles que la scoliose (courbure de la colonne vertébrale), la cyphose (une bosse thoracique),le syndrome de la moelle épinière attachée , l’instabilité craniocervicale et l’hypermobilité occipitoatlantoaxiale peuvent également être présents. [17] [18] Il peut également y avoir des myalgies (douleurs musculaires) et des arthralgies (douleurs articulaires), [19] qui peuvent être graves et invalidantes. Le signe de Trendelenburg est souvent observé, ce qui signifie que lorsque vous vous tenez sur une jambe, le bassin tombe de l’autre côté. [20] La maladie d’Osgood-Schlatter , une bosse douloureuse sur le genou, est également courante. [21] Chez les nourrissons, la marche peut être retardée (au-delà de 18 mois) et il se produit un mouvement des fesses au lieu de ramper. [22]
-
![]()
![]()
Individu avec EDS montrant des doigts hypermobiles, y compris la malformation en «col de cygne» sur les 2e à 5e chiffres et un pouce hypermobile
-
![]()
![]()
Individu avec EDS affichant un pouce hypermobile
-
![]()
![]()
Individu avec EDS affichant des articulations métacarpo-phalangiennes hypermobiles
-
![]()
![]()
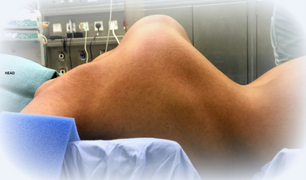
Cyphoscoliose du dos d’une personne atteinte de cyphoscoliose EDS
-
![]()
![]()
Hypermobilité articulaire sévère chez une fille avec arthrochalasie de type EDS
La peau
Le tissu conjonctif faible provoque une peau anormale. Cela peut se présenter comme extensible ou dans d’autres types être simplement doux comme du velours. Dans tous les types, une certaine fragilité accrue se produit, mais le degré varie en fonction du sous-type sous-jacent. La peau peut se déchirer et se meurtrir facilement et peut guérir avec des cicatrices atrophiques anormales, [14] et les cicatrices atrophiques qui ressemblent à du papier à cigarette sont un signe observé, y compris chez ceux dont la peau pourrait sembler autrement normale. [1] [10] [23] Dans certains sous-types, mais pas dans le sous-type hypermobile, des plis cutanés redondants se produisent, en particulier sur les paupières. Les plis cutanés redondants sont des zones d’excès de peau situées dans les plis. [14] [24]
D’autres symptômes cutanés comprennent les pseudotumeurs molluscoïdes, [25] en particulier sur les points de pression, les pétéchies , [26] les sphéroïdes sous-cutanés, [25] le livedo reticularis et les papules piézogènes sont moins fréquentes. [27] Dans l’EDS vasculaire, la peau peut également être fine et translucide. Dans la dermatosparaxis EDS, la peau est extrêmement fragile et flasque. [1]
-
![]()
![]()
Cicatrice atrophique dans un cas d’EDS
-
![]()
![]()
Peau translucide dans l’EDS vasculaire
-
![]()
![]()
Individu avec EDS affichant une hyperélasticité cutanée
-
![]()
![]()
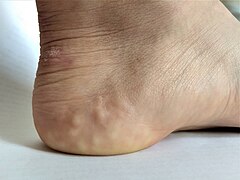
Papules piézogéniques sur le talon d’un individu atteint d’EDS hypermobile
-
![]()
![]()
Hyperélasticité cutanée au poignet
Cardiovasculaire
- Syndrome du défilé thoracique [28]
- Rupture artérielle [10]
- Les cardiopathies valvulaires , telles que le prolapsus de la valve mitrale , créent un risque accru d’ endocardite infectieuse pendant la chirurgie. Cela peut évoluer jusqu’à un degré potentiellement mortel . [29] Des anomalies de la conduction cardiaque ont été trouvées chez les personnes atteintes d’une forme d’hypermobilité de l’EDS. [30]
- Dilatation et/ou rupture ( anévrisme ) de l’aorte ascendante [31]
- Dysfonctionnement cardiovasculaire autonome tel que le syndrome de tachycardie orthostatique posturale [32] [33]
- Phénomène de raynaud
- Varices [34]
- Souffle au cœur
- Anomalies de la conduction cardiaque
Autres manifestations
- Hernie hiatale [25]
- Reflux gastro-oesophagien [35]
- Mauvaise motilité gastro-intestinale [36]
- Dysautonomie [37]
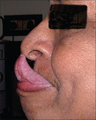
- Signe de Gorlin (toucher la langue au nez) [38]
- Prolapsus anal [25]
- Pied plat
- Trachéobronchomalacie / collapsus trachéal
- Poumon effondré ( pneumothorax spontané ) [14]
- Affections nerveuses ( syndrome du canal carpien , acroparesthésie , neuropathie , y compris neuropathie des petites fibres ) [39]
- Insensibilité aux anesthésiques locaux [40]
- Malformation d’Arnold-Chiari [41]
- Échec de l’ agrégation plaquettaire (les plaquettes ne s’agglutinent pas correctement) [42]
- Troubles mastocytaires (y compris le syndrome d’activation des mastocytes et la mastocytose ) [43]
- Complications de la grossesse : douleur accrue, saignement péripartum léger à modéré , insuffisance cervicale , déchirure utérine [16] ou rupture prématurée des membranes [44]
- Une perte auditive peut survenir dans certains types [45]
- Yeux : myopie , déchirure et décollement de la rétine , kératocône , sclérotique bleue, sécheresse oculaire, syndrome de Sjögren , subluxation du cristallin, stries angioïdes, plis épicanthiques , strabisme , cicatrisation cornéenne, syndrome de la cornée cassante, cataractes , fistules carotido-caverneuses du sinus , dégénérescence maculaire [ 46]
- Instabilité craniocervicale : causée par un ou plusieurs traumatismes de la tête et du cou tels qu’une commotion cérébrale et un coup de fouet cervical. Les ligaments du cou sont incapables de guérir correctement, par conséquent, la structure du cou n’a pas la capacité de soutenir le crâne, qui peut alors s’enfoncer dans le tronc cérébral en bloquant l’écoulement normal du liquide céphalo-rachidien, entraînant des problèmes liés à l’échec du système nerveux autonome. pour fonctionner correctement. [47] [48]
- L’ostéoporose et l’ostéopénie sont associées à l’EDS et à l’hypermobilité articulaire symptomatique [49] [50]
- Il existe certaines preuves que le SED peut être associé à des fréquences plus élevées que prévu de troubles neurodéveloppementaux tels que le trouble déficitaire de l’attention avec hyperactivité (TDAH) et d’autres problèmes d’ apprentissage , de communication et moteurs , y compris les troubles du spectre autistique et le syndrome de Tourette . [51]
-
![]()
![]()
Signe de Gorlin dans un cas d’EDS
-
![]()
![]()
Kératoglobe dans un cas de SDE avec syndrome de la cornée fragile
Parce qu’il est souvent non diagnostiqué ou mal diagnostiqué dans l’enfance, certains cas d’EDS ont été qualifiés à tort de maltraitance d’enfants. [52] La douleur peut également être diagnostiquée à tort comme un trouble du comportement ou Munchausen par procuration . [53]
La douleur associée à l’EDS varie de légère à débilitante. [54]
causes

 La fibrille de collagène et l’EDS : (a) Les fibrilles de collagène normales ont une taille et un espacement uniformes. Les fibrilles d’une personne atteinte de dermatosparaxis (b) présentent des altérations spectaculaires de la morphologie des fibrilles avec des effets graves sur la résistance à la traction des tissus conjonctifs. Une personne atteinte d’EDS classique (c) présente des fibrilles composites. Les fibrilles d’une personne déficiente en TNX (d) sont de taille uniforme et aucune fibrille composite n’est visible. Les fibrilles TNX-null (e) sont moins denses et moins bien alignées avec les fibrilles voisines.
La fibrille de collagène et l’EDS : (a) Les fibrilles de collagène normales ont une taille et un espacement uniformes. Les fibrilles d’une personne atteinte de dermatosparaxis (b) présentent des altérations spectaculaires de la morphologie des fibrilles avec des effets graves sur la résistance à la traction des tissus conjonctifs. Une personne atteinte d’EDS classique (c) présente des fibrilles composites. Les fibrilles d’une personne déficiente en TNX (d) sont de taille uniforme et aucune fibrille composite n’est visible. Les fibrilles TNX-null (e) sont moins denses et moins bien alignées avec les fibrilles voisines.
Chaque type d’EDS, à l’exception du type hypermobile (qui affecte la grande majorité des personnes atteintes d’EDS), peut être positivement lié à une variation génétique spécifique.
Des variations dans ces gènes peuvent provoquer le SED : [8]
- Structure primaire du collagène et traitement du collagène : ADAMTS2 , COL1A1 , COL1A2 , COL3A1 , COL5A1 , COL5A2
- Pliage du collagène et réticulation du collagène : PLOD1 , FKBP14
- Structure et fonction de myomatrix : TNXB , COL12A1
- Biosynthèse des glycosaminoglycanes : B4GALT7 , B3GALT6 , CHST14 , DSE
- Voie du complément : C1R , C1S
- Processus intracellulaires : SLC39A13 , ZNF469 , PRDM5
Les variations de ces gènes modifient généralement la structure, la production ou le traitement du collagène ou des protéines qui interagissent avec le collagène. Le collagène fournit structure et force au tissu conjonctif. Un défaut de collagène peut affaiblir le tissu conjonctif de la peau, des os, des vaisseaux sanguins et des organes, entraînant les caractéristiques de la maladie. [1] Les modèles d’hérédité dépendent du syndrome spécifique.
La plupart des formes d’EDS sont héritées selon un schéma autosomique dominant, ce qui signifie qu’une seule des deux copies du gène en question doit être modifiée pour provoquer un trouble. Quelques-uns sont hérités selon un schéma autosomique récessif, ce qui signifie que les deux copies du gène doivent être modifiées pour qu’une personne soit affectée par un trouble. Il peut également s’agir d’une variation individuelle ( de novo ou “sporadique”) . Des variations sporadiques se produisent sans aucun héritage. [55]
Diagnostic
Un diagnostic peut être posé par une évaluation des antécédents médicaux et une observation clinique. Les critères de Beighton sont largement utilisés pour évaluer le degré d’hypermobilité articulaire. Des études ADN et biochimiques peuvent aider à identifier les individus affectés. Les tests de diagnostic comprennent les tests de variantes du gène du collagène, le typage du collagène par biopsie cutanée, l’échocardiogramme et l’activité de la lysyl hydroxylase ou de l’oxydase. Cependant, ces tests ne sont pas en mesure de confirmer tous les cas, en particulier dans les cas d’une variation non cartographiée, de sorte que l’évaluation clinique reste importante. Si plusieurs personnes d’une famille sont touchées, il peut être possible d’effectuer un diagnostic prénatal en utilisant une technique d’information sur l’ADN connue sous le nom d’étude de liaison. [56] La connaissance de l’EDS parmi tous les types de praticiens est faible. [57] [58]Des recherches sont en cours pour identifier des marqueurs génétiques pour tous les types. [59]
Diagnostic différentiel
Plusieurs troubles partagent certaines caractéristiques avec l’EDS. Par exemple, dans la cutis laxa , la peau est lâche, pendante et ridée. Dans l’EDS, la peau peut être éloignée du corps, mais elle est élastique et revient à la normale lorsqu’elle est relâchée. Dans le syndrome de Marfan, les articulations sont très mobiles et des complications cardiovasculaires similaires surviennent. Les personnes atteintes d’EDS ont tendance à avoir une apparence “marfanoïde” (par exemple, des bras et des jambes longs, maigres, longs, des doigts “araignées”). Cependant, l’apparence physique et les caractéristiques de plusieurs types d’EDS ont également des caractéristiques telles qu’une petite taille, de grands yeux et l’apparence d’une petite bouche et d’un menton, en raison d’un petit palais. Le palais peut avoir une voûte élevée, provoquant un encombrement dentaire. Les vaisseaux sanguins peuvent parfois être facilement visibles à travers une peau translucide, en particulier sur la poitrine. Le trouble génétique du tissu conjonctif, le syndrome de Loeys-Dietz , présente également des symptômes qui se chevauchent avec l’EDS. [60]
Dans le passé, la maladie de Menkes , un trouble du métabolisme du cuivre, était considérée comme une forme d’EDS. Les gens sont souvent mal diagnostiqués avec la fibromyalgie , les troubles de la coagulation ou d’autres troubles qui peuvent imiter les symptômes du SED. En raison de ces troubles et complications similaires qui peuvent découler d’un cas non surveillé d’EDS, un diagnostic correct est important. [61] Pseudoxanthoma elasticum vaut la peine d’être pris en considération dans le diagnostic. [62]
Les types
En 2017, 13 sous-types d’EDS ont été classés à l’aide de critères diagnostiques spécifiques. [4] Selon la société Ehlers-Danlos , les syndromes peuvent également être regroupés par les symptômes déterminés par des mutations génétiques spécifiques. Les troubles du groupe A sont ceux qui affectent la structure et le traitement primaires du collagène. Les troubles du groupe B affectent le repliement et la réticulation du collagène. Le groupe C sont des troubles de la structure et de la fonction de la myomatrix. Les troubles du groupe D sont ceux qui affectent la biosynthèse des glycosaminoglycanes. Les troubles du groupe E sont caractérisés par des anomalies de la voie du complément. Le groupe F sont des troubles des processus intracellulaires, et le groupe G est considéré comme des formes non résolues d’EDS. [63]
EDS hypermobile
L’EDS hypermobile (hEDS, anciennement classé dans la catégorie 3) se caractérise principalement par une hypermobilité qui affecte à la fois les grandes et les petites articulations. Elle peut entraîner de fréquentes subluxations articulaires (luxations partielles) et des luxations. En général, les personnes atteintes de cette variante ont une peau douce, lisse et veloutée et des ecchymoses facilement, et peuvent avoir des douleurs musculaires et/ou osseuses chroniques. [4] Il affecte moins la peau que les autres formes. Il n’a pas de test génétique disponible. [29]Le SEDh est le plus courant des 19 types de troubles du tissu conjonctif. Puisqu’il n’existe aucun test génétique, les prestataires doivent diagnostiquer le SEDh en fonction de ce qu’ils savent déjà sur la condition et les attributs physiques que le patient présente. Outre les signes généraux, les attributs peuvent inclure des tissus conjonctifs défectueux dans tout le corps, des problèmes musculo-squelettiques et des antécédents familiaux. Parallèlement à ces signes généraux et effets secondaires, les patients peuvent avoir des difficultés à guérir. [64]
Les femmes enceintes doivent être averties de choses telles que la rupture des membranes avant le travail, la chute de la pression artérielle avec anesthésie, la naissance précipitée (travail très rapide et actif), la mauvaise position des saignements, etc. Les nouvelles mères atteintes du SEDh doivent accorder une attention particulière aux soins de leurs nouveaux bébés. Les mères peuvent avoir du mal à prendre soin du bébé en raison du risque de laisser tomber le bébé en raison de la faiblesse du tissu conjonctif dans les bras et les jambes, des chutes, de la dépression post-partum (plus que la population générale) et de la guérison du processus d’accouchement. [65]
Génétique de l’EDS hypermobile Alors que 12 des 13 sous-types d’EDS ont des variations génétiques qui peuvent être testées par des tests génétiques , il n’existe actuellement aucune cause génétique connue d’EDSh. Malgré le gène inconnu, le SEDh semble suivre un mode de transmission autosomique dominant . Cela signifie que pour être affecté, un individu n’a besoin que d’une mutation dans une copie du gène responsable (inconnu) dans chaque cellule. Cette mutation peut soit être héritée d’un parent, soit être une mutation de novo (nouvelle) dans le gène. Une personne atteinte du SEDh a 50 % de chances de transmettre son gène muté à ses enfants.
Récemment, plusieurs laboratoires et initiatives de recherche ont tenté de découvrir un potentiel gène hEDS. En 2018, la société Ehlers-Danlos a lancé l’étude Hypermobile Ehlers-Danlos Genetic Evaluation [66] (HEDGE). L’étude en cours a examiné plus de 1000 personnes qui ont reçu un diagnostic de SEDh selon les critères de 2017 afin d’évaluer leur génome pour une mutation commune potentielle. À ce jour, il n’y a eu que 200 personnes atteintes du SEDh qui ont subi un séquençage du génome entier et 500 personnes qui ont subi un séquençage de l’exome entier ; cette étude vise à augmenter ces chiffres de manière significative.
Le résultat le plus prometteur de ce dépistage accru provient du Norris Lab, dirigé par le Dr Russell Norris [67] , PhD, du département de médecine régénérative et de biologie cellulaire de l’Université médicale de Caroline du Sud. En utilisant l’édition du génome médiée par CRISPR Cas-9 sur des modèles murins de la maladie, le laboratoire a récemment identifié un “gène candidat très puissant [68] ” pour le SEDh. Cette découverte et une meilleure compréhension des complications cardiaques associées à la majorité des sous-types d’EDS ont conduit au développement de multiples voies médicamenteuses impliquées dans les valves aortique et mitrale.maladies. Bien que ce gène candidat n’ait pas été identifié publiquement, le laboratoire Norris a mené plusieurs études impliquant le séquençage du génome d’une petite population et a dressé une liste de travail de gènes hEDS possibles. Une mutation de COL3A1 [69] dans une seule famille avec un phénotype hEDS autosomique dominant s’est avérée entraîner une réduction de la sécrétion de collagène et une sur-modification du collagène. Dans 35 familles, des altérations du nombre de copies dans TPSAB1 [70] , codant pour l’alpha-tryptase, étaient associées à une augmentation des taux sériques basaux de tryptase , associée à un dysfonctionnement autonome , des troubles gastro -intestinaux, des symptômes allergiques et cutanés et des anomalies du tissu conjonctif, tous concomitants avec le phénotype hEDS. Enfin, la ténascine X [71] , une protéine de la matrice extracellulaire importante pour la mutation du collagène codée par le gène TNXB, a été associée au SEDh chez les patients présentant un déficit en ténascine X.
Le laboratoire Norris tente également de trouver ce gène insaisissable en examinant les gènes impliqués dans la formation de l’aorte et des valves mitrales, car ces valves sont souvent prolabées ou malformées en tant que symptôme de l’EDS. Étant donné que le SEDh est une maladie complexe et multi-organique, se concentrer sur un trait caractéristique s’est avéré fructueux. Un gène potentiel trouvé par cette voie est DZIP1 , qui régule le développement de la valve cardiaque chez les mammifères par un mécanisme Cby1-bêta-caténine. Mutations au niveau de ce gène effet de la bêta-caténinecascade impliquée dans le développement, provoquant une malformation de la matrice extra-cellulaire entraînant une perte de collagène. Un manque de collage ici est à la fois compatible avec le SEDh et explique la nature “floppy” des malformations cardiaques des valves mitrale et aortique. Une deuxième étude génétique spécifique au prolapsus de la valve mitrale s’est concentrée sur la voie de signalisation du PDGF , impliquée dans les ligands des facteurs de croissance et les isoformes des récepteurs [72] (15). Des mutations dans cette voie affectent la capacité de localiser les cils dans divers types de cellules, y compris les cellules cardiaques. Avec les ciliopathies qui en résultent, des structures telles que la voie d’éjection cardiaque, l’assemblage du tube cardiaque et la fusion cardiaque sont toutes limitées et/ou endommagées.
EDS classique
L’EDS classique (anciennement classé dans le type 1) se caractérise par une peau extrêmement élastique qui est fragile et se meurtrit facilement ; et hypermobilité des articulations. Les pseudotumeurs molluscoïdes (hématomes calcifiés qui se produisent sur les points de pression) et les sphéroïdes (kystes contenant de la graisse sur les avant-bras et les tibias) sont également souvent observés. Une complication secondaire de l’hyperélasticité présentée dans de nombreux cas d’EDS rend les plaies se refermant d’elles-mêmes plus difficiles. [23] Parfois, le développement moteur est retardé et une hypotonie se produit. [4] La variation provoquant ce type d’EDS se trouve dans les gènes COL5A2, COL5A1 et moins fréquemment COL1A1 . Il implique davantage la peau que le SEDh. [73]Dans l’EDS classique, une grande variation dans la présentation des symptômes d’un patient à l’autre est souvent observée. En raison de cette variance, le SED a souvent été un trouble sous-diagnostiqué. [74] Sans tests génétiques, les professionnels de la santé peuvent être en mesure de fournir un diagnostic provisoire basé sur un examen attentif de la bouche, de la peau et des os, ainsi que sur des évaluations neurologiques. [75] L’hyperélasticité de la peau chez les patients atteints d’EDS peut être difficile à utiliser dans le diagnostic car aucune bonne méthode standardisée pour mesurer et évaluer l’élasticité de la peau n’est connue, mais l’hyperélasticité est toujours un bon indicateur comme quelque chose qui peut pointer vers l’EDS avec d’autres symptômes.
Une bonne façon de commencer le processus de diagnostic consiste à examiner les antécédents familiaux; L’EDS est une maladie autosomique dominante, elle est donc souvent héritée des membres de la famille. [23] Les tests génétiques restent le moyen le plus fiable pour établir un diagnostic d’EDS. [76] Bien qu’aucun remède n’ait été trouvé pour l’EDS de type 1, un programme d’exercices sans mise en charge peut aider à réduire la tension musculaire, ce qui peut aider à corriger certains des symptômes de l’EDS. Les médicaments anti-inflammatoires et les changements de mode de vie peuvent aider à soulager les douleurs articulaires. Des choix de mode de vie doivent également être faits avec les enfants atteints d’EDS pour essayer de prévenir les blessures à la peau. Le port de vêtements de protection peut y contribuer. Dans une plaie, des points de suture profonds sont souvent utilisés et laissés en place plus longtemps que la normale. [23]
Variante vasculaire du syndrome d’Ehlers-Danlos
L’EDS vasculaire (anciennement classé dans le type 4) est identifié par une peau fine, translucide, extrêmement fragile et qui se meurtrit facilement. Elle se caractérise également par des vaisseaux sanguins et des organes fragiles qui peuvent facilement se rompre. Les personnes touchées sont souvent de petite taille et ont des cheveux fins. Il a également des traits caractéristiques du visage, notamment de grands yeux, un menton trop petit, des joues creuses, un nez et des lèvres fins et des oreilles sans lobes. [77] Une hypermobilité articulaire est présente, mais généralement confinée aux petites articulations (doigts, orteils). D’autres caractéristiques communes incluent le pied bot, la rupture des tendons et/ou des muscles, l’acrogérie (vieillissement prématuré de la peau des mains et des pieds), l’apparition précoce de varices, le pneumothorax (effondrement d’un poumon), la récession des gencives et une diminution de la quantité de graisse sous la peau. [4]Elle peut être causée par les variations du gène COL3A1 . [77] Rarement, les variations de COL1A1 peuvent également en être la cause. [8]
Cyphoscoliose EDS
La cyphoscoliose EDS (anciennement classée comme type 6) est associée à une hypotonie sévère à la naissance, un retard du développement moteur, une scoliose progressive (présente dès la naissance) et une fragilité sclérale. Les personnes peuvent également avoir des ecchymoses faciles, des artères fragiles susceptibles de se rompre, des cornées inhabituellement petites et une ostéopénie (faible densité osseuse). D’autres caractéristiques communes incluent un «habitus marfanoïde» qui se caractérise par de longs doigts fins (arachnodactylie), des membres inhabituellement longs et une poitrine enfoncée (pectus excavatum) ou une poitrine saillante (pectus carinatum). [4] Elle peut être causée par des variations du gène PLOD1 ou, plus rarement, du gène FKBP14 . [78]
Arthrochalasie EDS
L’arthrochalasie EDS (anciennement classée dans les types 7A et B) se caractérise par une hypermobilité articulaire sévère et une luxation congénitale de la hanche. D’autres caractéristiques communes incluent une peau fragile et élastique avec des ecchymoses faciles, une hypotonie, une cyphoscoliose (cyphose et scoliose) et une légère ostéopénie. [4] Le collagène de type I est généralement affecté. Il est très rare, avec environ 30 cas rapportés. Il est plus sévère que le type d’hypermobilité. Des variations dans les gènes COL1A1 et COL1A2 en sont la cause. [79]
Dermatosparaxis EDS
Dermatosparaxis EDS (anciennement classé dans le type 7C) est associé à une peau extrêmement fragile entraînant de graves ecchymoses et cicatrices ; peau affaissée et redondante, en particulier sur le visage; hypermobilité allant de légère à grave ; et hernies. Des variations du gène ADAMTS2 en sont la cause. Il est extrêmement rare, avec environ 11 cas signalés. [80]
Syndrome de la cornée fragile
Le syndrome de la cornée fragile est caractérisé par un amincissement progressif de la cornée , un kératoglobe ou un kératocône progressif d’apparition précoce , une myopie, une perte auditive et des sclères bleues . [4] [81] Les symptômes classiques, tels que les articulations hypermobiles et la peau hyperélastique, sont également souvent observés. [82] Il en existe deux types. Le type 1 est dû à des variations du gène ZNF469 . Le type 2 est dû à des variations du gène PRDM5 . [81]
EDS de type classique
L’EDS de type classique se caractérise par une hyperextensibilité cutanée avec un grain de peau velouté et l’absence de cicatrices atrophiques, une hypermobilité articulaire généralisée avec ou sans luxations récurrentes (le plus souvent épaule et cheville), et une peau facilement contusionnée ou des ecchymoses spontanées (décolorations de la peau résultant de saignements sous). [4] Elle peut être causée par des variations du gène TNXB . [8]
SED spondylodysplasique
L’EDS spondylodysplasique se caractérise par une petite taille (progressive dans l’enfance), une hypotonie musculaire (allant d’une forme congénitale sévère à une apparition tardive légère) et une courbure des membres. [4] Elle peut être causée par des variations dans les deux copies du gène B4GALT7 . D’autres cas peuvent être causés par des variations du gène B3GALT6 . Les personnes présentant des variations de ce gène peuvent souffrir de cyphoscoliose, de doigts effilés, d’ostéoporose, d’anévrismes aortiques et de problèmes pulmonaires. D’autres cas peuvent être causés par le gène SLC39A13 . Les personnes présentant des variations de ce gène ont les yeux protubérants, les paumes des mains ridées, les doigts effilés et une hypermobilité articulaire distale. [83]
EDS musculocontractural
L’EDS musculocontractural est caractérisé par des contractures multiples congénitales, typiquement des contractures d’adduction-flexion et/ou un pied bot varus équin, des caractéristiques craniofaciales caractéristiques, qui sont évidentes à la naissance ou au début de la petite enfance, et des caractéristiques cutanées telles qu’une hyperextensibilité cutanée, des ecchymoses, une fragilité cutanée avec cicatrices atrophiques et augmentation des rides palmaires. [4] Elle peut être causée par des variations du gène CHST14 . Certains autres cas peuvent être causés par des variations du gène DSE . [84]
SDE myopathique
L’EDS myopathique (mEDS) se caractérise par trois critères majeurs : une hypotonie musculaire congénitale et/ou une atrophie musculaire qui s’améliore avec l’âge, des contractures articulaires proximales du genou, de la hanche et du coude, et une hypermobilité des articulations distales (chevilles, poignets, pieds et mains). [4] En outre, quatre critères mineurs peuvent contribuer à un diagnostic de mEDS. Ce trouble peut être hérité par un mode autosomique dominant ou autosomique récessif. [63] Des tests moléculaires doivent être effectués pour vérifier la présence de mutations dans le gène COL12A1 ; sinon, d’autres myopathies de type collagène doivent être envisagées. [63]
EDS parodontal
Le SED parodontal (SEDp) est une maladie héréditaire autosomique dominante [63] caractérisée par quatre critères majeurs de parodontite sévère et réfractaire d’apparition précoce (enfance ou adolescence), absence de gencive attachée, plaques prétibiales et antécédents familiaux d’un premier- parent diplômé qui répond aux critères cliniques. [4] Huit critères mineurs peuvent également contribuer au diagnostic de pEDS. Les tests moléculaires peuvent révéler des mutations dans les gènes C1R ou C1S affectant la protéine C1r. [63]
EDS cardiaque-valvulaire
L’EDS cardiaque-valvulaire (EDScv) est caractérisé par trois critères principaux : des problèmes cardiaques-valvulaires progressifs sévères (affectant les valves aortiques et mitrales), des problèmes cutanés tels qu’une hyperextensibilité, des cicatrices atrophiques, une peau fine et des ecchymoses faciles, et une hypermobilité articulaire (généralisée ou limité aux petites articulations). [4] Quatre critères mineurs peuvent aider au diagnostic du SEDcv. [63] Le cvEDS est une maladie autosomique récessive, héritée par la variation des deux allèles du gène COL1A2. [85]
La gestion
Aucun remède pour les syndromes d’Ehlers-Danlos n’est connu et le traitement est de soutien. Une surveillance étroite du système cardiovasculaire, de la physiothérapie, de l’ergothérapie et des instruments orthopédiques (p. ex. fauteuils roulants, attelles, plâtre) peut être utile. Cela peut aider à stabiliser les articulations et à prévenir les blessures. Les instruments orthopédiques sont utiles pour prévenir d’autres lésions articulaires, en particulier sur de longues distances. Les gens doivent éviter les activités qui provoquent un blocage ou une extension excessive de l’articulation. [86]
Un médecin peut prescrire un plâtre pour stabiliser les articulations. Les médecins peuvent référer une personne à un orthésiste pour un traitement orthétique (attelle). Les médecins peuvent également consulter un physiothérapeute et/ou un ergothérapeute pour aider à renforcer les muscles et apprendre aux gens comment utiliser et préserver correctement leurs articulations. [87] [88]
L’aquathérapie favorise le développement musculaire et la coordination. [89] Avec la thérapie manuelle, l’articulation est doucement mobilisée dans l’amplitude des mouvements et/ou des manipulations. [87] [88] Si le traitement conservateur n’est pas utile, une réparation chirurgicale de l’articulation peut être nécessaire. Des médicaments pour diminuer la douleur ou gérer des affections cardiaques, digestives ou autres peuvent être prescrits. Pour diminuer les ecchymoses et améliorer la cicatrisation des plaies, certaines personnes ont réagi à la vitamine C. [90] Des précautions spéciales sont souvent prises par les travailleurs de la santé en raison du grand nombre de complications qui ont tendance à survenir chez les personnes atteintes d’EDS. Dans l’EDS vasculaire, les signes de douleurs thoraciques ou abdominales sont considérés comme des situations traumatiques. [91]
Les cannabinoïdes et la marijuana médicale ont montré une certaine efficacité pour réduire les niveaux de douleur. [92]
En général, l’intervention médicale se limite à un traitement symptomatique. Avant la grossesse, les personnes atteintes d’EDS devraient bénéficier d’un conseil génétique et se familiariser avec les risques pour leur propre corps que pose la grossesse. Les enfants atteints d’EDS doivent recevoir des informations sur leur trouble afin qu’ils puissent comprendre pourquoi ils doivent éviter les sports de contact et autres activités physiquement stressantes. Il faut apprendre aux enfants qu’il ne faut pas démontrer les positions inhabituelles qu’ils peuvent maintenir en raison d’articulations lâches, car cela peut provoquer une dégénérescence précoce des articulations. Un soutien émotionnel ainsi qu’une thérapie comportementale et psychologique peuvent être utiles. Les groupes de soutien peuvent être extrêmement utiles pour les personnes aux prises avec des changements majeurs dans leur mode de vie et une mauvaise santé. Les membres de la famille, les enseignants,[93]
Gestion de la douleur
Traiter avec succès la douleur chronique dans l’EDS nécessite une équipe multidisciplinaire. Les moyens de gérer la douleur peuvent consister à modifier les techniques de gestion de la douleur utilisées dans la population normale. La douleur chronique a deux types. Le premier type est le type nociceptif , qui est causé par une blessure subie par les tissus. Le deuxième type est la douleur neuropathique , causée par des signaux anormaux du système nerveux. Dans la plupart des cas, la douleur est un mélange inégal des deux. Physiothérapie(rééducation par l’exercice) a des preuves d’un effet positif. Il stabilise principalement le noyau du corps et les articulations. Les exercices d’étirement doivent être réduits à des étirements lents et doux pour réduire les risques de luxations ou de subluxations. Les méthodes utilisables peuvent inclure la rééducation de la posture, la libération musculaire, la mobilisation des articulations, la stabilisation du tronc et la thérapie manuelle pour les muscles surmenés. La thérapie cognitivo-comportementale est utilisée chez tous les patients souffrant de douleurs chroniques, en particulier ceux qui souffrent de douleurs sévères, chroniques, qui contrôlent la vie et qui ne répondent pas au traitement. Son efficacité n’a pas été vérifiée dans les essais cliniques à ce jour. L’état actuel de la gestion de la douleur avec l’EDS est considéré comme insuffisant. [53]
Médicaments
Les anti-inflammatoires non stéroïdiens ( AINS ) peuvent aider si la douleur est causée par une inflammation. Cependant, l’utilisation à long terme des AINS est souvent un facteur de risque d’effets secondaires gastro-intestinaux, rénaux et sanguins. Il peut aggraver les symptômes du syndrome d’activation des mastocytes , une maladie qui peut être associée au SED. L’acétaminophène peut être utilisé pour éviter les effets secondaires liés aux saignements des AINS. [53]
Les opioïdes ont montré une efficacité dans certains cas de SED pour la gestion de la douleur aiguë et chronique. 112
La lidocaïne peut être appliquée localement après des subluxations et des gencives douloureuses. Il peut également être injecté dans les zones douloureuses en cas de douleurs musculo-squelettiques. [53]
Si la douleur est d’origine neuropathique, des antidépresseurs tricycliques à faible dose, des anticonvulsivants et des inhibiteurs sélectifs de la recapture de la noradrénaline peuvent être utilisés. [53]
Prise en charge des luxations et subluxations
Lorsqu’une luxation ou une subluxation se produit, des spasmes musculaires et un stress ont tendance à se produire, augmentant la douleur et réduisant les risques de soulagement naturel de la luxation/subluxation. Les méthodes pour soutenir une articulation après un tel incident comprennent l’utilisation d’une élingue pour maintenir l’articulation en place et lui permettre de se détendre. Les plâtres orthopédiques ne sont pas conseillés car il pourrait y avoir de la douleur si des muscles non relâchés essaient toujours de se contracter contre le plâtre. D’autres solutions pour favoriser la relaxation sont la chaleur, les massages doux et les distractions mentales. [94]
Opération
L’instabilité des articulations, entraînant des subluxations et des douleurs articulaires, nécessite souvent une intervention chirurgicale chez les personnes atteintes d’EDS. L’instabilité de presque toutes les articulations peut survenir, mais apparaît le plus souvent dans les membres inférieurs et supérieurs, le poignet, les doigts, l’épaule, le genou, la hanche et la cheville étant les plus courants. [87]
Les interventions chirurgicales courantes sont le débridement articulaire , les remplacements de tendons, la capsulorraphie et l’ arthroplastie . Après la chirurgie, le degré de stabilisation, la réduction de la douleur et la satisfaction des personnes peuvent s’améliorer, mais la chirurgie ne garantit pas un résultat optimal ; les personnes concernées et les chirurgiens se disent insatisfaits des résultats. Le consensus est que le traitement conservateur est plus efficace que la chirurgie, [30]d’autant plus que les gens ont des risques supplémentaires de complications chirurgicales dues à la maladie. Trois problèmes chirurgicaux fondamentaux se posent en raison de l’EDS – la résistance des tissus est diminuée, ce qui rend le tissu moins adapté à la chirurgie ; la fragilité des vaisseaux sanguins peut causer des problèmes pendant la chirurgie ; et la cicatrisation est souvent retardée ou incomplète. [87] Si vous envisagez une intervention chirurgicale, il serait prudent de demander des soins à un chirurgien possédant des connaissances et une expérience approfondies dans le traitement des personnes atteintes d’EDS et de problèmes d’hypermobilité articulaire. [95]
Les anesthésiques locaux, les cathéters artériels et les cathéters veineux centraux entraînent un risque plus élevé de formation d’ecchymoses chez les personnes atteintes d’EDS. Certaines personnes atteintes d’EDS montrent également une résistance aux anesthésiques locaux. [96] La résistance à la lidocaïne et à la bupivacaïne n’est pas rare, et la mépivacaïne a tendance à mieux fonctionner chez les personnes atteintes d’EDS. Des recommandations spéciales pour l’anesthésie sont données aux personnes atteintes d’EDS. [97] Des recommandations détaillées pour l’anesthésie et les soins périopératoires des personnes atteintes d’EDS devraient être utilisées pour améliorer la sécurité. [95]
La chirurgie chez les personnes atteintes d’EDS nécessite une manipulation soigneuse des tissus et une immobilisation plus longue par la suite. [98]
Pronostic
Le résultat pour les personnes atteintes d’EDS dépend du type spécifique d’EDS qu’elles ont. Les symptômes varient en gravité, même dans le même trouble, et la fréquence des complications varie. Certaines personnes ont des symptômes négligeables, tandis que d’autres sont sévèrement limitées dans la vie quotidienne. Une instabilité articulaire extrême, des douleurs musculo-squelettiques chroniques, des maladies articulaires dégénératives, des blessures fréquentes et des déformations de la colonne vertébrale peuvent limiter la mobilité. De graves déformations de la colonne vertébrale peuvent affecter la respiration. Dans le cas d’une instabilité articulaire extrême, les luxations peuvent résulter de tâches simples telles que se retourner dans le lit ou tourner une poignée de porte. Les conditions secondaires telles que le dysfonctionnement autonome ou les problèmes cardiovasculaires, survenant dans n’importe quel type, peuvent affecter le pronostic et la qualité de vie. Une incapacité grave liée à la mobilité est plus souvent observée dans le SEDh que dans le SDE classique ou le SDE vasculaire.[99]
Bien que tous les types d’EDS soient potentiellement mortels, la plupart des gens ont une durée de vie normale. Cependant, les personnes présentant une fragilité des vaisseaux sanguins présentent un risque élevé de complications mortelles, notamment la rupture artérielle spontanée, qui est la cause la plus fréquente de mort subite. L’espérance de vie médiane dans la population atteinte d’EDS vasculaire est de 48 ans. [100]
Complications
Vasculaire
- Pseudoanévrisme [101]
- Lésions vasculaires (de nature contestée) dues à des déchirures de la paroi des artères ou à une détérioration de tissus congénitalement fins et fragiles [101]
- Artères hypertrophiées [101]
Gastro-intestinal
- Un risque de perforation colique de 50 % existe. [101]
Obstétrique
- La grossesse augmente le risque de rupture utérine. [101]
- La mortalité maternelle est d’environ 12 %. [101]
- Une hémorragie utérine peut survenir pendant la récupération post-partum. [101]
Développement de bases de données de recherche et de registres
La Ehlers-Danlos Society et la Bobby Jones Chiari and Syringomyelia Foundation se sont associées à LunaDNA pour créer des registres internationaux de patients afin de faire avancer la recherche sur les syndromes d’Ehlers-Danlos. Le registre et référentiel mondial EDS et HSD de la société Ehlers-Danlos permet la recherche de gènes pour l’EDS hypermobile et facilite la recherche sur la fréquence des symptômes associés et d’autres conditions. Ils cherchent également à cartographier les expériences des personnes vivant avec l’EDS et le HSD, à l’échelle mondiale, et à découvrir de nouvelles formes d’EDS ou de HSD. [102] Registre international des patients de la Bobby Jones Chiari and Syringomyelia Foundationcherche à évaluer l’efficacité des programmes de soins de santé et des traitements pour Chiari, la syringomyélie et d’autres troubles compliquant souvent trouvés dans l’EDS [103]
Épidémiologie
On estime que les syndromes d’Ehlers-Danlos surviennent dans environ une naissance sur 5 000 dans le monde. Initialement, les estimations de prévalence variaient d’une personne sur 250 000 à 500 000, mais ces estimations se sont rapidement avérées trop faibles, car davantage d’études ont été menées sur les troubles et les professionnels de la santé sont devenus plus aptes au diagnostic. L’EDS peut être beaucoup plus fréquent que l’estimation actuellement acceptée en raison du large éventail de gravités avec lesquelles le trouble se présente. [104]
La prévalence des troubles diffère considérablement. L’EDS hypermobile est le plus fréquent, suivi de l’EDS classique. Les autres sont très rares. Par exemple, moins de 10 nourrissons et enfants atteints de dermatosparaxis EDS ont été décrits dans le monde.
Certains types d’EDS sont plus fréquents chez les juifs ashkénazes . Par exemple, la probabilité d’être porteur de la dermatosparaxis EDS est d’une sur 2 000 dans la population générale, alors que la prévalence de cette variation chez les Juifs ashkénazes est d’une sur 248. [105]
Histoire
Jusqu’en 1997, le système de classification de l’EDS comprenait 10 types spécifiques et reconnaissait l’existence d’autres types extrêmement rares. À cette époque, le système de classification a subi une refonte et a été réduit à six grands types utilisant des titres descriptifs. Les spécialistes en génétique reconnaissent que d’autres types de cette condition existent, mais n’ont été documentés que dans des familles individuelles. À l’exception de l’ hypermobilité (type 3), le type le plus courant des 10 types, certaines des variations spécifiques impliquées ont été identifiées et peuvent être identifiées avec précision par des tests génétiques.; ceci est précieux en raison de la grande variation dans les cas individuels. Les résultats négatifs des tests génétiques, cependant, n’excluent pas le diagnostic, car toutes les variations n’ont pas été découvertes; par conséquent, la présentation clinique est très importante. [106]
Les formes d’EDS dans cette catégorie peuvent présenter une peau douce et légèrement extensible, des os raccourcis, une diarrhée chronique, une hypermobilité et une luxation articulaires, une rupture de la vessie ou une mauvaise cicatrisation. Les modèles d’hérédité dans ce groupe comprennent le récessif lié à l’X, l’autosomique dominant et l’autosomique récessif. Voici des exemples de types de syndromes apparentés autres que ceux mentionnés ci-dessus dans la littérature médicale : [107]
- 305200 : type 5
- 130080 : type 8 – gène non spécifié, locus 12p13
- 225310 : type 10 – gène non spécifié, locus 2q34
- 608763 : Type Beasley-Cohen
- 130070 : forme progéroïde – B4GALT7
- 130090 : type non spécifié
- 601776 : Syndrome d’Ehlers–Danlos déficient en D4ST1 (syndrome du pouce-pied bot en adduction) CHST14
Société et culture
EDS a peut-être contribué au talent du violoniste virtuose Niccolò Paganini , car il était capable de jouer des doigtés plus larges qu’un violoniste typique. [108]
De nombreux artistes interprètes ou exécutants ont un EDS. Plusieurs d’entre eux ont été présentés comme l’Elastic Skin Man, l’India Rubber Man et le Frog Boy. Ils comprenaient des personnalités aussi connues (à leur époque) que Felix Wehrle, James Morris et Avery Childs. Deux artistes avec EDS détiennent actuellement des records du monde. Le contorsionniste Daniel Browning Smith a un EDS hypermobile et détient l’actuel record du monde Guinness pour l’homme le plus flexible à partir de 2018, tandis que Gary “Stretch” Turner , artiste de spectacle dans le cirque des horreurs, a détenu l’actuel record du monde Guinness pour la peau la plus élastique depuis 1999, pour sa capacité à étirer la peau de son ventre de 6,25 pouces. [109]
Cas notables

 Stevie Boebi et Annie Elainey, qui ont EDS, debout avec des aides à la marche sur le tapis rouge.
Stevie Boebi et Annie Elainey, qui ont EDS, debout avec des aides à la marche sur le tapis rouge. 
 La candidate au concours, Victoria Graham, est atteinte d’EDS.
La candidate au concours, Victoria Graham, est atteinte d’EDS.
- L’actrice Cherylee Houston a un EDS hypermobile. Elle utilise un fauteuil roulant et a été la première actrice handicapée à plein temps sur Coronation Street [110]
- Drag queen et vainqueur de la 11ème saison de RuPaul’s Drag Race Yvie Oddly [111]
- Eric l’acteur , un visiteur régulier du Howard Stern Show [112]
- Actrice et activiste Jameela Jamil [113]
- Écrivain et actrice Lena Dunham [114]
- Chanteuse australienne Sia [115]
- Annie Elainey , YouTubeuse et militante des droits des personnes handicapées [116]
- Miss Amérique 2020 Camille Schrier [117]
- Chanteuse/compositrice sourde Mandy Harvey
- Actrice et écrivain pornographique Lorelei Lee [118]
- Trevor Jones, candidat à l’émission de télé-réalité, est mort de la forme vasculaire de la maladie [119]
Autres espèces
Il a été démontré que les syndromes de type Ehlers-Danlos sont héréditaires chez les chats himalayens , certains chats domestiques à poils courts [120] et certaines races de bovins. [121] Il est considéré comme une condition sporadique chez les chiens domestiques. Il a un traitement et un pronostic similaires. Les animaux atteints de la maladie ne doivent pas être élevés, car la maladie peut être héréditaire. [122]
- SDE pour animaux
-
![]()
![]()
EDS chez un chien
-
![]()
![]()
Même chien avec EDS
-
![]()
![]()
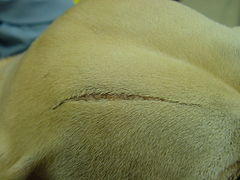
EDS chez le même chien montrant une cicatrice atrophique
La desmite dégénérative du ligament suspenseur est une affection similaire observée chez de nombreuses races de chevaux . [123] Il a été noté à l’origine dans le Paso péruvien et considéré comme une condition de surmenage et d’âge avancé, mais il est reconnu dans tous les groupes d’âge et à tous les niveaux d’activité. Il a été noté chez les poulains nouveau-nés.
Voir également
-
![icon]()
![icon]() Portail de la médecine
Portail de la médecine
- Société Ehlers-Danlos
- Trouble du spectre de l’hypermobilité
Références
- ^ un bcdefghijklmnop ” Syndrome d’ Ehlers – Danlos ” . _ _ _ _ _ _ _ _ Génétique Accueil Référence . Archivé de l’original le 8 mai 2016 . Récupéré le 8 mai 2016 .
- ^ un b Anderson BE (2012). La collection Netter d’illustrations médicales – Système tégumentaire (2 éd.). Sciences de la santé Elsevier. p. 235. ISBN 978-1455726646. Archivé de l’original le 2017-11-05 – via E-Book.
- ^ un bcdefghjk Lawrence EJ ( décembre 2005 ) . _ _ _ “La présentation clinique du syndrome d’Ehlers-Danlos”. Avancées en soins néonatals . 5 (6): 301–314. doi : 10.1016/j.adnc.2005.09.006 . PMID 16338669 . S2CID 7717730 .
- ^ un bcdefghijklmn ” Syndromes d’ Ehlers – Danlos ” . _ _ _ _ _ _ rarediseases.info.nih.gov . 20 avril 2017. Archivé de l’original le 24 septembre 2017 . Récupéré le 23 septembre 2017 .
![Public Domain]()
![Public Domain]() Cet article incorpore le texte de cette source, qui est dans le domaine public .
Cet article incorpore le texte de cette source, qui est dans le domaine public . - ^ un bc Ferri FF (2016). Conseiller patient Netter de Ferri . Sciences de la santé Elsevier. p. 939. ISBN 9780323393249. Archivé de l’original le 2017-11-05.
- ^ Tinkle, Brad; Castori, Marco; Berglund, Britta; Cohen, Hélène; Grahame, Rodney; Kazkaz, Hanadi; Lévy, Howard (2017). “Syndrome d’Ehlers-Danlos hypermobile (alias syndrome d’Ehlers-Danlos de type III et type d’hypermobilité du syndrome d’Ehlers-Danlos): description clinique et histoire naturelle” . American Journal of Medical Genetics Part C: Séminaires en génétique médicale . 175 (1): 48–69. doi : 10.1002/ajmg.c.31538 . ISSN 1552-4876 . PMID 28145611 . S2CID 4440630 .
- ^ Brady, Angela F.; Demirdas, Serwet ; Fournel-Gigleux, Sylvie; Ghali, Neeti ; Giunta, Cécile ; Kapferer-Seebacher, Inès; Kosho, Tomoki ; Mendoza-Londono, Roberto; Pope, Michael F.; Rohrbach, Marianne; Van Damme, Tim (mars 2017). “Les syndromes d’Ehlers-Danlos, types rares” . Journal américain de génétique médicale. Partie C, Séminaires en génétique médicale . 175 (1): 70-115. doi : 10.1002/ajmg.c.31550 . ISSN 1552-4876 . PMID 28306225 . S2CID 4439633 .
- ^ un bcd Malfait F, Francomano C , Byers P, Belmont J, Berglund B, Black J, et al. (mars 2017). “La classification internationale 2017 des syndromes d’Ehlers-Danlos”. Journal américain de génétique médicale. Partie C, Séminaires en génétique médicale . 175 (1): 8–26. doi : 10.1002/ajmg.c.31552 . PMID 28306229 . S2CID 4440499 .
![icon of an open green padlock]()
![icon of an open green padlock]()
- ^ Beighton PH, Grahame R, Bird HA (2011). Hypermobilité des Articulations . Springer. p. 1. ISBN 9781848820852. Archivé de l’original le 2017-11-05.
- ^ un bcd Byers PH , Murray ML (novembre 2012). “Troubles héréditaires du collagène: le paradigme du syndrome d’Ehlers-Danlos”. Le Journal de la dermatologie d’investigation . 132 (E1): E6–11. doi : 10.1038/skinbio.2012.3 . PMID 23154631 .
![open access]()
![open access]()
- ^ “Que sont les syndromes d’Ehlers-Danlos?” . La Société Ehlers Danlos . Récupéré le 16/02/2021 .
- ^ “Syndrome d’Ehlers-Danlos” . Référence génétique à domicile . Récupéré le 4 avril 2018 .
- ^ “Syndromes d’Ehlers Danlos” . NORD (Organisation Nationale des Maladies Rares) . Récupéré le 19/04/2022 .
- ^ un bcde ” Syndrome d’ Ehlers -Danlos” . Clinique Mayo . Archivé de l’original le 25 juin 2012 . Récupéré le 25 mai 2012 .
- ^ Wei DH, Terrono AL (octobre 2015). “Superficialis Sling (Flexor Digitorum Superficialis Tenodesis) pour la reconstruction du col de cygne”. Le Journal de chirurgie de la main . 40 (10): 2068-2074. doi : 10.1016/j.jhsa.2015.07.018 . PMID 26328902 .
- ^ un b “Type-EDS Vasculaire” . Réseau du syndrome d’Ehlers-Danlos CARES Inc . Archivé de l’original le 2012-06-04 . Récupéré le 25/05/2012 .
- ^ Dordoni C, Ciaccio C, Venturini M, Calzavara-Pinton P, Ritelli M, Colombi M (août 2016). “Délimitation plus poussée du syndrome d’Ehlers-Danlos lié à FKBP14 : un patient présentant des complications vasculaires précoces et une cyphoscoliose non progressive, et revue de la littérature” (PDF) . Journal américain de génétique médicale. Partie A. 170 (8) : 2031-2038. doi : 10.1002/ajmg.a.37728 . manche : 11379/494257 . PMID 27149304 . S2CID 43512125 .
- ^ Henderson, Fraser C.; Austin, Claudiu; Benzel, Edouard; Bolognaise, Paolo; Ellenbogen, Richard; Francomano, Clair A.; Ireton, Candace ; Klinge, Pétra ; Koby, Myles; Longtemps, Donlin ; Patel, Sunil (mars 2017). “Manifestations neurologiques et rachidiennes des syndromes d’Ehlers-Danlos” . Journal américain de génétique médicale. Partie C, Séminaires en génétique médicale . 175 (1): 195–211. doi : 10.1002/ajmg.c.31549 . ISSN 1552-4876 . PMID 28220607 . S2CID 4438281 .
- ^ Gedalia A, Press J, Klein M, Buskila D (juillet 1993). “Hypermobilité articulaire et fibromyalgie chez les écoliers” . Annales des maladies rhumatismales . 52 (7): 494–496. doi : 10.1136/ard.52.7.494 . PMC 1005086 . PMID 8346976 .
- ^ Dommerholt J (2012-01-27). “Colloque CSF Ehlers Danlos, Dr Jan Dommerholt” . Fondation Chiari & Syringomyélie. Archivé de l’original le 4 mai 2013 . Récupéré le 10 juin 2013 .
- ^ Vigorita VJ, Mintz D, Ghelman B (2008). Pathologie orthopédique (2e éd.). Philadelphie : Lippincott Williams et Wilkins. p. 5–6. ISBN 978-0781796705.
- ^ “Syndrome d’Ehlers-Danlos – Diagnostic – Approche” . Meilleures pratiques BMJ . 13 décembre 2016. Archivé de l’original le 19 août 2010 . Récupéré le 18 août 2017 .
- ^ un bcd Malfait F, Wenstrup R, De Paepe A (mai 2017). “Syndrome d’Ehlers-Danlos classique”. GeneReviews . Université de Washington.
- ^ “Syndrome d’Ehlers Danlos – Morphopédie” . morphopedics.wikidot.com . Récupéré le 15/06/2018 .
- ^ un bcd ” Classique Type-EDS “ . Réseau du syndrome d’Ehlers-Danlos CARES Inc . Archivé de l’original le 2012-05-30 . Récupéré le 25/05/2012 .
- ^ Signes et symptômes portables . Lippincott Williams & Wilkins. 2007. p. 465.ISBN _ 9781582556796. Archivé de l’original le 2017-11-05.
- ^ “Papules piézogènes – DermNet Nouvelle-Zélande” . www.dermnetnz.org . Archivé de l’original le 2016-11-26.
- ^ Ericson WB, Wolman R (mars 2017). “Gestion orthopédique des syndromes d’Ehlers-Danlos”. Journal américain de génétique médicale. Partie C, Séminaires en génétique médicale . 175 (1): 188–194. doi : 10.1002/ajmg.c.31551 . eISSN 1552-4876 . PMID 28192621 . S2CID 4377720 .
![icon of an open green padlock]()
![icon of an open green padlock]()
- ^ a b Levy HP, Adam MP, Ardinger HH, Pagon RA, Wallace SE, Bean LJH, Stephens K, Amemiya A (1993). Adam MP, Ardinger HH, Pagon RA, Wallace SE, Bean LJ, Stephens K, Amemiya A (eds.). “Syndrome d’Ehlers-Danlos hypermobile” . GeneReviews . Université de Washington, Seattle. PMID 20301456 .
- ^ un b Camerota F, Castori M, Celletti C, Colotto M, Amato S, Colella A, et al. (juillet 2014). “Anomalies de la fréquence cardiaque, de la conduction et des ultrasons chez les adultes atteints du syndrome d’hypermobilité articulaire/syndrome d’Ehlers-Danlos, type d’hypermobilité” . Rhumatologie Clinique . 33 (7): 981–987. doi : 10.1007/s10067-014-2618-y . PMID 24752348 . S2CID 32745869 .
- ^ Wenstrup RJ, et al. (2001). Les syndromes d’Ehlers-Danlos : gestion des syndromes génétiques . p. 131–149.
- ^ Grigoriou E, Boris JR, Dormans JP (février 2015). “Syndrome de tachycardie orthostatique posturale (POTS) : association avec le syndrome d’Ehlers-Danlos et considérations orthopédiques” . Orthopédie clinique et recherche connexe . 473 (2): 722–728. doi : 10.1007/s11999-014-3898-x . eISSN 1528-1132 . PMC 4294907 . PMID 25156902 .
- ^ Hakim A, O’Callaghan C, De Wandele I, Stiles L, Pocinki A, Rowe P (mars 2017). “Dysfonctionnement autonome cardiovasculaire dans le syndrome d’Ehlers-Danlos-type hypermobile”. Journal américain de génétique médicale. Partie C, Séminaires en génétique médicale . 175 (1): 168–174. doi : 10.1002/ajmg.c.31543 . PMID 28160388 . S2CID 4439857 .
![icon of an open green padlock]()
![icon of an open green padlock]()
- ^ Raffetto JD, Khalil RA (avril 2008). “Mécanismes de formation de varices : dysfonctionnement valvulaire et dilatation de la paroi” (PDF) . Phlébologie . 23 (2): 85–98. doi : 10.1258/phleb.2007.007027 . PMID 18453484 . S2CID 33320026 .
- ↑ Zeitoun JD, Lefèvre JH, de Parades V, Séjourné C, Sobhani I, Coffin B, Hamonet C (novembre 2013). “Symptômes digestifs fonctionnels et qualité de vie des patients atteints de syndromes d’Ehlers-Danlos : résultats d’une étude de cohorte nationale sur 134 patients” . PLOS ONE . 8 (11) : e80321. Bibcode : 2013PLoSO…880321Z . doi : 10.1371/journal.pone.0080321 . eISSN 1932-6203 . PMC 3838387 . PMID 24278273 .
- ^ Brockway L (avril 2016). “Manifestations gastro-intestinales du syndrome d’Ehlers-Danlos (type hypermobilité)” . Ehlers–Danlos Assistance Royaume-Uni. Archivé de l’original le 14/11/2016.
- ^ “Syndrome d’Ehlers-Danlos” . Causes sous-jacentes de la dysautonomie . Dysautonomie International. 2012. Archivé de l’original le 18/12/2014.
- ^ Létourneau Y, Pérusse R, Buithieu H (juin 2001). “Manifestations orales du syndrome d’Ehlers-Danlos” . Revue . 67 (6): 330–334. PMID 11450296 . Archivé de l’original le 15/12/2016.
- ^ “Syndrome d’Ehlers-Danlos: Définition de” . Réponses.com. Archivé de l’original le 2014-03-06 . Récupéré le 27/02/2014 .
- ^ Arendt-Nielsen L. “Les patients souffrant du syndrome d’Ehlers Danlos de type III ne répondent pas aux anesthésiques locaux” . Archivé de l’original le 2015-04-05.
- ^ Castori M, Voermans NC (octobre 2014). “Manifestations neurologiques du ou des syndromes d’Ehlers-Danlos : un examen” . Journal iranien de neurologie . 13 (4): 190-208. PMC 4300794 . PMID 25632331 .
- ^ Encyclopédie MedlinePlus : Syndrome d’Ehlers-Danlos
- ^ Seneviratne SL, Maitland A, Afrin L (mars 2017). “Troubles des mastocytes dans le syndrome d’Ehlers-Danlos”. Journal américain de génétique médicale. Partie C, Séminaires en génétique médicale . 175 (1): 226–236. doi : 10.1002/ajmg.c.31555 . PMID 28261938 . S2CID 4438476 .
- ^ Lind J, Wallenburg HC (avril 2002). « Grossesse et syndrome d’Ehlers-Danlos : une étude rétrospective dans une population néerlandaise » . Acta Obstetricia et Gynecologica Scandinavica . 81 (4): 293–300. doi : 10.1034/j.1600-0412.2002.810403.x . manche : 1765/72381 . PMID 11952457 . S2CID 39943713 .
![icon of an open green padlock]()
![icon of an open green padlock]()
- ^ “Syndromes d’Ehlers Danlos” . NORD (Organisation Nationale des Maladies Rares) . Récupéré le 11 novembre 2019 .
- ^ “Le syndrome d’Ehlers-Danilo – Le rôle du collagène dans l’œil – Information” . Récupéré le 06/07/2019 .
- ^ Henderson F (2015). « Indices d’instabilité cranio-vertébrale » . Recherche financée . Fondation Chiari & Syringomyélie. Archivé de l’original le 16/09/2016.
- ^ Henderson, Fraser C.; Austin, Claudiu; Benzel, Edouard; Bolognaise, Paolo; Ellenbogen, Richard; Francomano, Clair A.; Ireton, Candace ; Klinge, Pétra ; Koby, Myles; Longtemps, Donlin ; Patel, Sunil (2017). “Manifestations neurologiques et vertébrales des syndromes d’Ehlers-Danlos” . American Journal of Medical Genetics Part C: Séminaires en génétique médicale . 175 (1): 195–211. doi : 10.1002/ajmg.c.31549 . ISSN 1552-4876 . PMID 28220607 . S2CID 4438281 .
- ^ Carbone, L.; Tylavsky, FA; Bush, AJ ; Koo, W.; Orwoll, E.; En ligneCheng, S. (2000). “Densité osseuse dans le syndrome d’Ehlers-Danlos” . Ostéoporose International . 11 (5): 388–392. doi : 10.1007/s001980070104 . ISSN 0937-941X . PMID 10912839 . S2CID 441230 .
- ^ Nijs, J.; Van Essche, E.; De Munck, M.; Dequeker, J. (2000-07-01). “Mesures échographiques, axiales et périphériques chez les patientes atteintes du syndrome d’hypermobilité bénigne” . Tissu calcifié International . 67 (1): 37–40. doi : 10.1007/s00223001093 . ISSN 1432-0827 . PMID 10908410 . S2CID 21083444 .
- ^ Baeza-Velasco C (2021). “Atypismes neurodéveloppementaux dans le contexte de l’hypermobilité articulaire, des troubles du spectre de l’hypermobilité et des syndromes d’Ehlers-Danlos” . Journal américain de génétique médicale. Partie C, Séminaires en génétique médicale . 187 (4): 491–499. doi : 10.1002/ajmg.c.31946 . PMID 34741402 .
- ^ Santschi DR (3 avril 2008). “La mère de Redlands, piquée par de faux soupçons, réclame des comptes dans les enquêtes sur la maltraitance d’enfants” . L’entreprise de presse . Archivé de l’original le 28 février 2009.
- ^ un bcde Chopra , Pradeep ; Tinkle, Brad ; Hamonnet, Claude; Broc, Isabelle; Gompel, Anne; Bulbena, Antonio; Francomano, Clair (2017). “Gestion de la douleur dans les syndromes d’Ehlers-Danlos” . American Journal of Medical Genetics Part C: Séminaires en génétique médicale . 175 (1): 212–219. doi : 10.1002/ajmg.c.31554 . ISSN 1552-4876 . PMID 28186390 . S2CID 4433630 .
- ^ Chopra P, Tinkle B, Hamonet C, Brock I, Gompel A, Bulbena A, Francomano C (mars 2017). “Gestion de la douleur dans les syndromes d’Ehlers-Danlos”. Journal américain de génétique médicale. Partie C, Séminaires en génétique médicale . 175 (1): 212–219. doi : 10.1002/ajmg.c.31554 . PMID 28186390 . S2CID 4433630 .
![icon of an open green padlock]()
![icon of an open green padlock]()
- ^ “Types EDS | La Société Ehlers Danlos” . La Société Ehlers Danlos . Archivé de l’original le 2017-06-24 . Récupéré le 22/05/2017 .
- ^ Sobey G (janvier 2015). “Syndrome d’Ehlers-Danlos : comment diagnostiquer et quand effectuer des tests génétiques” . Archives des maladies de l’enfance . 100 (1): 57–61. doi : 10.1136/archdischild-2013-304822 . PMID 24994860 . S2CID 11660992 .
![icon of an open green padlock]()
![icon of an open green padlock]()
- ^ Ross J, Grahame R (janvier 2011). “Syndrome d’hypermobilité articulaire”. BMJ . 342 : c7167. doi : 10.1136/bmj.c7167 . PMID 21252103 . S2CID 1284069 .
- ^ Castori M (2012). “Syndrome d’Ehlers-danlos, type d’hypermobilité : un trouble du tissu conjonctif héréditaire sous-diagnostiqué avec des manifestations mucocutanées, articulaires et systémiques” . ISRN Dermatologie . 2012 : 751768. doi : 10.5402/2012/751768 . PMC 3512326 . PMID 23227356 .
- ^ “Les types d’EDS” . La Société Ehlers Danlos . Récupéré le 17/10/2018 .
- ^ “Diagnostic différentiel” . www.loeysdietz.org . Archivé de l’original le 2017-06-23.
- ^ “Syndrome d’Ehlers-Danlos” . Rarediseases.about.com. 2006-05-25. Archivé de l’original le 12/04/2014 . Récupéré le 27/02/2014 .
- ^ “Pseudoxanthome élastique” . Génétique Accueil Référence . Récupéré le 17/04/2018 .
- ^ un bcdef ” Les Types d’ EDS ” . La Société Ehlers Danlos . Récupéré le 06/11/2019 .
- ^ Carter, Kane. « EDS hypermobile et troubles du spectre de l’hypermobilité » . Ehlers-Danlos Assistance Royaume-Uni .
- ^ “Grossesse, naissance, alimentation et syndrome d’Ehlers-Danlos hypermobile / troubles du spectre d’hypermobilité – Le soutien Ehlers-Danlos UK” . Récupéré le 22/11/2019 .
- ^ https://www.ehlers-danlos.com/hedge/ . {{cite web}}: Manquant ou vide |title=( aide )
- ^ https://www.thenorrislab.com/home . {{cite web}}: Manquant ou vide |title=( aide )
- ^ Gensemer (2021). “Syndromes hypermobiles d’Ehlers-Danlos: phénotypes complexes, diagnostics difficiles et causes mal comprises”. {{cite journal}}: Cite journal requires |journal= (help)
- ^ Narcisi (1994). “Une famille avec le syndrome d’Ehlers-Danlos de type III/syndrome d’hypermobilité articulaire a une substitution de la glycine 637 à la sérine dans le collagène de type III “. Hum Mol Genet .
- ^ Lyon (2016). “La tryptase sérique basale élevée identifie un trouble multisystémique associé à un nombre accru de copies de TPSAB1”. Nat Genet .
- ^ Guo (2021). “DZIP1 régule le développement de la valve cardiaque des mammifères par un mécanisme Cby1-β-caténine”. {{cite journal}}: Cite journal requires |journal= (help)
- ^ Moore (2021). « PDGFRα : expression et fonction pendant la morphogénèse de la valve mitrale ». {{cite journal}}: Cite journal requires |journal= (help)
- ^ Malfait F, Wenstrup R, De Paepe A (1993). Adam MP, Ardinger HH, Pagon RA, Wallace SE, Bean LJ, Stephens K, Amemiya A (eds.). Syndrome d’Ehlers-Danlos classique . GeneReviews . Université de Washington, Seattle. PMID 20301422 . Récupéré le 03/06/2019 .
- ^ Kapferer-Seebacher I, Lundberg P, Malfait F, Zschocke J (novembre 2017). “Manifestations parodontales des syndromes d’Ehlers-Danlos: Une revue systématique”. Journal de parodontologie clinique . 44 (11): 1088–1100. doi : 10.1111/jcpe.12807 . PMID 28836281 . S2CID 36252998 .
- ^ Castori M (2012). “Syndrome d’Ehlers-Danlos, type d’hypermobilité : un trouble du tissu conjonctif héréditaire sous-diagnostiqué avec des manifestations mucocutanées, articulaires et systémiques” . ISRN Dermatologie . 2012 : 751768. doi : 10.5402/2012/751768 . PMC 3512326 . PMID 23227356 .
- ^ Rakhmanov Y, PE maltais, Bruson A, Castori M, Beccari T, Dundar M, Bertelli M (2018-09-01). “Tests génétiques pour le syndrome d’Ehlers-Danlos vasculaire et d’autres variantes avec fragilité des artères moyennes” . Le Journal EuroBiotech . 2 (s1) : 42–44. doi : 10.2478/ebtj-2018-0034 . ISSN 2564-615X . S2CID 86589984 .
- ^ un b Eagleton MJ (décembre 2016). “Complications artérielles du syndrome d’Ehlers-Danlos vasculaire” . Journal de chirurgie vasculaire . 64 (6): 1869-1880. doi : 10.1016/j.jvs.2016.06.120 . PMID 27687326 .
![open access]()
![open access]()
- ^ “Syndrome d’Ehlers-Danlos cyphoscoliotique | Centre d’information sur les maladies génétiques et rares (GARD) – un programme NCATS” . rarediseases.info.nih.gov . Récupéré le 03/06/2019 .
- ^ Klaassens M, Reinstein E, Hilhorst-Hofstee Y, Schrander JJ, Malfait F, Staal H, et al. (août 2012). “Type d’arthrochalasie Ehlers-Danlos (VIIA-B) – expansion du phénotype: de la vie prénatale à l’âge adulte” . Génétique Clinique . 82 (2): 121–130. doi : 10.1111/j.1399-0004.2011.01758.x . PMC 4026000 . PMID 21801164 .
- ^ “Syndrome de Dermatosparaxis Ehlers-Danlos | Centre d’information sur les maladies génétiques et rares (GARD) – un programme NCATS” . rarediseases.info.nih.gov . Récupéré le 03/06/2019 .
- ^ un b “Syndrome de la cornée cassante | Centre d’information sur les maladies génétiques et rares (GARD) – un programme NCATS” . rarediseases.info.nih.gov . Récupéré le 03/06/2019 .
- ^ “Entrée OMIM – # 614170 – Syndrome de la cornée fragile 2; BCS2” . www.omim.org . Récupéré le 18/06/2018 .
- ^ “Syndrome spondylodysplasique d’Ehlers-Danlos | Centre d’information sur les maladies génétiques et rares (GARD) – un programme NCATS” . rarediseases.info.nih.gov . Récupéré le 22/09/2019 .
- ^ “Syndrome d’Ehlers-Danlos, type musculocontractural – Conditions – GTR – NCBI” . www.ncbi.nlm.nih.gov . Récupéré le 22/09/2019 .
- ^ Guarnieri V, Morlino S, Di Stolfo G, Mastroianno S, Mazza T, Castori M (mai 2019). “Le syndrome d’Ehlers-Danlos valvulaire cardiaque est une condition bien définie due à des variantes nulles récessives dans COL1A2”. Journal américain de génétique médicale. Partie A. 179 (5): 846–851. doi : 10.1002/ajmg.a.61100 . PMID 30821104 . S2CID 73470267 .
- ^ “Physiothérapie et autogestion – Le Ehlers-Danlos Support UK” . www.ehlers-danlos.org . Récupéré le 17/04/2018 .
- ^ un bcd Rombaut L, Malfait F, De Wandele I, Cools A, Thijs Y, De Paepe A, Calders P (juillet 2011). “Médicaments, chirurgie et physiothérapie chez les patients atteints du type d’hypermobilité du syndrome d’Ehlers-Danlos” . Archives de médecine physique et de réadaptation . 92 (7): 1106-1112. doi : 10.1016/j.apmr.2011.01.016 . PMID 21636074 .
- ^ un b Woerdeman LA, Ritt MJ, Meijer B, Maas M (2000). “Problèmes de poignet chez les patients atteints du syndrome d’Ehlers-Danlos” . Journal européen de chirurgie plastique . 23 (4): 208-210. doi : 10.1007/s002380050252 . S2CID 29979747 .
- ^ Callewaert B, Malfait F, Loeys B, De Paepe A (mars 2008). “Syndromes d’Ehlers-Danlos et syndrome de Marfan”. Meilleures pratiques et recherche. Rhumatologie Clinique . 22 (1): 165–189. doi : 10.1016/j.berh.2007.12.005 . PMID 18328988 .
- ^ Génétique du syndrome d’Ehlers-Danlos ~ traitement à eMedicine
- ^ “Information d’urgence vasculaire (VEDS)” . La Société Ehlers Danlos . Récupéré le 17/04/2018 .
- ^ “Sujets dans la gestion de la douleur : gestion de la douleur chez les patients atteints de troubles de l’hypermobilité : causes fréquemment manquées de la douleur chronique” (PDF) . Sujets en gestion de la douleur .
- ^ Giroux CM, Corkett JK, Carter LM (2016). “Les impacts académiques et psychosociaux du syndrome d’Ehlers-Danlos sur les étudiants postsecondaires : une revue intégrative de la littérature” (PDF) . Journal de l’éducation postsecondaire et du handicap . 29 (4): 414.
- ^ “Gestion de la luxation / subluxation” . La Société Ehlers Danlos . Récupéré le 19/04/2022 .
- ^ un b Wiesmann T, Castori M, Malfait F, Wulf H (juillet 2014). “Recommandations pour l’anesthésie et la gestion périopératoire chez les patients atteints du ou des syndromes d’Ehlers-Danlos” . Revue Orphanet des maladies rares . 9 : 109. doi : 10.1186/s13023-014-0109-5 . PMC 4223622 . PMID 25053156 .
- ^ Parapia LA, Jackson C (avril 2008). “Syndrome d’Ehlers-Danlos – une revue historique”. Journal britannique d’hématologie . 141 (1): 32–35. doi : 10.1111/j.1365-2141.2008.06994.x . PMID 18324963 . S2CID 7809153 .
![icon of an open green padlock]()
![icon of an open green padlock]()
- ^ Directives d’anesthésie pour les orphelins harvnb error: no target: CITEREFOrphanAnesthesia_Guidelines (help)
- ^ Shirley ED, Demaio M, Bodurtha J (septembre 2012). “Syndrome d’Ehlers-danlos en orthopédie : étiologie, diagnostic et implications thérapeutiques” . Santé sportive . 4 (5): 394–403. doi : 10.1177/1941738112452385 . PMC 3435946 . PMID 23016112 .
- ^ “Que sont les syndromes d’Ehlers-Danlos?” . La Société Ehlers Danlos . Récupéré le 10/09/2019 .
- ^ Pepin M, Schwarze U, Superti-Furga A, Byers PH (mars 2000). “Caractéristiques cliniques et génétiques du syndrome d’Ehlers-Danlos de type IV, le type vasculaire”. Le New England Journal of Medicine . 342 (10): 673–680. CiteSeerX 10.1.1.603.1293 . doi : 10.1056/NEJM200003093421001 . PMID 10706896 .
![icon of an open green padlock]()
![icon of an open green padlock]()
- ^ un bcdefg Pepin M, Schwarze U, Superti – Furga A, Byers PH (mars 2000). “Caractéristiques cliniques et génétiques du syndrome d’Ehlers-Danlos de type IV, le type vasculaire”. Le New England Journal of Medicine . 342 (10): 673–680. doi : 10.1056/NEJM200003093421001 . PMID 10706896 .
- ^ “LA SOCIÉTÉ EHLERS-DANLOS EDS ET LE REGISTRE MONDIAL ET LE RÉFÉRENTIEL HSD” . Récupéré le 14/05/2022 .
- ^ “REGISTREMENT INTERNATIONAL DES PATIENTS POUR CHIARI & SYRINGOMYELIE” . Récupéré le 14/05/2022 .
- ^ “Syndrome d’Ehlers-Danlos: épidémiologie” . Medscape.com. Archivé de l’original le 2013-04-24 . Récupéré le 27/02/2014 .
- ^ “Le syndrome d’Ehlers-Danlos de type VIIc” . geneaware.clinical.bcm.edu . Archivé de l’original le 14/08/2017 . Récupéré le 24/07/2017 .
- ^ “Qu’est-ce que l’EDS | La Fondation nationale Ehlers-Danlos” . www.ednf.org . Archivé de l’original le 2016-04-26 . Récupéré le 06/01/2016 .
- ^ “Recherche d’entrée OMIM – syndrome d’Ehlers-Danlos” . www.omim.org . Récupéré le 27/04/2019 .
- ^ Yücel D (janvier 1995). “Est-ce que Paganini est né avec le phénotype 4 ou 3 du syndrome d’Ehlers-Danlos?” . Chimie clinique . 41 (1): 124–125. doi : 10.1093/clinchem/41.1.124 . PMID 7813066 .
![icon of an open green padlock]()
![icon of an open green padlock]()
- ^ “La peau la plus extensible” . Records du monde Guinness . Récupéré le 22/06/2019 .
- ^ “Houston s’attaque aux” idées préconçues “- Coronation Street News – Soaps” . Espion numérique . 2010-05-22. Archivé de l’original le 2013-05-09 . Récupéré le 27/02/2014 .
- ^ “Yvie de Drag Race ouvre bizarrement sur la vie avec la maladie d’Ehlers Danos” . www.out.com . 11 avril 2019.
- ^ Rosenberg P (30 septembre 2014). “Eric l’acteur : un éloge funèbre” . Pierre roulante . Récupéré le 23 juillet 2019 .
- ^ Gillespie, Claire (21 février 2019). ” Jameela Jamil confirme qu’elle a le syndrome d’Ehlers-Danlos ” . SOI . Récupéré le 9 août 2019 .
- ^ Ellis, Ralph (3 novembre 2019). “Lena Dunham va sur Instagram pour révéler qu’elle a le syndrome d’Ehlers-Danlos” . CNN .
- ^ Doherty, Jennifer (2019-10-05). “Syndrome d’Ehlers-Danlos: l’état de Singer Sia expliqué” . Newsweek . Récupéré le 11/11/2019 .
- ^ “Voici ce que YouTuber Annie Elainey veut que vous sachiez sur le fait d’être handicapé” . Brit + Co. 2017-09-01 . Récupéré le 11/11/2019 .
- ^ “Vivre avec un trouble peu connu d’Ehlers-Danlos a suscité l’amour de Miss Virginia pour la science” . Nouvelles de l’école de pharmacie VCU . Récupéré le 01/03/2020 .
- ^ “Publication du profil Instagram de Lorelei Lee : “S’il semble ici sur IG que j’ai toujours une autre procédure médicale, c’est parce que cela semble aussi être le cas dans la vraie vie. Vous êtes tous…” ” . Instagram.com. 2020-11-10 . Récupéré le 2022-03-03 .
- ^ “L’ancien concurrent de ‘Millionaire Matchmaker’ Trevor Jones meurt subitement” . Aujourd’hui . Récupéré le 20/10/2021 .
- ^ Scott DV (octobre 1974). “Asthénie cutanée chez un chat, ressemblant au syndrome d’Ehlers-Danlos chez l’homme”. Médecine vétérinaire, clinicienne pour petits animaux . 69 (10): 1256–1258. doi : 10.3906/vet-1203-64 . PMID 4496767 .
- ^ Scott DW (2008). “Maladies cutanées congénitales et héréditaires” . Atlas en couleurs de la dermatologie des animaux de ferme . Bibliothèque en ligne Wiley. p. 61. doi : 10.1002/9780470344460 . ISBN 9780470344460.
- ^ “Syndrome d’Ehler-Danlos (asthénie cutanée, dermatosparaxis)” . cabinet-veterinaire.com . Récupéré le 03/06/2019 .
- ^ Halper J (2014). “Troubles du tissu conjonctif chez les animaux domestiques” . Progrès de la médecine expérimentale et de la biologie . 802 : 231–240. doi : 10.1007/978-94-007-7893-1_14 . ISBN 978-94-007-7892-4. PMID 24443030 .
Liens externes
| Wikimedia Commons a des médias liés au syndrome d’ Ehlers-Danlos . |
- Syndromes d’Ehlers-Danlos à Curlie