Syndrome d’irradiation aiguë
Le syndrome d’irradiation aiguë ( ARS ), également connu sous le nom de mal des rayons ou d’empoisonnement aux rayonnements , est un ensemble d’effets sur la santé qui sont causés par l’exposition à de grandes quantités de rayonnements ionisants sur une courte période de temps. [1] Les symptômes peuvent apparaître dans l’heure qui suit l’exposition et peuvent durer plusieurs mois. [1] [3] [5] Au cours des premiers jours, les symptômes sont généralement des nausées, des vomissements et une perte d’appétit. [1] Dans les quelques heures ou semaines suivantes, il y aura quelques symptômes, qui deviendront plus tard des symptômes supplémentaires, après quoi la guérison ou la mort suivra. [1]
| Syndrome d’irradiation aiguë | |
|---|---|
| Autres noms | Empoisonnement aux radiations, maladie des radiations, toxicité des radiations |
 |
|
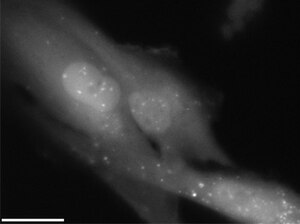
| Les radiations provoquent une dégradation cellulaire par autophagie . | |
| Spécialité | Médecine de soins intensifs |
| Les symptômes | Précoces : Nausées, vomissements, perte d’appétit [1] Postérieures : Infections, saignements, déshydratation, confusion [1] |
| Complications | Cancer [2] |
| Début habituel | En quelques jours [1] |
| Les types | Syndrome de la moelle osseuse, syndrome Gastro-intestinal, syndrome neurovasculaire [1] [3] |
| causes | De grandes quantités de rayonnements ionisants sur une courte période de temps [1] |
| Méthode diagnostique | Basé sur les antécédents d’exposition et les symptômes [4] |
| Traitement | Soins de support ( Transfusions sanguines , Antibiotiques , Facteurs de stimulation des colonies , Greffe de cellules souches ) [3] |
| Pronostic | Dépend de la dose d’exposition [4] |
| La fréquence | rares [3] |
L’ARS implique une dose totale supérieure à 0,7 Gy (70 rad ), qui provient généralement d’une source extérieure au corps, délivrée en quelques minutes. [1] Les sources d’un tel rayonnement peuvent se produire accidentellement ou intentionnellement. [6] Ils peuvent impliquer des Réacteurs nucléaires , des Cyclotrons , certains appareils utilisés dans le traitement du cancer , des Armes nucléaires ou des Armes radiologiques . [4] Il est généralement divisé en trois types : syndrome médullaire, Gastro-intestinal et neurovasculaire, le syndrome médullaire survenant entre 0,7 et 10 Gy et le syndrome neurovasculaire survenant à des doses supérieures à 50 Gy. [1][3] Les cellules les plus touchées sont généralement celles qui se divisent rapidement. [3] À fortes doses, cela provoque des dommages à l’ADN qui peuvent être irréparables. [4] Le diagnostic est basé sur les antécédents d’exposition et les symptômes. [4] Des numérations globulaires complètes (CBC) répétées peuvent indiquer la gravité de l’exposition. [1]
Le traitement du SRA consiste généralement en des Soins de support . Cela peut inclure des Transfusions sanguines , des Antibiotiques , des Facteurs de stimulation des colonies ou une Greffe de cellules souches . [3] Les matières radioactives restant sur la peau ou dans l’estomac doivent être retirées. Si l’ Iode radioactif a été inhalé ou ingéré, l’iodure de potassium est recommandé. Les complications comme la leucémie et d’autres Cancers chez ceux qui survivent sont gérées comme d’habitude. Les résultats à court terme dépendent de l’exposition à la dose. [4]
L’ARS est généralement rare. [3] Un seul événement, cependant, peut affecter un nombre relativement important de personnes. [7] Des cas notables se sont produits à la suite des bombardements atomiques d’Hiroshima et de Nagasaki et de la catastrophe de la centrale nucléaire de Tchernobyl . [1] Le SRA diffère du syndrome d’irradiation chronique , qui survient à la suite d’expositions prolongées à des doses de rayonnement relativement faibles. [8] [9]
Signes et symptômes

 Maladie des rayons
Maladie des rayons
Classiquement, l’ARS est divisée en trois présentations principales : hématopoïétique , gastro -intestinale et neuro – Vasculaire . Ces syndromes peuvent être précédés d’un prodrome . [3] La vitesse d’apparition des symptômes est liée à l’exposition aux rayonnements, des doses plus élevées entraînant un délai plus court d’apparition des symptômes. [3] Ces présentations supposent une exposition du corps entier, et nombre d’entre elles sont des marqueurs qui ne sont pas valides si le corps entier n’a pas été exposé. Chaque syndrome nécessite que le tissu présentant le syndrome lui-même soit exposé (p. ex., le syndrome Gastro-intestinal n’est pas observé si l’estomac et les intestins ne sont pas exposés aux radiations). Certains domaines concernés sont :
- Hématopoïétique. Ce syndrome est marqué par une baisse du nombre de Cellules sanguines , appelée anémie aplasique . Cela peut entraîner des infections, dues à un faible nombre de globules blancs , des saignements, dus à un manque de Plaquettes , et une anémie , due à un trop petit nombre de globules rouges en circulation. [3] Ces changements peuvent être détectés par des tests sanguins après avoir reçu une dose aiguë sur tout le corps aussi faible que 0,25 grays (25 rad), bien qu’ils puissent ne jamais être ressentis par le patient si la dose est inférieure à 1 gray (100 rad). Les traumatismes conventionnels et les brûlures résultant de l’explosion d’une bombe sont compliqués par la mauvaise cicatrisation des plaies causée par le syndrome hématopoïétique, ce qui augmente la mortalité.
- Gastro-intestinal. Ce syndrome suit souvent des doses absorbées de 6 à 30 grays (600 à 3 000 rad). [3] Les signes et symptômes de cette forme de lésion par irradiation comprennent des nausées , des vomissements , une perte d’appétit et des douleurs abdominales . [10] Les vomissements dans ce laps de temps sont un marqueur des expositions du corps entier qui se situent dans la plage fatale au-dessus de 4 grays (400 rad). Sans traitement exotique comme la greffe de moelle osseuse, la mort avec cette dose est courante, [3] due généralement plus à une infection qu’à un dysfonctionnement Gastro-intestinal.
- Neurovasculaire. Ce syndrome survient généralement à des doses absorbées supérieures à 30 grays (3 000 rad), bien qu’il puisse survenir à des doses aussi faibles que 10 grays (1 000 rad). [3] Il présente des symptômes neurologiques tels que des étourdissements , des maux de tête ou une Diminution du niveau de conscience , survenant en quelques minutes à quelques heures, avec une absence de vomissements, et est presque toujours mortel, même avec des soins intensifs agressifs. [3]
Les premiers symptômes du SRA comprennent généralement des nausées , des vomissements , des maux de tête , de la fatigue, de la fièvre et une courte période de rougeur de la peau . [3] Ces symptômes peuvent survenir à des doses de rayonnement aussi faibles que 0,35 grays (35 rad). Ces symptômes sont communs à de nombreuses maladies et peuvent ne pas, à eux seuls, indiquer un mal aigu des rayons. [3]
Effets doses
| Phase | Symptôme | Dose absorbée par le corps entier ( Gy ) | ||||
|---|---|---|---|---|---|---|
| 1–2 Gy | 2 à 6 Gy | 6 à 8 Gy | 8–30 Gy | > 30 Gy | ||
| Immédiat | Nausées et vomissements | 5 à 50 % | 50–100 % | 75–100 % | 90–100 % | 100% |
| Heure de début | 2 à 6 heures | 1 à 2 heures | 10 à 60 minutes | < 10 minutes | Minutes | |
| Durée | < 24h | 24–48h | < 48h | < 48h | N/A (les patients décèdent en < 48 h) | |
| Diarrhée | Rien | Aucun à léger (< 10 %) | Lourd (> 10%) | Lourd (> 95%) | Lourd (100%) | |
| Heure de début | — | 3–8 heures | 1 à 3 heures | < 1h | < 1h | |
| Mal de crâne | Léger | Léger à modéré (50 %) | Modéré (80 %) | Sévère (80–90 %) | Sévère (100 %) | |
| Heure de début | — | 4–24 heures | 3 à 4 heures | 1 à 2 heures | < 1h | |
| Fièvre | Rien | Augmentation modérée (10–100 %) | Modéré à sévère (100 %) | Sévère (100 %) | Sévère (100 %) | |
| Heure de début | — | 1 à 3 heures | < 1h | < 1h | < 1h | |
| Fonction SNC | Aucune déficience | Déficience cognitive 6–20 h | Déficience cognitive > 24 h | Incapacité rapide | Convulsions , tremblements , ataxie , léthargie | |
| Periode de latence | 28–31 jours | 7–28 jours | < 7 jours | Rien | Rien | |
| Maladies | Légère à modérée Leucopénie Fatigue Faiblesse |
Modérée à sévère Leucopénie Purpura Hémorragie Infections Alopécie après 3 Gy |
Leucopénie sévère Fièvre élevée Diarrhée Vomissements Étourdissements et désorientation Hypotension Perturbation électrolytique |
Nausées Vomissements Diarrhée sévère Forte fièvre Perturbation électrolytique Choc |
N/A (les patients décèdent en < 48h) | |
| Mortalité | Sans attention | 0–5 % | 5 à 95 % | 95–100 % | 100% | 100% |
| Avec soin | 0–5 % | 5 à 50 % | 50–100 % | 99–100 % | 100% | |
| La mort | 6 à 8 semaines | 4 à 6 semaines | 2 à 4 semaines | 2 jours – 2 semaines | 1 à 2 jours | |
| Source du tableau [11] |
Une personne qui se trouvait à moins de 1,6 km de l’ hypocentre de la bombe atomique Little Boy à Hiroshima , au Japon, a absorbé environ 9,46 grays (Gy) de rayonnement ionisant. [12] [13] [14] [15]
Les doses aux hypocentres des bombardements atomiques d’Hiroshima et de Nagasaki étaient respectivement de 240 et 290 Gy. [16]
Changements cutanés

 La main de Harry K. Daghlian 9 jours après qu’il ait arrêté manuellement une réaction de fission critique rapide lors d’un accident avec ce qui plus tard a obtenu le surnom de noyau démoniaque . Il a reçu une dose de 5,1 Sv , [17] ou 3,1 Gy . [18] Il est décédé 16 jours après la prise de cette photo.
La main de Harry K. Daghlian 9 jours après qu’il ait arrêté manuellement une réaction de fission critique rapide lors d’un accident avec ce qui plus tard a obtenu le surnom de noyau démoniaque . Il a reçu une dose de 5,1 Sv , [17] ou 3,1 Gy . [18] Il est décédé 16 jours après la prise de cette photo.
Le syndrome d’irradiation cutanée (SRC) fait référence aux symptômes cutanés de l’exposition aux rayonnements. [1] Quelques heures après l’irradiation, une rougeur transitoire et irrégulière (associée à des démangeaisons ) peut apparaître. Ensuite, une phase latente peut se produire et durer de quelques jours à plusieurs semaines, lorsque des rougeurs intenses, des cloques et une ulcération du site irradié sont visibles. Dans la plupart des cas, la guérison se produit par des moyens régénératifs ; cependant, de très fortes doses cutanées peuvent provoquer une perte de cheveux permanente, des glandes sébacées et sudoripares endommagées , une atrophie , une fibrose (principalement des chéloïdes ).), diminution ou augmentation de la pigmentation de la peau et ulcération ou nécrose des tissus exposés. [1] Notamment, comme on l’a vu à Tchernobyl , lorsque la peau est irradiée avec des particules bêta à haute énergie , une desquamation humide (desquamation de la peau) et des effets précoces similaires peuvent guérir, pour être suivis par l’effondrement du système Vasculaire dermique après deux mois, entraînant la perte de toute l’épaisseur de la peau exposée. [19] Cet effet avait déjà été démontré avec de la peau de porc en utilisant des sources bêta à haute énergie au Churchill Hospital Research Institute, à Oxford . [20]
Cause

 La dose et le débit de dose contribuent à la gravité du syndrome d’irradiation aiguë. Les effets du fractionnement de la dose ou des périodes de repos avant une exposition répétée déplacent également la dose DL50 vers le haut.
La dose et le débit de dose contribuent à la gravité du syndrome d’irradiation aiguë. Les effets du fractionnement de la dose ou des périodes de repos avant une exposition répétée déplacent également la dose DL50 vers le haut. 
 Comparaison des doses de rayonnement – comprend la quantité détectée lors du voyage de la Terre à Mars par le RAD sur le MSL (2011-2013). [21] [22] [23] [24]
Comparaison des doses de rayonnement – comprend la quantité détectée lors du voyage de la Terre à Mars par le RAD sur le MSL (2011-2013). [21] [22] [23] [24]
Le SRA est causé par une exposition à une forte dose de rayonnement ionisant (> ~0,1 Gy) sur une courte période (> ~0,1 Gy/h). Les rayonnements alpha et bêta ont un faible pouvoir de pénétration et sont peu susceptibles d’affecter les organes internes vitaux depuis l’extérieur du corps. Tout type de rayonnement ionisant peut provoquer des brûlures, mais les rayonnements alpha et bêta ne peuvent le faire qu’en cas de contamination radioactive ou de retombées nucléaires .se dépose sur la peau ou les vêtements de l’individu. Les rayonnements gamma et neutroniques peuvent parcourir des distances beaucoup plus grandes et pénétrer facilement dans le corps, de sorte que l’irradiation de tout le corps provoque généralement un SRA avant que les effets cutanés ne soient évidents. L’irradiation gamma locale peut provoquer des effets cutanés sans aucune maladie. Au début du XXe siècle, les radiographes étalonnaient généralement leurs appareils en irradiant leurs propres mains et en mesurant le délai d’apparition de l’ érythème . [25]
Accidentel
Une exposition accidentelle peut résulter d’un accident de criticité ou de radiothérapie . Il y a eu de nombreux accidents de criticité remontant aux essais atomiques pendant la Seconde Guerre mondiale, tandis que les appareils de radiothérapie contrôlés par ordinateur tels que Therac-25 ont joué un rôle majeur dans les accidents de radiothérapie. Le dernier des deux est causé par la défaillance du logiciel de l’équipement utilisé pour surveiller la dose de rayonnement administrée. L’erreur humaine a joué un rôle important dans les incidents d’exposition accidentelle, y compris certains des accidents de criticité, et des événements à plus grande échelle tels que la catastrophe de Tchernobyl . D’autres événements ont à voir avec des sources orphelines, dans lequel des matières radioactives sont conservées, vendues ou volées sans le savoir. L’ accident de Goiânia en est un exemple, où une source radioactive oubliée a été extraite d’un hôpital, entraînant la mort de 4 personnes de l’ARS. [26] Le vol et la tentative de vol de matières radioactives par des voleurs ignorants ont également conduit à une exposition mortelle lors d’au moins un incident. [27]
L’exposition peut également provenir de vols spatiaux de routine et d’éruptions solaires qui entraînent des effets de rayonnement sur la terre sous la forme de tempêtes solaires . Pendant les vols spatiaux, les astronautes sont exposés à la fois au rayonnement cosmique galactique (GCR) et au rayonnement des événements de particules solaires (SPE). L’exposition se produit particulièrement lors des vols au-delà de l’orbite terrestre basse (LEO). Les preuves indiquent des niveaux de rayonnement SPE passés qui auraient été mortels pour les astronautes non protégés. [28] Les niveaux de GCR qui pourraient conduire à un empoisonnement aigu aux rayonnements sont moins bien compris. [29] Cette dernière cause est plus rare, un événement pouvant survenir lors de la tempête solaire de 1859 .
Intentionnel
L’exposition intentionnelle est controversée car elle implique l’utilisation d’ Armes nucléaires , des expériences humaines ou est donnée à une victime dans un acte de meurtre. Les bombardements atomiques intentionnels d’Hiroshima et de Nagasaki ont fait des dizaines de milliers de victimes ; les survivants de ces bombardements sont connus aujourd’hui sous le nom de Hibakusha . Les Armes nucléaires émettent de grandes quantités de rayonnement thermique sous forme de lumière visible, infrarouge et ultraviolette, à laquelle l’atmosphère est largement transparente. Cet événement est également connu sous le nom de “Flash”, où la chaleur et la lumière rayonnantes sont bombardées sur la peau exposée d’une victime donnée, provoquant des brûlures par rayonnement. [30]La mort est très probable et l’empoisonnement aux radiations est presque certain si l’on est pris à découvert sans effet de masquage du terrain ou du bâtiment dans un rayon de 0 à 3 km d’une explosion aérienne de 1 mégatonne. Le risque de 50% de décès dû à l’explosion s’étend à environ 8 km d’une explosion atmosphérique de 1 mégatonne. [31]
Les tests scientifiques sur des humains effectués sans consentement sont interdits depuis 1997 aux États-Unis. Les patients sont désormais tenus de donner leur consentement éclairé et d’être informés si des expériences ont été classées. [32] Partout dans le monde, le programme nucléaire soviétique impliquait des expériences humaines à grande échelle, qui sont encore tenues secrètes par le gouvernement russe et l’ agence Rosatom . [33] [34] Les expériences humaines qui relèvent de l’ARS intentionnelle excluent celles qui impliquaient une exposition à long terme . L’activité criminelle a impliqué un meurtre et une tentative de meurtre par contact brutal de la victime avec une substance radioactive telle que le polonium ou le plutonium.
Physiopathologie
Le prédicteur de SRA le plus couramment utilisé est la dose absorbée par l’ensemble du corps . Plusieurs quantités liées, telles que la dose équivalente , la dose efficace et la dose engagée , sont utilisées pour évaluer les effets biologiques stochastiques à long terme tels que l’incidence du cancer, mais elles ne sont pas conçues pour évaluer l’ARS. [35] Pour éviter toute confusion entre ces grandeurs, la dose absorbée est mesurée en unités de grays (en SI , symbole d’unité Gy ) ou de rads (en CGS ), tandis que les autres sont mesurées en sieverts (en SI , symbole d’unité Sv ) ou rems(en CGS). 1 rad = 0,01 Gy et 1 rem = 0,01 Sv. [36]
Dans la plupart des scénarios d’exposition aiguë qui conduisent au mal des rayons, la majeure partie du rayonnement est un gamma externe du corps entier, auquel cas les doses absorbées, équivalentes et efficaces sont toutes égales. Il existe des exceptions, comme les accidents de Thérac-25 et l’ accident de criticité Cecil Kelley de 1958 , où les doses absorbées en Gy ou rad sont les seules grandeurs utiles, du fait du caractère ciblé de l’exposition de l’organisme.
Les traitements de radiothérapie sont généralement prescrits en fonction de la dose absorbée locale, qui peut être de 60 Gy ou plus. La dose est fractionnée à environ 2 Gy par jour pour un traitement “curatif”, ce qui permet aux tissus normaux de subir une réparation , leur permettant de tolérer une dose plus élevée que celle à laquelle on s’attendrait autrement. La dose à la masse tissulaire ciblée doit être moyennée sur l’ensemble de la masse corporelle, dont la plupart reçoit un rayonnement négligeable, pour arriver à une dose absorbée par l’ensemble du corps qui peut être comparée au tableau ci-dessus. [ citation nécessaire ]
Dommages à l’ADN
L’exposition à de fortes doses de rayonnement cause des dommages à l’ADN , créant plus tard des aberrations chromosomiques graves et même mortelles si elles ne sont pas réparées. Les rayonnements ionisants peuvent produire des espèces réactives de l’oxygène et endommagent directement les cellules en provoquant des événements d’ionisation localisés. Le premier est très dommageable pour l’ADN, tandis que les derniers événements créent des grappes de dommages à l’ADN. [37] [38] Ces dommages comprennent la perte de nucléobases et la rupture du squelette sucre-phosphate qui se lie aux nucléobases. L’organisation de l’ADN au niveau des histones , des nucléosomes et de la chromatine affecte également sa sensibilité aux dommages causés par les radiations . [39]Les dommages groupés, définis comme au moins deux lésions dans un tour hélicoïdal, sont particulièrement nocifs. [38] Alors que les dommages à l’ADN se produisent fréquemment et naturellement dans la cellule à partir de sources endogènes, les dommages groupés sont un effet unique de l’exposition aux rayonnements. [40] Les dommages groupés prennent plus de temps à réparer que les bris isolés et sont moins susceptibles d’être réparés. [41] Des doses de rayonnement plus importantes sont plus susceptibles de provoquer un regroupement plus serré des dommages, et les dommages étroitement localisés sont de moins en moins susceptibles d’être réparés. [38]
Les mutations somatiques ne peuvent pas être transmises du parent à la progéniture, mais ces mutations peuvent se propager dans des lignées cellulaires au sein d’un organisme. Les dommages causés par les radiations peuvent également provoquer des aberrations chromosomiques et chromatidiques, et leurs effets dépendent du stade du cycle mitotique auquel se trouve la cellule au moment de l’irradiation. Si la cellule est en interphase, alors qu’il s’agit encore d’un seul brin de chromatine, les dommages seront répliqués pendant la phase S1 du cycle cellulaire et il y aura une cassure sur les deux bras chromosomiques ; les dommages seront alors apparents dans les deux cellules filles. Si l’irradiation se produit après la réplication, un seul bras subira les dommages ; ces dommages seront apparents dans une seule cellule fille. Un chromosome endommagé peut se cycliser, se lier à un autre chromosome ou à lui-même. [42]
Diagnostic
Le diagnostic est généralement établi sur la base d’antécédents d’exposition significative aux rayonnements et de résultats cliniques appropriés. [3] Un nombre absolu de lymphocytes peut donner une estimation approximative de l’exposition aux rayonnements. [3] Le temps d’exposition aux vomissements peut également donner des estimations des niveaux d’exposition s’ils sont inférieurs à 10 Gray (1000 rad). [3]
La prévention
Un principe directeur de radioprotection est aussi bas que raisonnablement possible (ALARA). [43] Cela signifie essayer d’éviter l’exposition autant que possible et inclut les trois composantes du temps, de la distance et du blindage. [43]
Temps
Plus les êtres humains sont soumis longtemps aux radiations, plus la dose sera élevée. Le conseil du manuel de guerre nucléaire intitulé Nuclear War Survival Skills publié par Cresson Kearny aux États- Unis était que si l’on devait quitter l’abri, cela devrait être fait le plus rapidement possible pour minimiser l’exposition. [44]
Au chapitre 12, il déclare que “[r]emment mettre ou déverser des déchets à l’extérieur n’est pas dangereux une fois que les retombées ne sont plus déposées. Par exemple, supposons que l’abri se trouve dans une zone de fortes retombées et que le débit de dose à l’extérieur est de 400 roentgen ( R) par heure, assez pour donner une dose potentiellement mortelle en environ une heure à une personne exposée à l’air libre. Si une personne n’a besoin d’être exposée que 10 secondes pour vider un seau, dans ce 1/360 d’heure elle va recevoir une dose d’environ 1 R seulement. Dans des conditions de guerre, une dose supplémentaire de 1-R est peu préoccupante. En temps de paix, les travailleurs sous rayonnement apprennent à travailler le plus rapidement possible lorsqu’ils effectuent une tâche qui les expose aux rayonnements. Par exemple, la récupération d’une source radioactive doit se faire le plus rapidement possible. [ citation nécessaire]
Blindage
La matière atténue le rayonnement dans la plupart des cas, donc placer n’importe quelle masse (par exemple, du plomb, de la terre, des sacs de sable, des véhicules, de l’eau, même de l’air) entre les humains et la source réduira la dose de rayonnement. Ce n’est pas toujours le cas, cependant; des précautions doivent être prises lors de la construction d’un blindage dans un but spécifique. Par exemple, bien que les matériaux à numéro atomique élevé soient très efficaces pour protéger les photons , leur utilisation pour protéger les particules bêta peut entraîner une exposition aux rayonnements plus élevée en raison de la production de rayons X de bremsstrahlung , et donc des matériaux à faible numéro atomique sont recommandés. En outre, en utilisant un matériau avec une section efficace d’activation neutronique élevée protéger les neutrons aura pour conséquence que le matériau de protection lui-même deviendra radioactif et donc plus dangereux que s’il n’était pas présent. [ citation nécessaire ]
Il existe de nombreux types de stratégies de protection qui peuvent être utilisées pour réduire les effets de l’exposition aux rayonnements. Des équipements de protection contre la contamination interne tels que des respirateurs sont utilisés pour empêcher le dépôt interne résultant de l’inhalation et de l’ingestion de matières radioactives. L’équipement de protection cutanée, qui protège contre la contamination externe, fournit un blindage pour empêcher le dépôt de matières radioactives sur des structures externes. [45] Bien que ces mesures de protection fournissent une barrière contre le dépôt de matières radioactives, elles ne protègent pas des rayonnements gamma pénétrant de l’extérieur. Cela laisse toute personne exposée à des rayons gamma pénétrants à haut risque de SRA.
Naturellement, protéger tout le corps des rayonnements gamma à haute énergie est optimal, mais la masse requise pour fournir une atténuation adéquate rend le mouvement fonctionnel presque impossible. En cas de catastrophe radiologique, le personnel médical et de sécurité a besoin d’un équipement de protection mobile afin d’aider en toute sécurité au confinement, à l’évacuation et à de nombreux autres objectifs de sécurité publique nécessaires.
Des recherches ont été menées pour explorer la faisabilité du blindage corporel partiel, une stratégie de radioprotection qui fournit une atténuation adéquate uniquement aux organes et tissus les plus radiosensibles à l’intérieur du corps. Les lésions irréversibles des cellules souches dans la moelle osseuse sont le premier effet potentiellement mortel d’une exposition intense aux rayonnements et, par conséquent, l’un des éléments corporels les plus importants à protéger. En raison de la propriété régénératrice des cellules souches hématopoïétiques , il suffit de protéger suffisamment de moelle osseuse pour repeupler les zones exposées du corps avec l’apport blindé. [46] Ce concept permet le développement d’ équipements mobiles légers de radioprotection, qui assure une protection adéquate, reportant l’apparition du SRA à des doses d’exposition beaucoup plus élevées. Un exemple d’un tel équipement est le 360 gamma , une ceinture de radioprotection qui applique un blindage sélectif pour protéger la moelle osseuse stockée dans la région pelvienne ainsi que d’autres organes radiosensibles dans la région abdominale sans entraver la mobilité fonctionnelle.
Plus d’informations sur le blindage de la moelle osseuse peuvent être trouvées dans le “Health Physics Radiation Safety Journal” .article Waterman, Gédéon; Kase, Kenneth ; Orion, Itzhak ; Broisman, Andrey; Milstein, Oren (septembre 2017). « Blindage sélectif de la moelle osseuse : une approche pour protéger les humains contre le rayonnement gamma externe ». Physique de la Santé . 113 (3): 195–208. doi : 10.1097/HP.0000000000000688 . PMID 28749810 . S2CID 3300412 . , ou dans le rapport 2015 de l’ Organisation de coopération et de développement économiques (OCDE) et de l’Agence pour l’énergie nucléaire (AEN) : « Occupational Radiation Protection in Severe Accident Management » (PDF) .
Réduction de l’incorporation
En cas de contamination radioactive , un respirateur en élastomère , un masque anti-poussière ou de bonnes pratiques d’hygiène peuvent offrir une protection, selon la nature du contaminant. Les comprimés d’ iodure de potassium (KI) peuvent réduire le risque de cancer dans certaines situations en raison d’une absorption plus lente de l’Iode radioactif ambiant. Bien que cela ne protège aucun organe autre que la glande thyroïde, leur efficacité est encore fortement dépendante du moment de l’ingestion, qui protégerait la glande pendant une durée de vingt-quatre heures. Ils n’empêchent pas l’ARS car ils ne fournissent aucune protection contre les autres radionucléides environnementaux. [47]
Fractionnement de la dose
Si une dose intentionnelle est fractionnée en un certain nombre de doses plus petites, avec un temps de récupération entre les irradiations, la même dose totale provoque moins de mort cellulaire . Même sans interruption, une réduction du débit de dose en dessous de 0,1 Gy/h tend également à réduire la mort cellulaire. [35] Cette technique est couramment utilisée en radiothérapie. [ citation nécessaire ]
Le corps humain contient de nombreux types de cellules et un être humain peut être tué par la perte d’un seul type de cellules dans un organe vital. Pour de nombreux décès par rayonnement à court terme (3 à 30 jours), la perte de deux types importants de cellules qui se régénèrent constamment entraîne la mort. La perte des cellules formant les globules sanguins ( moelle osseuse ) et les cellules du système digestif ( microvillosités , qui font partie de la paroi des intestins ) est fatale. [ citation nécessaire ]
La gestion

 Effet des soins médicaux sur le syndrome d’irradiation aiguë
Effet des soins médicaux sur le syndrome d’irradiation aiguë
Le traitement implique généralement des soins de soutien avec d’éventuelles mesures symptomatiques employées. Le premier implique l’utilisation possible d’ Antibiotiques , de produits sanguins , de Facteurs de stimulation des colonies et de Greffe de cellules souches . [3]
Antimicrobiens
Il existe une relation directe entre le degré de neutropénie qui apparaît après une exposition aux rayonnements et le risque accru de développer une infection. Puisqu’il n’y a pas d’études contrôlées d’intervention thérapeutique chez l’homme, la plupart des recommandations actuelles sont basées sur la recherche animale. [ citation nécessaire ]
Le traitement d’une infection avérée ou suspectée suite à une exposition aux radiations (caractérisée par une neutropénie et de la fièvre) est similaire à celui utilisé pour les autres patients neutropéniques fébriles. Cependant, il existe des différences importantes entre les deux conditions. Les personnes qui développent une neutropénie après une exposition aux rayonnements sont également susceptibles de subir des lésions d’irradiation dans d’autres tissus, tels que le tractus Gastro-intestinal, les poumons et le système nerveux central. Ces patients peuvent nécessiter des interventions thérapeutiques non nécessaires chez d’autres types de patients neutropéniques. La réponse des animaux irradiés à la thérapie antimicrobienne peut être imprévisible, comme cela a été mis en évidence dans des études expérimentales où le métronidazole [48] et la péfloxacine [49]thérapeutiques étaient préjudiciables.
Les antimicrobiens qui réduisent le nombre de la composante anaérobie stricte de la flore intestinale (c’est-à-dire le métronidazole ) ne doivent généralement pas être administrés car ils peuvent augmenter l’infection systémique par des bactéries aérobies ou facultatives, facilitant ainsi la mortalité après irradiation. [50]
Un régime empirique d’antimicrobiens doit être choisi en fonction du schéma de sensibilité bactérienne et des infections nosocomiales dans la zone et le centre médical touchés et du degré de neutropénie . Un traitement empirique à large spectre (voir ci-dessous pour les choix) avec des doses élevées d’un ou plusieurs Antibiotiques doit être initié dès l’apparition de la fièvre. Ces antimicrobiens devraient viser l’éradication des bacilles aérobies à Gram négatif (c.-à-d. Enterobacteriace, Pseudomonas) qui représentent plus des trois quarts des isolats causant une septicémie. Étant donné que les bactéries Gram-positives aérobies et facultatives (principalement les streptocoques alpha-hémolytiques) provoquent une septicémie chez environ un quart des victimes, une couverture pour ces organismes peut également être nécessaire. [51]
Un plan de prise en charge standardisé pour les personnes atteintes de neutropénie et de fièvre doit être élaboré. Les schémas thérapeutiques empiriques contiennent des Antibiotiques largement actifs contre les bactéries aérobies à Gram négatif ( quinolones : c’est-à-dire ciprofloxacine , lévofloxacine , une céphalosporine de troisième ou quatrième génération avec une couverture pseudomonale : par exemple, céfépime , ceftazidime ou un aminoglycoside : c’est-à-dire gentamicine , amikacine ). [52]
Pronostic
Le pronostic de l’ARS dépend de la dose d’exposition, tout ce qui dépasse 8 Gy étant presque toujours mortel, même avec des soins médicaux. [4] [53] Les brûlures par rayonnement dues à des expositions de niveau inférieur se manifestent généralement après 2 mois, tandis que les réactions des brûlures se produisent des mois à des années après la radiothérapie. [54] [55] Les complications de l’ARS incluent un risque accru de développer un cancer radio-induit plus tard dans la vie. Selon le modèle linéaire sans seuil controversé mais couramment appliqué, toute exposition aux rayonnements ionisants, même à des doses trop faibles pour produire des symptômes de maladie des rayonnements, peut induire un cancer en raison de dommages cellulaires et génétiques. La probabilité de développer un cancer est une fonction linéaire par rapport à la dose de rayonnement efficace . Le cancer radiologique peut survenir après une exposition aux rayonnements ionisants après une période de latence moyenne de 20 à 40 ans. [56] [54]
Histoire
Les effets aigus des rayonnements ionisants ont été observés pour la première fois lorsque Wilhelm Röntgen a intentionnellement soumis ses doigts à des rayons X en 1895. Il a publié ses observations concernant les brûlures qui se sont développées et qui ont finalement guéri et les a attribuées à tort à l’ozone. Röntgen pensait que le radical libre produit dans l’air par les rayons X de l’ozone en était la cause, mais d’autres radicaux libres produits dans le corps sont maintenant considérés comme plus importants. David Walsh a établi pour la première fois les symptômes du mal des rayons en 1897. [57]
L’ingestion de matières radioactives a causé de nombreux Cancers radio-induits dans les années 1930, mais personne n’a été exposé à des doses suffisamment élevées à des taux suffisamment élevés pour provoquer le SRA.
Les bombardements atomiques d’Hiroshima et de Nagasaki ont entraîné de fortes doses aiguës de rayonnement pour un grand nombre de Japonais, permettant une meilleure compréhension de ses symptômes et de ses dangers. Le chirurgien de l’hôpital de la Croix-Rouge, Terufumi Sasaki, a mené des recherches intensives sur le syndrome dans les semaines et les mois qui ont suivi les attentats d’Hiroshima et de Nagasaki. Le Dr Sasaki et son équipe ont pu surveiller les effets des radiations chez des patients à proximité variable de l’explosion elle-même, ce qui a conduit à l’établissement de trois stades enregistrés du syndrome. Dans les 25 à 30 jours suivant l’explosion, Sasaki a remarqué une forte baisse du nombre de globules blancs et a établi cette baisse, ainsi que des symptômes de fièvre, comme normes pronostiques pour l’ARS. [58] Actrice Midori Naka, qui était présent lors du bombardement atomique d’Hiroshima, a été le premier incident d’empoisonnement aux radiations à être étudié de manière approfondie. Sa mort, le 24 août 1945, est la première mort officiellement attestée des suites de l’ARS (ou “maladie de la bombe atomique”).
Deux grandes bases de données permettent de suivre les accidents radiologiques : l’américaine ORISE REAC /TS et l’européenne IRSN ACCIRAD. Le REAC/TS fait état de 417 accidents survenus entre 1944 et 2000, causant environ 3000 cas d’ARS, dont 127 mortels. [59] L’ACCIRAD répertorie 580 accidents avec 180 morts ARS pour une période quasiment identique. [60] Les deux attentats à la bombe délibérés ne sont inclus dans aucune des bases de données, ni aucun cancer radio-induit possibleà partir de faibles doses. La comptabilisation détaillée est difficile en raison de facteurs confondants. L’ARS peut s’accompagner de blessures conventionnelles telles que des brûlures à la vapeur, ou peut survenir chez une personne souffrant d’une maladie préexistante et subissant une radiothérapie. Il peut y avoir plusieurs causes de décès et la contribution des rayonnements peut ne pas être claire. Certains documents peuvent désigner à tort les Cancers radio-induits comme un empoisonnement aux radiations, ou peuvent compter toutes les personnes surexposées comme des survivants sans mentionner s’ils présentaient des symptômes du SRA.
Cas notables
Le tableau suivant ne comprend que ceux connus pour leur tentative de survie avec ARS. Ces cas excluent le syndrome d’irradiation chronique tel qu’Albert Stevens , dans lequel le rayonnement est exposé à un sujet donné pendant une longue durée. La colonne “résultat” représente le temps d’exposition jusqu’au moment du décès attribué aux effets à court et à long terme attribués à l’exposition initiale. Comme l’ARS est mesuré par une dose absorbée par le corps entier , la colonne “exposition” ne comprend que les unités de Gray (Gy).
| Date | Nom | Exposition ( Gy ) | Incident/accident | Résultat |
|---|---|---|---|---|
| 21 août 1945 | Harry Daghlian | 3,1 Gy [18] | Accident de criticité Harry Daghlian | 04Mort en 25 jours |
| 21 mai 1946 | Louis Slotin | 11 Gy [61] | Accident de criticité Slotin | 02Mort en 9 jours |
| Alvin C. Graves | 1,9 Gy [18] | 05Mort à 19 ans | ||
| 30 décembre 1958 | Cécile Kelley | 36 Gy [62] | Accident de criticité de Cecil Kelley | 01Mort en 38 heures |
| 26 avril 1986 | Alexandre Akimov | 15 Gy [63] | Catastrophe de Tchernobyl | 03Mort en 14 jours |
Autres animaux
Des milliers d’expériences scientifiques ont été réalisées pour étudier l’ARS chez les animaux. [ citation nécessaire ] Il existe un guide simple pour prédire la survie et la mort chez les mammifères, y compris les humains, suite aux effets aigus de l’inhalation de particules radioactives. [64]
Voir également
-
![]()
![]() Portail de la technologie nucléaire
Portail de la technologie nucléaire
- 5-androstènediol
- Effets biologiques des rayonnements ionisants
- Effets biologiques des rayonnements sur l’épigénome
- CBLB502
- Ex-Rad
- Liste des accidents nucléaires civils
- Liste des accidents nucléaires militaires
- Terrorisme nucléaire
- Ordres de grandeur (rayonnement)
- Atoll de Rongelap
Références
- ^ un bcdefghijklmno ” Une fiche d’ information pour les médecins ” . _ _ _ _ _ CDC . CDC Radiation Emergencies Acute Radiation Syndrome. 22 avril 2019 . Récupéré le 17 mai 2019 .
- ^ “Beir VII: Risques pour la santé liés à l’exposition à de faibles niveaux de rayonnement ionisant” (PDF) . L’Académie Nationale . Archivé de l’original (PDF) le 2020-03-07 . Récupéré le 02/12/2019 .
- ^ un bcd e f g h i j k l m n o p q r s t u Donnelly , EH ; Nemhauser, JB; Smith, JM; Kazzi, ZN; Farfan, EB ; Chang, AS ; Naeem, SF (juin 2010). “Syndrome aigu d’irradiation : bilan et prise en charge” . Journal médical du sud . 103 (6) : 541–6. doi : 10.1097/SMJ.0b013e3181ddd571 . PMID 20710137 . S2CID 45670675 .
- ^ un bcdefg ” Le mal des radiations ” . Organisation nationale des maladies rares . Récupéré le 6 juin 2019 .
- ^ Xiao M, Whitnall MH (janvier 2009). « Contre-mesures pharmacologiques pour le syndrome de rayonnement aigu ». Curr Mol Pharmacol . 2 (1): 122–133. doi : 10.2174/1874467210902010122 . PMID 20021452 .
- ^ Chao, NJ (avril 2007). “Exposition accidentelle ou intentionnelle aux rayonnements ionisants : biodosimétrie et options de traitement”. Hématologie expérimentale . 35 (4 Supplément 1) : 24–7. doi : 10.1016/j.exphem.2007.01.008 . PMID 17379083 .
- ^ Acosta, R; Warrington, SJ (janvier 2019). “Syndrome de rayonnement”. PMID 28722960 . {{cite journal}}:Cite journal requires |journal= (help)
- ^ Akleyev, Alexandre V. (2014). “chronic%20radiation%20syndrome”&pg=PA1 Syndrome d’irradiation chronique . Springer Science et médias d’affaires. p. 1. ISBN 9783642451171.
- ^ Gusev, Igor; Guskova, Angelina ; En ligneMettler, Fred A. (2001). Gestion médicale des accidents radiologiques . Presse CRC. p. 18. ISBN 9781420037197.
- ^ Christensen DM, Iddins CJ, Sugarman SL (février 2014). “Blessures et maladies liées aux rayonnements ionisants”. Emerg Med Clin North Am . 32 (1): 245–265. doi : 10.1016/j.emc.2013.10.002 . PMID 24275177 .
- ^ “Exposition aux rayonnements et contamination – Blessures; Empoisonnement – Édition professionnelle du Manuel Merck” . Édition professionnelle des manuels Merck . Récupéré le 06/09/2017 .
- ^ Geggel, Laura (2018-05-01). “L’os humain révèle la quantité de rayonnement émis par la bombe d’Hiroshima – et c’est stupéfiant” . livescience.com . Récupéré le 27/12/2019 .
- ^ Phillips, Kristine (2018-05-02). “Une seule mâchoire a révélé la quantité de radiation absorbée par les victimes de la bombe d’Hiroshima” . Poste de Washington . Récupéré le 27/12/2019 .
- ^ Cullings, Harry M.; Fujita, Shoichiro; Funamoto, Sachiyo; Grant, Eric J.; Kerr, George D.; Preston, Dale L. (2006). “Estimation de la dose pour les études sur les survivants de la bombe atomique: son évolution et son statut actuel”. Recherche sur les rayonnements . Société de recherche sur les radiations. 166 (1): 219-254. Bibcode : 2006RadR..166..219C . doi : 10.1667/rr3546.1 . ISSN 0033-7587 . PMID 16808610 . S2CID 32660773 .
- ^ Ozasa, Kotaro; Grant, Eric J; Kodama, Kazunori (2018-04-05). “Cohortes héritées japonaises: la cohorte de survivants de la bombe atomique de l’étude de la durée de vie et la progéniture des survivants” . Journal d’épidémiologie . Association japonaise d’épidémiologie. 28 (4): 162–169. doi : 10.2188/jea.je20170321 . ISSN 0917-5040 . PMC 5865006 . PMID 29553058 .
- ^ Holdstock, Douglas (1995). Hiroshima et Nagasaki : rétrospective et perspective . Londres Portland, ou : Frank Cass. p. 4. ISBN 978-1-135-20993-3. OCLC 872115191 .
- ^ McLaughlin, Thomas P.; Monahan, Shean P.; Pruvost, Norman L.; Frolov, Vladimir V.; Ryazanov, Boris G.; Sviridov, Victor I. (mai 2000), A Review of Criticality Accidents (PDF) , Los Alamos, New Mexico : Los Alamos National Laboratory , pp. 74–75, LA-13638, archivé (PDF) de l’original le 27 septembre , 2007 , récupéré le 21 avril 2010
- ^ un bc Hempelman , Louis Henry; Lushbaugh, Clarence C.; Voelz, George L. (19 octobre 1979). Qu’est-il arrivé aux survivants des premiers accidents nucléaires de Los Alamos ? (PDF) . Conférence sur la préparation aux accidents radiologiques. Oak Ridge : Laboratoire scientifique de Los Alamos . LA-UR-79-2802. Archivé (PDF) de l’original le 12 septembre 2014 . Consulté le 5 janvier 2013 . Les numéros de patients dans ce document ont été identifiés comme suit : 1 – Daghlian, 2 – Hemmerly, 3 – Slotin, 4 – Graves, 5 – Kline, 6 – Young, 7 – Cleary, 8 – Cieleski, 9 – Schreiber, 10 – Perlman
- ↑ La prise en charge médicale des lésions cutanées suite à une irradiation accidentelle de haut niveau, réunion du groupe consultatif de l’AIEA, septembre 1987 Paris.
- ^ Wells J; et coll. (1982), “Non-Uniform Irradiation of Skin: Criteria for limiting non-stochastic effects”, Actes du troisième symposium international de la Society for Radiological Protection , Advances in Theory and Practice, vol. 2, p. 537–542, ISBN 978-0-9508123-0-4
- ^ Kerr, Richard (31 mai 2013). “Les radiations rendront le voyage des astronautes vers Mars encore plus risqué”. Sciences . 340 (6136) : 1031. Bibcode : 2013Sci…340.1031K . doi : 10.1126/science.340.6136.1031 . PMID 23723213 .
- ^ Zeitlin, C.; et coll. (31 mai 2013). “Mesures du rayonnement de particules énergétiques en transit vers Mars sur le laboratoire scientifique de Mars”. Sciences . 340 (6136): 1080–1084. Bib code : 2013Sci …340.1080Z . doi : 10.1126/science.1235989 . PMID 23723233 . S2CID 604569 .
- ^ Chang, Kenneth (30 mai 2013). “Point de données sur le risque de rayonnement pour les voyageurs vers Mars” . New York Times . Archivé de l’original le 31 mai 2013 . Récupéré le 31 mai 2013 .
- ^ Gelling, Cristy (29 juin 2013). “Le voyage sur Mars fournirait une grande dose de rayonnement ; l’instrument Curiosity confirme les prévisions d’expositions majeures” . Actualités scientifiques . 183 (13): 8. doi : 10.1002/scin.5591831304 . Archivé de l’original le 15 juillet 2013 . Consulté le 8 juillet 2013 .
- ^ Encre, William C.; Meinhold, Charles B.; Taschner, John C. (1995). “Une brève histoire des normes de radioprotection” (PDF) . Sciences de Los Alamos (23): 116–123. Archivé (PDF) de l’original le 29 octobre 2012 . Récupéré le 12 novembre 2012 .
- ^ L’accident radiologique de Goiânia (PDF) . Vienne : Agence internationale de l’énergie atomique. 1988. ISBN 92-0-129088-8. Archivé (PDF) de l’original le 2016-03-12 . Récupéré le 22/08/2005 .
- ^ “Source orpheline de Grozny, 1999” . www.johnstonsarchive.net . Récupéré le 02/04/2022 .
- ^ “Les superfusées pourraient tuer des astronautes non protégés” . Nouveau scientifique . 21 mars 2005. Archivé de l’original le 27 mars 2015.
- ^ Conseil national de la recherche (États-Unis). Comité ad hoc sur l’environnement radiatif du système solaire et vision de la NASA pour l’exploration spatiale (2006). Les dangers des rayonnements spatiaux et la vision de l’exploration spatiale . Presse des académies nationales. doi : 10.17226/11760 . ISBN 978-0-309-10264-3. Archivé de l’original le 2010-03-28.
- ^ “Effets de la bombe nucléaire” . Les archives atomiques . solcomhouse.com. Archivé de l’original le 5 avril 2014 . Récupéré le 12 septembre 2011 .
- ^ “Gamme d’effets d’armes” . johnstonarchive.net . Récupéré le 7 mars 2022 .
- ^ “Expériences de rayonnement humain” . www.atomicheritage.org . 11 juillet 2017 . Consulté le 1er décembre 2019 .
- ^ Федоров, Юрий. « Живущие в стеклянном доме » . Радио Свобода (en russe) . Récupéré le 31/08/2015 .
- ^ “Mort lente au pays des essais nucléaires du Kazakhstan” . RadioFreeEurope/RadioLiberty . 2011-08-29 . Récupéré le 31/08/2015 .
- ^ un b ICRP (2007). “Les recommandations de 2007 de la Commission internationale de protection radiologique” . Annales de la CIPR . Publication CIPR 103. 37 (2–4). ISBN 978-0-7020-3048-2. Archivé de l’original le 16 novembre 2012 . Récupéré le 17 mai 2012 .
- ^ Les effets des Armes nucléaires (édition révisée). Département américain de la Défense. 1962. p. 579.
- ^ Yu, Y.; Cui, Y.; Niedernhofer, L.; En ligneWang, Y. (2016). “Occurrence, conséquences biologiques et pertinence pour la santé humaine des dommages à l’ADN induits par le stress oxydatif” . Recherche chimique en toxicologie . 29 (12): 2008-2039. doi : 10.1021/acs.chemrestox.6b00265 . PMC 5614522 . PMID 27989142 .
- ^ un bc Eccles , L.; O’Neill, P.; En ligneLomax, M. (2011). “Réparation retardée des dommages à l’ADN induits par les radiations : ami ou ennemi ?” . Recherche sur les mutations . 711 (1–2): 134–141. doi : 10.1016/j.mrfmmm.2010.11.003 . PMC 3112496 . PMID 21130102 .
- ^ Lavelle, C.; Foray, N. (2014). “Structure de la chromatine et dommages à l’ADN induits par les radiations : de la biologie structurale à la radiobiologie”. Journal international de biochimie et de biologie cellulaire . 49 : 84–97. doi : 10.1016/j.biocel.2014.01.012 . PMID 24486235 .
- ^ Goodhead, D. (1994). “Événements initiaux dans les effets cellulaires des rayonnements ionisants: dommages groupés dans l’ADN”. Tourillon international de biologie de rayonnement . 65 (1): 7-17. doi : 10.1080/09553009414550021 . PMID 7905912 .
- ^ Georgakilas, A.; Bennett, P.; Wilson, D.; En ligneSutherland, B. (2004). “Traitement de grappes d’ADN abasique bibrin dans des cellules hématopoïétiques humaines irradiées aux rayons gamma” . Recherche sur les acides nucléiques . 32 (18): 5609–5620. doi : 10.1093/nar/gkh871 . PMC 524283 . PMID 15494449 .
- ^ Hall, E.; En ligneGiaccia, A. (2006). Radiobiologie pour le radiobiologiste (6e éd.). Lippincott Williams & Wilkins.
- ^ un b “Sécurité de Radiation” . Centres de contrôle et de prévention des maladies . 7 décembre 2015 . Récupéré le 23 avril 2020 .
- ^ Kearny, Cresson H. (1988). Compétences de survie à la guerre nucléaire . Institut des sciences et de la médecine de l’Oregon. ISBN 978-0-942487-01-5. Archivé de l’original le 17 octobre 2017.
- ^ “Équipement de protection individuelle (EPI) en cas d’urgence radiologique” . www.remm.nlm.gov . Gestion médicale des urgences radiologiques. Archivé de l’original le 21 juin 2018 . Récupéré le 26 juin 2018 .
- ^ Waterman, Gédéon; Kase, Kenneth ; Orion, Itzhak ; Broisman, Andrey; Milstein, Oren (septembre 2017). « Blindage sélectif de la moelle osseuse ». Physique de la Santé . 113 (3): 195–208. doi : 10.1097/hp.0000000000000688 . ISSN 0017-9078 . PMID 28749810 . S2CID 3300412 .
- ^ “Le rayonnement et ses effets sur la santé” . Commission de réglementation nucléaire. Archivé de l’original le 14 octobre 2013 . Récupéré le 19 novembre 2013 .
- ^ Brook, I.; Ledney, GD (1994). “Effet de la thérapie antimicrobienne sur la flore bactérienne gastro-intestinale, l’infection et la mortalité chez les souris exposées à différentes doses d’irradiation” . Journal de chimiothérapie antimicrobienne . 33 (1): 63–74. doi : 10.1093/jac/33.1.63 . ISSN 1460-2091 . PMID 8157575 .
- ^ Patchen ML, Brook I, Elliott TB, Jackson WE (1993). “Effets indésirables de la péfloxacine chez les souris C3H/HeN irradiées : correction par thérapie au glucane” . Agents antimicrobiens et chimiothérapie . 37 (9) : 1882–1889. doi : 10.1128/AAC.37.9.1882 . ISSN 0066-4804 . PMC 188087 . PMID 8239601 .
- ^ Brook I, Walker RI, MacVittie TJ (1988). “Effet de la thérapie antimicrobienne sur la flore intestinale et l’infection bactérienne chez les souris irradiées” . Tourillon international de biologie de rayonnement . 53 (5): 709–718. doi : 10.1080/09553008814551081 . ISSN 1362-3095 . PMID 3283066 .
- ^ Brook I, Ledney D (1992). “Thérapie quinolone dans la gestion de l’infection après irradiation”. Crit Rev Microbiol . 18 (4): 18235–18246. doi : 10.3109/10408419209113516 . PMID 1524673 .
- ^ Brook I, Elliot TB, Ledney GD, Shomaker MO, Knudson GB (2004). “Gestion de l’infection post-irradiation : enseignements tirés des modèles animaux” . Médecine militaire . 169 (3): 194-197. doi : 10.7205/MILMED.169.3.194 . ISSN 0026-4075 . PMID 15080238 .
- ^ “Phases temporelles du syndrome de rayonnement aigu (ARS) – Dose> 8 Gy” . Gestion médicale des urgences radiologiques. Archivé de l’original le 28 juin 2019 . Consulté le 1er décembre 2019 .
- ^ un b James, W.; Berger, T.; En ligneElston, D. (2005). Maladies d’Andrews de la peau : dermatologie clinique (10e éd.). Saunders. ISBN 0-7216-2921-0.
- ^ Wagner, LK; McNeese, MD; Marx, MV ; Siegel, EL (1999). “Réactions cutanées sévères de la fluoroscopie interventionnelle: rapport de cas et revue de la littérature”. Radiologie . 213 (3): 773–776. doi : 10.1148/radiology.213.3.r99dc16773 . PMID 10580952 .
- ^ Gawkrodger, DJ (2004). « Cancers cutanés professionnels » . Médecine du travail . Londres. 54 (7): 458–63. doi : 10.1093/occmed/kqh098 . PMID 15486177 .
- ^ Walsh, D (31 juillet 1897). “Traumatisme des tissus profonds dû à l’exposition aux rayons Roentgen” . Journal médical britannique . 2 (1909) : 272–3. doi : 10.1136/bmj.2.1909.272 . PMC 2407341 . PMID 20757183 .
- ^ Carmichael, Ann G. (1991). Médecine : un trésor d’art et de littérature . New York : Service d’édition Harkavy. p. 376.ISBN _ 978-0-88363-991-7.
- ^ Turai, Istvan; Veress, Katalin (2001). “Accidents radiologiques : occurrence, types, conséquences, prise en charge médicale et leçons à tirer” . Journal d’Europe centrale de médecine du travail et de l’environnement . 7 (1) : 3–14. Archivé de l’original le 15 mai 2013 . Récupéré le 1er juin 2012 .
- ↑ Chambrette, V. ; Hardy, S.; Nénot, JC (2001). “Les accidents d’irradiation : Mise en place d’une base de données “ACCIRAD” à l’IPSN” (PDF) . Radioprotection . 36 (4): 477–510. doi : 10.1051/radiopro:2001105 . Archivé (PDF) de l’original le 4 mars 2016 . Récupéré le 13 juin 2012 .
- ^ Lawrence, James NP (6 octobre 1978). “Mémorandum interne sur les accidents de criticité de Los Alamos, 1945–1946, expositions du personnel”. Laboratoire scientifique de Los Alamos. Hl-78. {{cite journal}}: Cite journal requires |journal= (help)
- ^ Harold, Catherine, éd. (2009). Guide professionnel des maladies (9e éd.). Philadelphie, Pennsylvanie : Lippincott Williams & Wilkins. ISBN 978-0-7817-7899-2. OCLC 475981026 .
- ^ Serhii Plokhii (2018). Tchernobyl : l’histoire d’une catastrophe nucléaire . Livres de base. ISBN 9781541617087.
- ^ Wells, J. (1976). “Un guide sur le pronostic de survie chez les mammifères suite aux effets aigus des particules radioactives inhalées”. Journal de l’Institut des ingénieurs nucléaires . 17 (5): 126–131. ISSN 0368-2595 .
Cet article incorpore du matériel du domaine public provenant de sites Web ou de documents de l’ Institut de recherche en radiobiologie des forces armées américaines et des Centers for Disease Control and Prevention des États-Unis.
Liens externes
| Wikimedia Commons a des médias liés au syndrome d’ irradiation aiguë . |
- “Préparation aux situations d’urgence et expertise en la matière sur la gestion médicale des incidents radiologiques” . Site de formation du centre américain d’assistance aux urgences radiologiques REACts .{{cite web}}: CS1 maint: url-status (link)
- “Fiche d’information sur le syndrome d’irradiation aiguë” . Centres américains de contrôle et de prévention des maladies . Archivé de l’original le 16 juillet 2006 . Récupéré le 22 juillet 2006 .
- “L’accident de criticité à Sarov” (PDF) . Agence internationale de l’énergie atomique . 2001.– Un compte rendu bien documenté des effets biologiques d’un accident de criticité.
- “Institut de recherche en radiobiologie des forces armées” .
