Polyphénol
Les polyphénols ( / ˌ p ɒ l i ˈ f iː n oʊ l , – n ɒ l / ) sont une grande famille de composés organiques naturels caractérisés par des multiples d’ unités phénol . [1] Ils sont abondants dans les plantes et structurellement diversifiés. [1] [2] [3] Les polyphénols comprennent les flavonoïdes , l’acide tannique et l’ ellagitanin , dont certains ont été utilisés historiquement comme colorants et pourvêtements de bronzage .
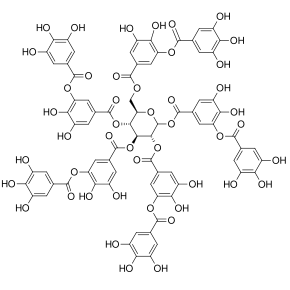 Polyphénol d’origine végétale, acide tannique, formé par estérification de dix équivalents d’ acide gallique dérivé de phénylpropanoïde en un noyau de monosaccharide (glucose) issu du métabolisme primaire
Polyphénol d’origine végétale, acide tannique, formé par estérification de dix équivalents d’ acide gallique dérivé de phénylpropanoïde en un noyau de monosaccharide (glucose) issu du métabolisme primaire  La curcumine , un composant jaune vif du curcuma ( Curcuma longa ) est un polyphénol bien étudié.
La curcumine , un composant jaune vif du curcuma ( Curcuma longa ) est un polyphénol bien étudié.
Étymologie
Le nom dérive du mot grec ancien πολύς ( polus , qui signifie “beaucoup, beaucoup”) et du mot phénol qui fait référence à une structure chimique formée en se liant à un cycle benzénoïde aromatique ( Phényle ) à un Groupe hydroxyle (-OH) tel quel. trouvé dans les alcools (d’où le suffixe -ol ). Le terme polyphénol est utilisé depuis au moins 1894. [4]
Définition
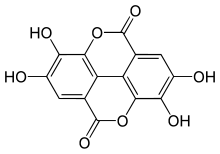
 L’acide ellagique , un polyphénol.
L’acide ellagique , un polyphénol. 
 Framboise ellagitanin , un tanin composé de 14 unités d’acide gallique autour d’un noyau de trois unités de glucose, avec deux acides galliques sous forme d’Esters simples, et les 12 restants apparaissant dans 6 unités de type acide ellagique. Des liaisons ester, éther et biaryle sont présentes, voir ci-dessous.
Framboise ellagitanin , un tanin composé de 14 unités d’acide gallique autour d’un noyau de trois unités de glucose, avec deux acides galliques sous forme d’Esters simples, et les 12 restants apparaissant dans 6 unités de type acide ellagique. Des liaisons ester, éther et biaryle sont présentes, voir ci-dessous.
Le terme polyphénol n’est pas bien défini, mais il est généralement admis qu’il s’agit de produits naturels “ayant une structure polyphénolique (c’est-à-dire plusieurs groupes Hydroxyle sur des cycles aromatiques )” comprenant quatre classes principales : “acides phénoliques, flavonoïdes, stilbènes et lignanes” . [5]
- Les flavonoïdes comprennent les flavones, les flavonols, les flavanols, les flavanones, les isoflavones, les proanthocyanidines et les anthocyanines. Les flavonoïdes particulièrement abondants dans les aliments sont la catéchine (thé, fruits), l’hespérétine (agrumes), la cyanidine (fruits rouges et baies), la daidzéine ( soja ), les proanthocyanidines (pomme, raisin, cacao) et la quercétine (oignon, thé, pommes) . [2]
- L’acide phénolique comprend l’acide caféique
- Les lignanes sont des polyphénols dérivés de la phénylalanine présents dans les graines de lin et d’autres céréales.
Définition “WBSSH”
La définition de White-Bate-Smith-Swain-Haslam (WBSSH) [6] caractérisait les caractéristiques structurelles communes aux composés phénoliques végétaux utilisés dans le tannage (c’est-à-dire les tanins). [7]
En termes de propriétés, le WBSSH décrit ainsi les polyphénols :
- composés généralement modérément solubles dans l’eau
- avec un poids moléculaire de 500 à 4000 Da
- avec > 12 groupes hydroxyles phénoliques
- avec 5 à 7 anneaux aromatiques par 1000 Da
En termes de structures, le WBSSH reconnaît deux familles structurelles qui ont ces propriétés :
- proanthocyanidines et ses dérivés
- Esters de galloyle et d’hexahydroxydiphénoyle et leurs dérivés
Définition Quideau
Selon Stéphane Quideau, le terme « polyphénol » désigne des composés issus de la voie Shikimate / phénylpropanoïde et/ou polykétide , comportant plus d’un motif phénolique et dépourvus de fonctions azotées. [ citation nécessaire ]
L’acide ellagique , une molécule au cœur de composés phénoliques naturels de tailles variables, n’est pas lui-même un polyphénol selon la définition WBSSH, mais selon la définition Quideau. L’ ellagitanin de framboise [8] , d’autre part, avec ses 14 fractions d’acide gallique (la plupart dans des composants de type acide ellagique) et plus de 40 groupes hydroxyles phénoliques, répond aux critères des deux définitions d’un polyphénol. D’autres exemples de composés qui relèvent à la fois des définitions WBSSH et Quideau comprennent le thé noir théaflavine-3-gallate illustré ci-dessous et le tanin hydrolysable, l’acide tannique . [ citation nécessaire ]

 Théaflavine-3-gallate , un polyphénol d’origine végétale, un ester d’acide gallique et un noyau de théaflavine . Il existe 9 groupes hydroxyles phénoliques et deux liaisons éther phénolique .
Théaflavine-3-gallate , un polyphénol d’origine végétale, un ester d’acide gallique et un noyau de théaflavine . Il existe 9 groupes hydroxyles phénoliques et deux liaisons éther phénolique .
Chimie
Les polyphénols sont des espèces réactives vis-à-vis de l’ Oxydation , d’où leur description comme antioxydants in vitro. [9]
Chimie structurale
Les polyphénols sont souvent des molécules plus grosses ( macromolécules ). Leur limite supérieure de poids moléculaire est d’environ 800 daltons , ce qui permet la possibilité de se diffuser rapidement à travers les membranes cellulaires afin qu’ils puissent atteindre des sites d’action intracellulaires ou rester sous forme de pigments une fois que la cellule est sénescente . Par conséquent, de nombreux polyphénols plus grands sont biosynthétisés in situ à partir de polyphénols plus petits en tanins non hydrolysables et restent non découverts dans la matrice végétale. La plupart des polyphénols contiennent des fragments phénoliques répétés de pyrocatéchol, de résorcinol, de pyrogallol et de phloroglucinol reliés par des Esters (tanins hydrolysables) ou des liaisons CC plus stables ( Tanins condensés non hydrolysables ). Proanthocyanidinessont principalement des unités polymériques de catéchine et d’ épicatéchine .

 La sous-structure C-glucoside des polyphénols est illustrée par le conjugué phénol-saccharide puerarine, un produit naturel végétal de poids moléculaire moyen. La fixation du phénol au saccharide se fait par une liaison carbone-carbone. L’ isoflavone et son système « d’anneau condensé » de benzopyrane à 10 atomes, également une caractéristique structurelle ici, sont courants dans les polyphénols.
La sous-structure C-glucoside des polyphénols est illustrée par le conjugué phénol-saccharide puerarine, un produit naturel végétal de poids moléculaire moyen. La fixation du phénol au saccharide se fait par une liaison carbone-carbone. L’ isoflavone et son système « d’anneau condensé » de benzopyrane à 10 atomes, également une caractéristique structurelle ici, sont courants dans les polyphénols.
Les polyphénols ont souvent des groupes fonctionnels au-delà des groupes Hydroxyle . Les liaisons éther – ester sont courantes, tout comme les acides carboxyliques .

 Un exemple d’un petit ellagitanin obtenu par synthèse, la tellimagrandine II , dérivé biosynthétiquement et parfois synthétiquement par jonction oxydative de deux des fragments galloyle du 1,2,3,4,6-pentagalloyl-glucose
Un exemple d’un petit ellagitanin obtenu par synthèse, la tellimagrandine II , dérivé biosynthétiquement et parfois synthétiquement par jonction oxydative de deux des fragments galloyle du 1,2,3,4,6-pentagalloyl-glucose
Chimie analytique
Les techniques d’analyse sont celles de la phytochimie : extraction , isolement, élucidation structurale , [10] puis quantification . [ citation nécessaire ]
Extraction
L’extraction des polyphénols [11] peut être réalisée à l’aide d’un solvant tel que l’eau, l’ eau chaude , le méthanol, le méthanol/acide formique, le méthanol/eau/acide acétique ou formique. L’extraction liquide-liquide peut également être effectuée ou la chromatographie à contre -courant . L’Extraction en phase solide peut également être effectuée sur des cartouches de sorbant C18. D’autres techniques sont l’extraction par ultrasons, l’extraction par reflux thermique, l’extraction assistée par micro-ondes, [12] le Dioxyde de carbone critique , [13] [14] l’extraction liquide sous pression [15] ou l’utilisation d’éthanol dans un extracteur à immersion. [16]Les conditions d’extraction (température, temps d’extraction, rapport solvant/matière première, solvant et concentrations) doivent être optimisées.
Présents principalement dans les peaux et les pépins de fruits, les niveaux élevés de polyphénols peuvent refléter uniquement la teneur mesurée en polyphénols extractibles (EPP) d’un fruit qui peut également contenir des polyphénols non extractibles. Le thé noir contient de grandes quantités de polyphénols et représente 20 % de son poids. [17]
La concentration peut être réalisée par ultrafiltration . [18] La purification peut être réalisée par Chromatographie préparative .
Techniques d’analyse 

L’acide phosphomolybdique est utilisé comme réactif pour la coloration des composés phénoliques en Chromatographie sur couche mince . Les polyphénols peuvent être étudiés par spectroscopie , notamment dans le domaine ultraviolet, par fractionnement ou chromatographie sur papier . Ils peuvent également être analysés par caractérisation chimique.
Les analyses de chimie instrumentale comprennent la séparation par chromatographie liquide à haute performance (HPLC), et plus particulièrement par chromatographie liquide en phase inverse (RPLC), pouvant être couplée à la spectrométrie de masse . [13] Les composés purifiés peuvent être identifiés au moyen de la résonance magnétique nucléaire . [ citation nécessaire ]
Analyse microscopique
Le Réactif DMACA est un colorant histologique spécifique des polyphénols utilisés dans les analyses en microscopie. L’ autofluorescence des polyphénols peut également être utilisée, notamment pour la localisation de la lignine et de la subérine . Lorsque la fluorescence des molécules elles-mêmes est insuffisante pour la visualisation par microscopie optique, le DPBA (ester 2-aminoéthylique de l’acide diphénylborique, également appelé réactif Naturstoff A) est traditionnellement utilisé, du moins en phytologie , pour améliorer le signal de fluorescence. [19]
Quantification
Le contenu polyphénolique peut être quantifié par séparation/isolement par titrage volumétrique . Un agent oxydant, le permanganate , est utilisé pour oxyder des concentrations connues d’une solution de tanin standard, produisant une courbe standard . La teneur en tanin de l’inconnu est ensuite exprimée en équivalents du tanin hydrolysable ou condensé approprié. [20]
Certaines méthodes de quantification de la teneur totale en polyphénols sont basées sur des mesures colorimétriques . Certains tests sont relativement spécifiques aux polyphénols (par exemple le test de Porter). Les phénols totaux (ou effet antioxydant) peuvent être mesurés à l’aide de la réaction de Folin-Ciocalteu . [13] Les résultats sont généralement exprimés en équivalents d’acide gallique. Les polyphénols sont rarement évalués par les technologies d’ anticorps . [21]
D’autres tests mesurent la capacité antioxydante d’une fraction. Certains utilisent le cation radical ABTS qui est réactif vis-à-vis de la plupart des antioxydants, notamment les composés phénoliques, les thiols et la vitamine C. [22] Au cours de cette réaction, le cation radical ABTS bleu est reconverti en sa forme neutre incolore. La réaction peut être contrôlée par spectrophotométrie. Ce test est souvent appelé test de capacité antioxydante équivalente Trolox (TEAC). La réactivité des différents antioxydants testés est comparée à celle du Trolox , qui est un analogue de la vitamine E.
D’autres tests de capacité antioxydante qui utilisent le Trolox comme standard comprennent le diphénylpicrylhydrazyl (DPPH), la capacité d’absorption des radicaux oxygène (ORAC), [23] les tests de capacité de réduction ferrique du plasma (FRAP) [24] ou l’inhibition de la faible concentration humaine in vitro catalysée par le cuivre. –Oxydation des lipoprotéines de densité . [25]
De nouvelles méthodes, notamment l’utilisation de biocapteurs , peuvent aider à surveiller la teneur en polyphénols des aliments. [26]
Les résultats de quantification produits par la moyenne de HPLC couplée à un détecteur à barrette de diodes sont généralement donnés sous forme de valeurs relatives plutôt qu’absolues car il y a un manque de normes disponibles dans le commerce pour toutes les molécules polyphénoliques. [ citation nécessaire ]
Applications industrielles
Certains polyphénols sont traditionnellement utilisés comme colorants . Par exemple, dans le sous-continent indien , l’ écorce de grenade , riche en tanins et autres polyphénols, ou son jus, est employée dans la teinture de tissus non synthétiques. [27]
Les polyphénols, notamment les tanins, étaient utilisés traditionnellement pour le tannage du cuir et aujourd’hui aussi comme précurseurs en chimie verte [28] notamment pour produire des plastiques ou des résines par polymérisation avec [29] ou sans l’utilisation de formaldéhyde [30] ou des adhésifs pour panneaux de particules. [31] Les objectifs sont généralement de valoriser les résidus végétaux de raisin, d’olive (appelés grignons ) ou de coques de noix de pécan laissés après transformation. [13]
Le pyrogallol et la pyrocatéchine sont parmi les plus anciens révélateurs photographiques . [32]
Biochimie
On pense que les polyphénols jouent divers rôles dans l’écologie des plantes. Ces fonctions comprennent : [33]
- Libération et suppression des hormones de croissance telles que l’ auxine .
- Écrans UV pour protéger des rayonnements ionisants et pour apporter une coloration ( pigments végétaux ). [5]
- Dissuasion des herbivores (propriétés sensorielles).
- Prévention des infections microbiennes ( phytoalexines ). [5] [34]
- Molécules de signalisation dans la maturation et d’autres processus de croissance.
Occurrence dans la nature
Les polyphénols les plus abondants sont les Tanins condensés , présents dans pratiquement toutes les familles de plantes. Les polyphénols plus gros sont souvent concentrés dans les tissus foliaires, l’épiderme, les couches d’écorce, les fleurs et les fruits, mais jouent également un rôle important dans la décomposition de la litière forestière et les cycles des nutriments dans l’écologie forestière. Les concentrations absolues de phénols totaux dans les tissus végétaux diffèrent largement selon la source de la littérature, le type de polyphénols et le dosage ; ils se situent dans la plage de 1 à 25 % de phénols et de polyphénols naturels totaux , calculés par rapport à la masse sèche des feuilles vertes. [35]
Des niveaux élevés de polyphénols dans certains bois peuvent expliquer leur préservation naturelle contre la pourriture. [36]
Le lin et Myriophyllum spicatum (une plante aquatique submergée) sécrètent des polyphénols impliqués dans les interactions allélopathiques . [37] [38]
Les polyphénols sont également présents chez les animaux. Chez les arthropodes tels que les insectes [39] et les crustacés [40] , les polyphénols jouent un rôle dans le durcissement de l’ épicuticule ( sclérotisation ). Le durcissement de la cuticule est dû à la présence d’une polyphénol oxydase . [41] Chez les crustacés, il existe une deuxième activité oxydase conduisant à la pigmentation de la cuticule . [42] Il n’y a apparemment pas de tannage aux polyphénols dans la cuticule des arachnides . [43]
Biosynthèse et métabolisme
Les polyphénols incorporent des parties plus petites et des éléments constitutifs de phénols naturels plus simples , qui proviennent de la voie des phénylpropanoïdes pour les acides phénoliques ou de la voie de l’acide shikimique pour les gallotanins et leurs analogues. Les flavonoïdes et les dérivés de l’acide caféique sont biosynthétisés à partir de la phénylalanine et du malonyl-CoA . Les gallotanins complexes se développent par l’ Oxydation in vitro du 1,2,3,4,6-pentagalloylglucose ou par des processus de dimérisation donnant des tanins hydrolysables. Pour les anthocyanidines, précurseurs de la biosynthèse des Tanins condensés, dihydroflavonol réductase et leucoanthocyanidine réductase(LAR) sont des enzymes cruciales avec l’ajout ultérieur de fragments de catéchine et d’épicatéchine pour des tanins plus gros et non hydrolysables. [44]
La forme glycosylée se développe à partir de l’activité glucosyltransférase et augmente la solubilité des polyphénols. [45]
La polyphénol oxydase (PPO) est une enzyme qui catalyse l’Oxydation des o-diphénols pour produire des o-quinones . C’est la polymérisation rapide des o-quinones pour produire des pigments polyphénoliques noirs, bruns ou rouges qui provoque le brunissement des fruits . Chez les insectes, la PPO est impliquée dans le durcissement des cuticules. [46]
Présence dans les aliments
Les polyphénols représentent jusqu’à 0,2 à 0,3 % du poids frais de nombreux fruits, raisins et baies. Consommer des portions courantes de vin, de chocolat, de légumineuses ou de thé peut également contribuer à environ un gramme de consommation par jour. [2] [47] Selon une revue de 2005 sur les polyphénols :
Les sources alimentaires les plus importantes sont les produits largement consommés en grandes quantités tels que les fruits et légumes, le thé vert, le thé noir, le vin rouge, le café, le chocolat, les olives et l’huile d’olive extra vierge. Les herbes et les épices, les noix et les algues sont également potentiellement importantes pour fournir certains polyphénols. Certains polyphénols sont spécifiques à certains aliments (flavanones dans les agrumes, isoflavones dans le soja, phloridzine dans les pommes) ; tandis que d’autres, comme la quercétine, se retrouvent dans tous les produits végétaux comme les fruits, les légumes, les céréales, les légumineuses, le thé et le vin. [48]
Certains polyphénols sont considérés comme des antinutriments – des composés qui interfèrent avec l’absorption des nutriments essentiels – en particulier le fer et d’autres ions métalliques, qui peuvent se lier aux enzymes digestives et à d’autres protéines, en particulier chez les ruminants . [49]
Dans une comparaison des méthodes de cuisson, les niveaux de phénols et de caroténoïdes dans les légumes ont été mieux conservés à la vapeur qu’à la friture . [50] Les polyphénols présents dans le vin, la bière et diverses boissons à base de jus non alcoolisées peuvent être éliminés à l’aide de collages , des substances qui sont généralement ajoutées à la fin ou vers la fin du processus de brassage. [ citation nécessaire ]
Astringence
En ce qui concerne les aliments et les boissons, la cause de l’ astringence n’est pas entièrement comprise, mais elle est mesurée chimiquement comme la capacité d’une substance à précipiter les protéines. [51]
Une revue publiée en 2005 a révélé que l’astringence augmente et que l’amertume diminue avec le degré moyen de polymérisation . Pour les polyphénols solubles dans l’eau, des poids moléculaires entre 500 et 3000 ont été signalés comme étant nécessaires pour la précipitation des protéines. Cependant, des molécules plus petites peuvent encore avoir des qualités astringentes probablement dues à la formation de complexes non précipités avec des protéines ou à la réticulation de protéines avec des phénols simples qui ont des groupes 1,2-dihydroxy ou 1,2,3-trihydroxy. [52] Les configurations flavonoïdes peuvent également entraîner des différences significatives dans les propriétés sensorielles, par exemple l’ épicatéchine est plus amère et astringente que sa catéchine isomère chirale . En revanche, les acides hydroxycinnamiques n’ont pas de qualités astringentes, mais sont amers. [53]
Effets potentiels sur la santé
Bien que des effets sur la santé puissent être attribués aux polyphénols dans les aliments, [54] le métabolisme important des polyphénols dans l’intestin et le foie, et leur devenir indéfini en tant que métabolites qui sont rapidement excrétés dans l’urine, empêchent de définir leurs effets biologiques. [2] Étant donné que le métabolisme des polyphénols ne peut être évalué in vivo, aucun apport nutritionnel de référence (ANREF) n’est établi ou recommandé. [2]
Aux États-Unis, la Food and Drug Administration (FDA) a publié des directives d’étiquetage à l’intention des fabricants selon lesquelles les polyphénols ne peuvent pas être mentionnés comme nutriments antioxydants à moins qu’il existe des preuves physiologiques pour vérifier une telle qualification et qu’une valeur DRI ait été établie. [55] [56] En outre, étant donné que les prétendues allégations de santé pour des aliments spécifiques enrichis en polyphénols restent non prouvées, [57] les déclarations de santé sur les polyphénols sur les étiquettes des produits sont interdites par la FDA [56] et l’ EFSA . [58] Cependant, au cours du 21e siècle, l’EFSA a reconnu certaines allégations de santé de produits polyphénoliques spécifiques, tels que le cacao [59] et l’huile d’olive.[60]
Par rapport aux effets des polyphénols in vitro , les fonctions possibles in vivo restent inconnues en raison 1) de l’absence de biomarqueurs validés in vivo ; [2] 2) études à long terme ne démontrant pas d’effets avec un mécanisme d’action , de sensibilité et de spécificité ou d’ efficacité ; [2] et 3) applications invalides de concentrations d’essai élevées et non physiologiques dans les études in vitro, qui sont par la suite sans pertinence pour la conception d’expériences in vivo. [48]
Voir également
- Liste des antioxydants dans les aliments
- Liste des composés phytochimiques dans les aliments
- Oligostilbénoïdes
- Phytochimie
- Protéines polyphénoliques
- Métabolites secondaires
Références
- ^ un b Quideau, SP; Deffieux, D.; Douat-Casassus, CL; Pouységu, L. (2011). “Polyphénols végétaux: propriétés chimiques, activités biologiques et synthèse”. Angewandte Chemie International Edition . 50 (3): 586–621. doi : 10.1002/anie.201000044 . PMID 21226137 .
- ^ un bcdefg ” Flavonoïdes ” . _ _ _ Centre d’information sur les micronutriments, Institut Linus Pauling, Université d’État de l’Oregon. 1 février 2016 . Récupéré le 28 octobre 2020 .
- ^ Nonaka, G. (1989). “Isolation et élucidation de la structure des tanins” (PDF) . Application pure. Chim . 61 (3): 357–360. doi : 10.1351/pac198961030357 . S2CID 84226096 .
- ^ “Polyphénol” . Merriam-Webster, Inc. 2019 . Récupéré le 23 février 2019 .
- ^ un bc Manach , Claudine; Scalbert, Augustin; Morand, Christine; Rémésy, Christian; Jiménez, Liliana (1er mai 2004). “Polyphénols : sources alimentaires et biodisponibilité” . Le tourillon américain de la nutrition clinique . 79 (5): 727–747. doi : 10.1093/ajcn/79.5.727 . ISSN 0002-9165 . PMID 15113710 .
- ^ Haslam, E.; En ligneCai, Y. (1994). “Polyphénols végétaux (tanins végétaux) : Métabolisme de l’acide gallique”. Rapports sur les produits naturels . 11 (1): 41–66. doi : 10.1039/NP9941100041 . PMID 15206456 .
- ^ Polyphénols pratiques, Edwin Haslam, 1998, ISBN 0-521-46513-3
- ^ Maladies cardiovasculaires et phytochimiques. Anonyme. C.Hamilton et al.
- ^ Santos, MA; Bonilla Venceslada, JL; Martin Martin, A; Garcia Garcia, I (2005). “Estimation de la sélectivité de l’ozone dans l’élimination des polyphénols de la vinasse”. Journal de la technologie chimique et de la biotechnologie . 80 (4): 433–438. doi : 10.1002/jctb.1222 . INIST : 16622840 .
- ^ Owen, RW; Haubner, R.; Coque, NOUS ; Erben, G.; Spiegelhalder, B.; Bartsch, H.; Haber, B. (2003). “Isolation et élucidation de la structure des principaux polyphénols individuels dans la fibre de caroube”. Toxicologie alimentaire et chimique . 41 (12): 1727-1738. doi : 10.1016/S0278-6915(03)00200-X . PMID 14563398 .
- ^ Escribano-Bailon, Maria Teresa; Santos-Buelga, Celestino (2003). “Extraction de polyphénols à partir d’aliments” (PDF) . A Santos-Buelga, Celestino; Williamson, Gary (éd.). Méthodes d’analyse des polyphénols . Société royale de chimie. p. 1–16. ISBN 978-0-85404-580-8.
- ^ Pan, X (2003). “Extraction assistée par micro-ondes des polyphénols de thé et de la caféine du thé à partir de feuilles de thé vert”. Génie chimique et transformation . 42 (2): 129-133. doi : 10.1016/S0255-2701(02)00037-5 .
- ^ un bcd Aizpurua – Olaizola , Oier; Ormazabal, Markel; Vallejo, Asier; Olivares, Maitane ; Navarro, Patricia; Etxebarria, Nestor ; Usobiaga, Aresatz (2015). “Optimisation des extractions consécutives de fluide supercritique d’acides gras et de polyphénols à partir de déchets de raisin Vitis Vinifera “. Journal des sciences alimentaires . 80 (1) : E101–107. doi : 10.1111/1750-3841.12715 . PMID 25471637 .
- ^ Palma, M; Taylor, L (1999). “Extraction de composés polyphénoliques à partir de pépins de raisin avec du dioxyde de carbone presque critique”. Journal de chromatographie A . 849 (1): 117–124. doi : 10.1016/S0021-9673(99)00569-5 . PMID 10444839 .
- ^ Alonsosalces, R; Korta, E; Barranco, A; Berrueta, L; Gallo, B; Vicente, F (2001). “Extraction liquide sous pression pour la détermination des polyphénols dans la pomme”. Journal de chromatographie A . 933 (1-2) : 37-43. doi : 10.1016/S0021-9673(01)01212-2 . PMID 11758745 .
- ^ Sineiro, J.; Domínguez, H.; Nuñez, MJ; Lema, JM (1996). “Extraction à l’éthanol des polyphénols dans un extracteur à immersion. Effet du flux pulsé”. Journal de l’American Oil Chemists’ Society . 73 (9): 1121–1125. doi : 10.1007/BF02523372 . S2CID 96009875 .
- ^ Arranz, Sara; Saura-Calixto, Fulgencio ; Shaha, Shika; En ligneKroon, Paul A. (2009). “Les teneurs élevées en polyphénols non extractibles dans les fruits suggèrent que la teneur en polyphénols des aliments végétaux a été sous-estimée”. Journal de chimie agricole et alimentaire . 57 (16): 7298–7303. doi : 10.1021/jf9016652 . manche : 10261/82508 . PMID 19637929 .
- ^ Nawaz, H; Shi, J; Mittal, G; Kakuda, Y (2006). “Extraction des polyphénols des pépins de raisin et concentration par ultrafiltration”. Technologie de séparation et de purification . 48 (2): 176–181. doi : 10.1016/j.seppur.2005.07.006 .
- ^ Ferrara BT, Thompson EP (février 2019). “Une méthode pour visualiser la fluorescence des flavonoïdes thérapeutiques in vivo dans le modèle eucaryote Dictyostelium discoideum ” . BioTechniques (Papier). 66 (2): 65–71. doi : 10.2144/btn-2018-0084 . PMID 30744410 .
![open access]()
![open access]()
- ^ Tempel, AS (1982). “Techniques de mesure du tanin”. Journal d’écologie chimique . 8 (10): 1289–1298. doi : 10.1007/BF00987762 . PMID 24414735 . S2CID 39848160 .
- ^ Gani, M.; McGuinness, BJ; Da Vies, AP (1998). “Anticorps monoclonaux contre les polyphénols de thé: Un nouvel immunoessai pour détecter les polyphénols dans les fluides biologiques”. Immunologie alimentaire et agricole . 10 : 13–22. doi : 10.1080/09540109809354964 .
- ^ Walker, Richard B.; Everette, Jace D. (2009). “Taux de réaction comparatifs de divers antioxydants avec le cation radical ABTS”. Journal de chimie agricole et alimentaire . 57 (4): 1156–1161. doi : 10.1021/jf8026765 . PMID 19199590 .
- ^ Roy, Molay K; Koide, Motoki ; Rao, Theertham P; Okubo, Tsutomu ; Ogasawara, Yutaka; Juneja, Lekh R (2010). “Comparaison des tests ORAC et DPPH pour évaluer la capacité antioxydante des infusions de thé: relation entre le polyphénol total et la teneur individuelle en catéchine”. Journal international des sciences alimentaires et de la nutrition . 61 (2): 109–124. doi : 10.3109/09637480903292601 . PMID 20109129 . S2CID 1929167 .
- ^ Pulido, R.; Bravo, L.; En ligneSaura-Calixto, F. (2000). “Activité antioxydante des polyphénols alimentaires telle que déterminée par un dosage de puissance réductrice / antioxydante ferrique modifié”. Journal de chimie agricole et alimentaire . 48 (8): 3396–3402. doi : 10.1021/jf9913458 . manche : 10261/112476 . PMID 10956123 .
- ^ Meyer, COMME; Yi, OS ; Pearson, DA; Waterhouse, AL ; Frankel, EN (1997). “Inhibition de l’Oxydation des lipoprotéines humaines de faible densité en relation avec la composition des antioxydants phénoliques dans les raisins (Vitis vinifera)”. Journal de chimie agricole et alimentaire . 45 (5): 1638-1643. doi : 10.1021/jf960721a .
- ^ Mello, L; Sotomayor, Maria Del Pilar Taboada; Kubota, Lauro Tatsuo (2003). “Biocapteur ampérométrique à base de HRP pour la détermination des polyphénols dans l’extrait de légumes”. Capteurs et actionneurs B : Chimique . 96 (3): 636–645. doi : 10.1016/j.snb.2003.07.008 .
- ^ KK Jindal; RC Sharma (2004). Tendances récentes de l’horticulture dans l’Himalaya . Edition Indus. ISBN 978-81-7387-162-7. … l’écorce d’arbre et l’écorce de fruit sont couramment utilisées dans l’ayurveda … également utilisées pour la teinture …
- ^ Polshettiwar, Vivek; En ligneVarma, Rajender S. (2008). “Synthèse plus verte et rapide d’hétérocycles bioactifs utilisant l’irradiation par micro-ondes”. Chimie pure et appliquée . 80 (4): 777–790. doi : 10.1351/pac200880040777 . S2CID 11940026 .
- ^ Hillis, NOUS; Urbach, G. (1959). “Réaction des polyphénols avec le formaldéhyde”. Journal de chimie appliquée . 9 (12): 665–673. doi : 10.1002/jctb.5010091207 .
- ↑ Fukuoka, Tokuma ; Uyama, Hiroshi; Kobayashi, Shiro (2003). “Synthèse de polyphénols de poids moléculaire ultraélevé par couplage oxydatif”. Macromolécules . 36 (22): 8213–8215. Bibcode : 2003MaMol..36.8213F . doi : 10.1021/ma034803t .
- ^ Pizzi, A.; Valenezuela, J.; En ligneWestermeyer, C. (1994). “Adhésifs à faible émission de formaldéhyde, à pressage rapide, au tanin de pin et de noix de pécan pour panneaux de particules extérieurs”. Holz Als Roh- und Werkstoff . 52 (5): 311–315. doi : 10.1007/BF02621421 . S2CID 36500389 .
- ^ Stephen G. Anchell & Bill Troop (1998). Le livre de recettes de développement de films . p. 25. ISBN 978-0240802770.
- ^ V. Lattanzio et al. (2006). « Rôle des composés phénoliques dans les mécanismes de résistance des plantes contre les pathogènes fongiques et les insectes » (et les références qui s’y trouvent). Phytochimie : Avancées de la recherche, 23–67. ISBN 81-308-0034-9 .
- ^ Huber, B; Eberl, L; Feucht, W; En lignePolster, J (2003). “Influence des polyphénols sur la formation de biofilm bactérien et la détection du quorum”. Z. Naturforsch. C. _ 58 (11–12): 879–884. doi : 10.1515/znc-2003-11-1224 . PMID 14713169 . S2CID 25764128 .
- ^ Hättenschwiler, Stephan; Vitousek, Peter M (2000). “Le rôle des polyphénols dans le cycle des nutriments de l’écosystème terrestre”. Tendances en écologie et évolution . 15 (6): 238–243. doi : 10.1016/S0169-5347(00)01861-9 . PMID 10802549 .
- ^ Hart, John H.; Hillis, NOUS (1974). “Inhibition des champignons de pourriture du bois par les stilbènes et autres polyphénols dans Eucalyptus sideroxylon”. Phytopathologie . 64 (7): 939–948. doi : 10.1094/Phyto-64-939 .
- ^ Popa, V; Dumitru, M; Volf, je ; Anghel, N (2008). “Lignine et polyphénols comme allélochimiques”. Cultures et produits industriels . 27 (2): 144-149. doi : 10.1016/j.indcrop.2007.07.019 .
- ^ Nakai, S (2000). “Polyphénols allélopathiques libérés par Myriophyllum spicatum inhibant la croissance des algues bleu-vert Microcystis aeruginosa”. Recherche sur l’eau . 34 (11): 3026–3032. doi : 10.1016/S0043-1354(00)00039-7 .
- ^ Wigglesworth, VB (1988). “La source de lipides et de polyphénols pour la cuticule des insectes : Le rôle du corps gras, des oenocytes et des oenocytoïdes”. Tissu et Cellule . 20 (6): 919–932. doi : 10.1016/0040-8166(88)90033-X . PMID 18620248 .
- ^ Dennell, R. (1947). “L’occurrence et l’importance du durcissement phénolique dans la cuticule nouvellement formée de Crustacea decapoda” . Actes de la Royal Society B: Sciences biologiques . 134 (877): 485–503. Bibcode : 1947RSPSB.134..485D . doi : 10.1098/rspb.1947.0027 . PMID 20265564 .
- ^ Locke, M.; Krishnan, N. (1971). “La distribution des phénoloxydases et des polyphénols lors de la formation de la cuticule”. Tissu et Cellule . 3 (1): 103–126. doi : 10.1016/S0040-8166(71)80034-4 . PMID 18631545 .
- ^ Krishnan, G. (septembre 1951). “Tannage phénolique et pigmentation de la cuticule chez Carcinus maenas” . Journal trimestriel de la science microscopique . 92 (19): 333–342.
- ^ Krishnan, G. (septembre 1954). “L’épicuticule d’un arachnide, Palamneus swammerdami” . Journal trimestriel de la science microscopique . 95 (31): 371–381.
- ^ Tanner, Gregory J; Francki, Kathy T; Abrahams, Sharon ; Watson, John M; Larkin, Philip J; Ashton, Anthony R (2003). “La biosynthèse des proanthocyanidines dans les plantes” . Journal de chimie biologique . 278 (34): 31647–31656. doi : 10.1074/jbc.M302783200 . PMID 12788945 .
- ^ Krasnow, MN; Murphy, TM (2004). “Activité de glucosylation des polyphénols dans les suspensions cellulaires de raisin (Vitis vinifera)”. Journal de chimie agricole et alimentaire . 52 (11): 3467–3472. doi : 10.1021/jf035234r . PMID 15161217 .
- ^ Malek, SRA (1961). “Polyphénols et leurs dérivés de quinone dans la cuticule du criquet pèlerin, Schistocerca gregaria (Forskål)”. Biochimie et physiologie comparées . 2 : 35–77. doi : 10.1016/0010-406X(61)90071-8 .
- ^ Pandey, Ko; Rizvi, SI (2009). “Polyphénols végétaux comme antioxydants alimentaires dans la santé et la maladie humaines” . Médecine Oxydative et Longévité Cellulaire . 2 (5): 270–278. doi : 10.4161/oxim.2.5.9498 . PMC 2835915 . PMID 20716914 .
- ^ un b d’Archivio, M; Filesi, C; Vari, R; Scazzocchio, B; Masella, R (2010). « Biodisponibilité des polyphénols : statut et controverses » . Journal international des sciences moléculaires . 11 (4): 1321–1342. doi : 10.3390/ijms11041321 . PMC 2871118 . PMID 20480022 .
- ^ L. Mennen; et coll. (janvier 2005). « Risques et sécurité de la consommation de polyphénols » . Suis J Clin Nutr . 81 (1): 3265–3295. doi : 10.1093/ajcn/81.1.326S . PMID 15640498 .
- ^ Miglio C, Chiavaro E, Visconti A, Fogliano V, Pellegrini N (2008). “Effets des différents modes de cuisson sur les caractéristiques nutritionnelles et physico-chimiques des légumes sélectionnés” . J Agric Food Chem . 56 (1): 139–147. doi : 10.1021/jf072304b . PMID 18069785 .
- ^ Personnel, Société sensorielle. Goûts de base : astringence Archivé le 27 septembre 2013 sur la Wayback Machine
- ^ Lesschaeve I, Noble AC (2005). « Polyphénols : facteurs influençant leurs propriétés sensorielles et leurs effets sur les préférences alimentaires et de boissons » . Suis J Clin Nutr . 81 (1) : 330S–335S. doi : 10.1093/ajcn/81.1.330S . PMID 15640499 .
- ^ Hufnagel JC, Hofmann T (2008). “Identification orosensorielle dirigée de la sensation en bouche astringente et des composés au goût amer dans le vin rouge”. J Agric Food Chem . 56 (4): 1376-1386. doi : 10.1021/jf073031n . PMID 18193832 .
- ^ Scalbert, A; Manach, C; Morand, C; Rémésy, C; Jimenez, L (2005). “Polyphénols alimentaires et prévention des maladies”. Revues critiques en science alimentaire et nutrition . 45 (4): 287–306. doi : 10.1080/1040869059096 . ISSN 1040-8398 . PMID 16047496 . S2CID 15475614 .
- ^ “Conseils pour l’industrie : étiquetage des aliments ; allégations relatives à la teneur en éléments nutritifs ; définition de” haute puissance” et définition d'”antioxydant” à utiliser dans les allégations de teneur en éléments nutritifs pour les compléments alimentaires et les aliments conventionnels ; Guide de conformité des petites entités” . Centre pour la sécurité alimentaire et la nutrition appliquée, US Food and Drug Administration. juillet 2008 . Récupéré le 2 octobre 2017 .
- ^ un b Gross, Paul (1er mars 2009). “Nouveaux rôles pour les polyphénols. Un rapport en 3 parties sur la réglementation actuelle et l’état de la science” . Monde nutraceutique.
- ^ Halliwell B (2007). “Polyphénols alimentaires : bons, mauvais ou indifférents pour la santé ?” . Res cardiovasculaire . 73 (2): 341–347. doi : 10.1016/j.cardiores.2006.10.004 . PMID 17141749 .
- ^ “Avis scientifique sur la justification des allégations de santé liées aux: flavonoïdes et acide ascorbique dans les jus de fruits, y compris les jus de baies (ID 1186); flavonoïdes d’agrumes (ID 1471); flavonoïdes de Citrus paradisi Macfad. (ID 3324, 3325); flavonoïdes (ID” . EFSA Journal . 9 (4): 2082. Avril 2011. doi : 10.2903/j.efsa.2011.2082 .
- “Les Antioxydants D’origine Alimentaire” . Agence pour la Recherche et l’Information en Fruits et Légumes (en français). Archivé de l’original le 1er juin 2017.
- ^ “Avis scientifique sur la modification de l’autorisation d’une allégation de santé relative aux flavanols de cacao et au maintien d’une vasodilatation normale dépendante de l’endothélium conformément à l’article 13, paragraphe 5, du règlement (CE) n ° 1924/2006 suite à une demande conformément à l’article 19 du règlement (CE) n° 1924/2006” . Journal de l’EFSA . 12 (5). Mai 2014. doi : 10.2903/j.efsa.2014.3654 .
- ^ “Avis scientifique sur la justification des allégations de santé liées aux polyphénols dans l’olive et la protection des particules de LDL contre les dommages oxydatifs (ID 1333, 1638, 1639, 1696, 2865), le maintien des concentrations normales de cholestérol HDL dans le sang (ID 1639), main” . Journal de l’EFSA . 9 (4): 2033. Avril 2011. doi : 10.2903/j.efsa.2011.2033 .
Liens externes
| Recherchez polyphénol dans Wiktionary, le dictionnaire gratuit. |
- Phenol-Explorer, base de données électronique sur la teneur en polyphénols des aliments
- Liste dictionnaire des formules moléculaires des phénols et polyphénols naturels
- Société dédiée à l’étude des polyphénols
