Un glucide ( / ˌ k ɑːr b oʊ ˈ h Aɪ d r eɪ t / ) est une biomolécule composée d’ atomes de carbone (C), d’hydrogène (H) et d’oxygène (O), généralement avec un rapport atomique hydrogène-oxygène de 2 : 1 (comme dans l’eau) et donc avec la formule empirique C m (H 2 O) n (où m peut ou non être différent de n). Cependant, tous les glucides ne sont pas conformes à cette définition stoechiométrique précise (par exemple, les acides uroniques , les sucres désoxy tels que le fucose ), et tous les produits chimiques qui se conforment à cette définition ne sont pas automatiquement classés comme glucides (par exemple , le formaldéhyde et l’acide acétique ).
 Le lactose est un disaccharide présent dans le lait animal. Il se compose d’une molécule de D-galactose et d’une molécule de D-glucose liées par une liaison bêta-1-4 glycosidique .
Le lactose est un disaccharide présent dans le lait animal. Il se compose d’une molécule de D-galactose et d’une molécule de D-glucose liées par une liaison bêta-1-4 glycosidique .
Le terme est le plus courant en biochimie , où il est synonyme de saccharide , un groupe qui comprend les sucres , l’amidon et la cellulose . Les saccharides sont divisés en quatre groupes chimiques : les monosaccharides , les disaccharides , les oligosaccharides et les polysaccharides . Les monosaccharides et les disaccharides, les glucides les plus petits ( de poids moléculaire inférieur ), sont communément appelés sucres. [1] Le mot saccharide vient du mot grec ancien σάκχαρον ( sákkharon), signifiant “sucre”. [2] Alors que la nomenclature scientifique des glucides est complexe, les noms des monosaccharides et des disaccharides se terminent très souvent par le suffixe -ose , dérivé originellement du glucose , du grec ancien γλεῦκος ( gleûkos ), signifiant « vin, moût ». “, et est utilisé pour presque tous les sucres, par exemple le fructose (sucre de fruits), le saccharose ( sucre de canne ou de betterave ), le ribose , l’ amylose , le lactose (sucre du lait), etc.
Les glucides jouent de nombreux rôles dans les organismes vivants. Les polysaccharides servent de réserve d’ énergie (par exemple, l’amidon et le glycogène ) et de composants structurels (par exemple, la cellulose chez les plantes et la chitine chez les arthropodes). Le ribose , un monosaccharide à 5 carbones, est un composant important des coenzymes (p. ex. ATP , FAD et NAD ) et le squelette de la molécule génétique connue sous le nom d’ ARN . Le désoxyribose apparenté est un composant de l’ADN. Les saccharides et leurs dérivés comprennent de nombreuses autres Biomolécules importantes qui jouent un rôle clé dans lasystème immunitaire , fécondation , prévention de la pathogenèse , coagulation du sang et développement . [3]
Les glucides sont au cœur de la nutrition et se trouvent dans une grande variété d’aliments naturels et transformés. L’amidon est un polysaccharide. Il est abondant dans les céréales (blé, maïs, riz), les pommes de terre, et les aliments transformés à base de farine de céréales , comme le pain , la pizza ou les pâtes. Les sucres apparaissent dans l’alimentation humaine principalement sous forme de sucre de table (saccharose, extrait de la Canne à sucre ou de la betterave à sucre ), du lactose (abondant dans le lait), du glucose et du fructose, tous deux présents naturellement dans le miel , de nombreux fruits et certains légumes. Le sucre de table, le lait ou le miel sont souvent ajoutés aux boissons et à de nombreux aliments préparés tels que la Confiture, les biscuits et les gâteaux.
La cellulose , un polysaccharide présent dans les parois cellulaires de toutes les plantes, est l’un des principaux composants des fibres alimentaires insolubles . Bien qu’elle ne soit pas digestible par l’homme, la cellulose et les fibres alimentaires insolubles aident généralement à maintenir un système digestif sain [4] en facilitant les selles . D’autres polysaccharides contenus dans les fibres alimentaires comprennent l’amidon résistant et l’ inuline , qui nourrissent certaines bactéries du microbiote du gros intestin et sont métabolisés par ces bactéries pour produire des Acides gras à chaîne courte . [5] [6]
Terminologie
Dans la littérature scientifique , le terme « glucide » A de nombreux synonymes, comme « sucre » (au sens large), « saccharide », « ose », [2] « glucide », [7] « hydrate de carbone » ou « polyhydroxy composés avec un aldéhyde ou une cétone “. Certains de ces termes, en particulier “glucides” et “sucre”, sont également utilisés avec d’autres significations.
En science alimentaire et dans de nombreux contextes informels, le terme «glucides» désigne souvent tout aliment particulièrement riche en amidon de glucides complexes (comme les céréales, le pain et les pâtes) ou en glucides simples, comme le sucre (que l’on trouve dans les bonbons, les confitures , et dessert). Cette informalité est parfois déroutante puisqu’elle confond structure chimique et digestibilité chez l’homme.
Souvent, dans les listes d’ informations nutritionnelles , telles que la base de données nationale sur les nutriments de l’USDA , le terme «glucides» (ou «glucides par différence») est utilisé pour tout autre chose que l’eau, les protéines, les graisses, les cendres et l’éthanol. [8] Cela inclut les composés chimiques tels que l’acide acétique ou lactique , qui ne sont normalement pas considérés comme des glucides. Il comprend également des fibres alimentaires qui sont des glucides mais qui n’apportent pas d’énergie alimentaire ( kilocalories) chez l’homme, même s’il est souvent inclus dans le calcul de l’énergie alimentaire totale comme s’il l’était (c’est-à-dire comme s’il s’agissait d’un glucide digestible et absorbable tel qu’un sucre). Au sens strict, le « sucre » s’applique aux glucides sucrés et solubles, dont beaucoup sont utilisés dans l’alimentation humaine.
Histoire
| Apprendre encore plus Cette section A besoin d’être agrandie . Vous pouvez aider en y ajoutant . ( janvier 2022 ) |
Structure
Autrefois, le nom “glucide” était utilisé en chimie pour tout composé de formule C m (H 2 O) n . Suite à cette définition, certains chimistes considéraient le formaldéhyde (CH 2 O) comme le glucide le plus simple, [9] tandis que d’autres revendiquaient ce titre pour le glycolaldéhyde . [dix]Aujourd’hui, le terme est généralement compris au sens de la biochimie, ce qui exclut les composés à un ou deux carbones et inclut de nombreux glucides biologiques qui s’écartent de cette formule. Par exemple, alors que les formules représentatives ci-dessus semblent capturer les glucides communément connus, les glucides omniprésents et abondants s’en écartent souvent. Par exemple, les glucides présentent souvent des groupes chimiques tels que : N -acétyle (par exemple , chitine ), sulfate (par exemple , glycosaminoglycanes ), acide carboxylique et modifications désoxy (par exemple , fucose et acide sialique ).
Les saccharides naturels sont généralement constitués de glucides simples appelés monosaccharides de formule générale (CH 2 O) n où n vaut trois ou plus. Un monosaccharide typique A la structure H–(CHOH) x (C=O)–(CHOH) y –H, c’est-à-dire un aldéhyde ou une cétone avec de nombreux groupes Hydroxyle ajoutés, généralement un sur chaque atome de carbone qui ne fait pas partie du fonction aldéhyde ou cétone . Des exemples de monosaccharides sont le glucose , le fructose et les glycéraldéhydes .. Cependant, certaines substances biologiques communément appelées “monosaccharides” ne sont pas conformes à cette formule (par exemple , les acides uroniques et les désoxy-sucres tels que le fucose ) et il existe de nombreux produits chimiques qui se conforment à cette formule mais ne sont pas considérés comme des monosaccharides (par exemple, le formaldéhyde CH 2 O et inositol (CH 2 O) 6 ). [11]
La forme à Chaîne ouverte d’un monosaccharide coexiste souvent avec une forme en anneau fermé où le carbone du groupe carbonyle aldéhyde / cétone (C = O) et le groupe Hydroxyle (–OH) réagissent en formant un hémiacétal avec un nouveau pont C – O – C.
Les monosaccharides peuvent être liés ensemble dans ce qu’on appelle des polysaccharides (ou oligosaccharides ) d’une grande variété de façons. De nombreux glucides contiennent une ou plusieurs unités monosaccharidiques modifiées dont un ou plusieurs groupes ont été remplacés ou supprimés. Par exemple, le désoxyribose , un composant de l’ADN , est une version modifiée du ribose ; la chitine est composée d’unités répétitives de N-acétyl glucosamine , une forme de glucose contenant de l’azote .
Division
Les glucides sont les polyhydroxy aldéhydes, les cétones, les alcools, les acides, leurs dérivés simples et leurs polymères ayant des liaisons de type acétal. Ils peuvent être classés selon leur degré de polymérisation , et peuvent être divisés initialement en trois groupes principaux, à savoir les sucres, les oligosaccharides et les polysaccharides. [12]
| Classe (degré de polymérisation) |
Sous-groupe | Composants |
|---|---|---|
| Sucres (1–2) | Monosaccharides | Glucose , galactose , fructose , xylose |
| Disaccharides | Saccharose , lactose , maltose , isomaltulose , tréhalose | |
| Polyols | Sorbitol , mannitol | |
| Oligosaccharides (3–9) | Malto-oligosaccharides | Maltodextrines |
| Autres oligosaccharides | Raffinose , stachyose , fructo-oligosaccharides | |
| Polysaccharides (>9) | Amidon | Amylose , amylopectine , amidons modifiés |
| Polysaccharides non amylacés | Glycogène , Cellulose , Hémicellulose , Pectines , Hydrocolloïdes |
Monosaccharides

 Le D-glucose est un Aldohexose de formule (C·H 2 O) 6 . Les atomes rouges mettent en évidence le groupe aldéhyde et les atomes bleus mettent en évidence le centre asymétrique le plus éloigné de l’aldéhyde; parce que ce -OH est à droite de la projection de Fischer , c’est un sucre D.
Le D-glucose est un Aldohexose de formule (C·H 2 O) 6 . Les atomes rouges mettent en évidence le groupe aldéhyde et les atomes bleus mettent en évidence le centre asymétrique le plus éloigné de l’aldéhyde; parce que ce -OH est à droite de la projection de Fischer , c’est un sucre D.
Les monosaccharides sont les glucides les plus simples en ce sens qu’ils ne peuvent pas être hydrolysés en glucides plus petits. Ce sont des aldéhydes ou des cétones avec deux groupes Hydroxyle ou plus. La formule chimique générale d’un monosaccharide non modifié est (C•H 2 O) n , littéralement un « hydrate de carbone ». Les monosaccharides sont des molécules de carburant importantes ainsi que des éléments constitutifs des acides nucléiques. Les plus petits monosaccharides, pour lesquels n = 3, sont la dihydroxyacétone et les D- et L-glycéraldéhydes.
Classification des monosaccharides
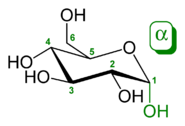



Les anomères α et β du glucose. Noter la position du groupement Hydroxyle (rouge ou vert) sur le carbone anomérique par rapport au groupement CH 2 OH lié au carbone 5 : ils ont soit des configurations absolues identiques (R,R ou S,S) (α), soit des configurations absolues opposées configurations (R,S ou S,R) (β). [13]
Les monosaccharides sont classés selon trois caractéristiques différentes : le placement de son groupe carbonyle , le nombre d’ atomes de carbone qu’il contient et sa chiralité . Si le groupe carbonyle est un aldéhyde , le monosaccharide est un aldose ; si le groupe carbonyle est une cétone , le monosaccharide est un cétose . Les monosaccharides à trois atomes de carbone sont appelés trioses , ceux à quatre sont appelés tétroses , cinq sont appelés pentoses , six sont hexoses , etc. [14]Ces deux systèmes de classification sont souvent combinés. Par exemple, le glucose est un Aldohexose (un aldéhyde à six carbones), le ribose est un Aldopentose (un aldéhyde à cinq carbones) et le fructose est un Cétohexose (une cétone à six carbones).
Chaque atome de carbone portant un groupe Hydroxyle (-OH), à l’exception du premier et du dernier carbone, est asymétrique , ce qui en fait un centre stéréo avec deux configurations possibles chacun (R ou S). En raison de cette asymétrie, un certain nombre d’ isomères peuvent exister pour toute formule de monosaccharide donnée. En utilisant la règle de Le Bel-van’t Hoff , l’Aldohexose D-glucose, par exemple, A la formule (C·H 2 O) 6 , dont quatre de ses six atomes de carbone sont stéréogéniques, faisant du D-glucose l’un des 2 4 =16 stéréoisomères possibles . Dans le cas des glycéraldéhydes, un aldotriose, il existe une paire de stéréoisomères possibles, qui sont des énantiomères et des épimères . La 1,3-dihydroxyacétone , le cétose correspondant aux aldoses glycéraldéhydes, est une molécule symétrique sans stéréocentres. L’attribution de D ou L se fait selon l’orientation du carbone asymétrique le plus éloigné du groupe carbonyle : dans une projection standard de Fischer si le groupe Hydroxyle est à droite la molécule est un sucre D, sinon c’est un sucre L. Les préfixes “D-” et “L-” ne doivent pas être confondus avec “d-” ou “l-“, qui indiquent le sens dans lequel le sucre fait tourner la lumière polarisée plane . Cette utilisation de “d-” et “l-” n’est plus suivi dans la chimie des glucides. [15]
Isomérie de la chaîne annulaire droite

 Le saccharose , également connu sous le nom de sucre de table, est un disaccharide commun. Il est composé de deux monosaccharides : le D-glucose (à gauche) et le D-fructose (à droite).
Le saccharose , également connu sous le nom de sucre de table, est un disaccharide commun. Il est composé de deux monosaccharides : le D-glucose (à gauche) et le D-fructose (à droite).
Deux monosaccharides joints sont appelés un disaccharide et ce sont les polysaccharides les plus simples. Les exemples incluent le saccharose et le lactose . Ils sont composés de deux unités monosaccharidiques liées entre elles par une liaison covalente connue sous le nom de Liaison glycosidique formée via une réaction de déshydratation , entraînant la perte d’un atome d’hydrogène d’un monosaccharide et d’un groupe Hydroxyle de l’autre. La formule des disaccharides non modifiés est C 12 H 22 O 11. Bien qu’il existe de nombreux types de disaccharides, une poignée de disaccharides sont particulièrement remarquables.
Le saccharose , illustré à droite, est le disaccharide le plus abondant et la principale forme sous laquelle les glucides sont transportés dans les plantes. Il est composé d’une molécule de D-glucose et d’une molécule de D-fructose . Le nom systématique du saccharose, O -α-D-glucopyranosyl-(1→2)-D-fructofuranoside, indique quatre choses :
- Ses monosaccharides : glucose et fructose
- Leurs types d’anneaux : le glucose est un pyranose et le fructose est un furanose
- Comment ils sont liés entre eux : l’oxygène sur le carbone numéro 1 (C1) de l’α-D-glucose est lié au C2 du D-fructose.
- Le suffixe -oside indique que le carbone anomérique des deux monosaccharides participe à la Liaison glycosidique.
Le lactose , un disaccharide composé d’une molécule de D-galactose et d’une molécule de D-glucose , est naturellement présent dans le lait des mammifères. Le nom systématique du lactose est O -β-D-galactopyranosyl-(1→4)-D-glucopyranose. D’autres disaccharides notables comprennent le maltose (deux D-glucoses liés en α-1,4) et le cellobiose (deux D-glucoses liés en β-1,4). Les disaccharides peuvent être classés en deux types : les disaccharides réducteurs et non réducteurs. Si le groupe fonctionnel est présent en liaison avec une autre unité de sucre, il est appelé disaccharide réducteur ou biose.
La nutrition

 Produits céréaliers : riches sources de glucides
Produits céréaliers : riches sources de glucides
Les glucides consommés dans les aliments donnent 3,87 kilocalories d’énergie par gramme pour les sucres simples [18] et 3,57 à 4,12 kilocalories par gramme pour les glucides complexes dans la plupart des autres aliments. [19] Des niveaux relativement élevés de glucides sont associés aux aliments transformés ou aux aliments raffinés à base de plantes, y compris les sucreries, les biscuits et les bonbons, le sucre de table, le miel, les boissons gazeuses, les pains et les craquelins, les confitures et les produits à base de fruits, les pâtes et les céréales du petit-déjeuner. De plus faibles quantités de glucides sont généralement associées à des aliments non raffinés, notamment les haricots, les tubercules, le riz et les fruits non raffinés [ douteux – discuter ] . [20]Les aliments d’origine animale ont généralement les plus faibles niveaux de glucides, bien que le lait contienne une forte proportion de lactose .
Les organismes ne peuvent généralement pas métaboliser tous les types de glucides pour produire de l’énergie. Le glucose est une source d’énergie quasi universelle et accessible. De nombreux organismes ont également la capacité de métaboliser d’autres monosaccharides et disaccharides , mais le glucose est souvent métabolisé en premier. Chez Escherichia coli , par exemple, l’ opéron lac exprimera des enzymes pour la digestion du lactose lorsqu’il est présent, mais si le lactose et le glucose sont présents, l’ opéron lac est réprimé, ce qui fait que le glucose est utilisé en premier (voir : Diauxie ). Polysaccharidessont également des sources d’énergie courantes. De nombreux organismes peuvent facilement décomposer les amidons en glucose ; la plupart des organismes, cependant, ne peuvent pas métaboliser la cellulose ou d’autres polysaccharides comme la chitine et les arabinoxylanes . Ces types de glucides peuvent être métabolisés par certaines bactéries et protistes. Les ruminants et les termites , par exemple, utilisent des micro-organismes pour transformer la cellulose. Même si ces glucides complexes sont peu digestibles, ils représentent un élément alimentaire important pour l’homme, appelé fibre alimentaire . Les fibres améliorent la digestion, entre autres avantages. [21]
L’ Institute of Medicine recommande que les adultes américains et canadiens tirent entre 45 et 65 % de leur énergie alimentaire de glucides de grains entiers. [22] L’ Organisation des Nations Unies pour l’alimentation et l’agriculture et l’Organisation mondiale de la santé recommandent conjointement que les directives alimentaires nationales fixent un objectif de 55 à 75 % de l’énergie totale provenant des glucides, mais seulement 10 % provenant directement des sucres (leur terme désignant les glucides simples). [23] Une revue systématique Cochrane de 2017 A conclu qu’il n’y avait pas suffisamment de preuves pour étayer l’affirmation selon laquelle les régimes à base de grains entiers peuvent affecter les maladies cardiovasculaires. [24]
Classification
Les nutritionnistes qualifient souvent les glucides de simples ou de complexes. Cependant, la distinction exacte entre ces groupes peut être ambiguë. Le terme glucides complexes A été utilisé pour la première fois dans la publication Dietary Goals for the United States (1977) du Comité spécial du Sénat américain sur la nutrition et les besoins humains , où il visait à distinguer les sucres des autres glucides (qui étaient perçus comme étant nutritionnellement supérieurs). [25]Cependant, le rapport place les « fruits, légumes et grains entiers » dans la colonne des glucides complexes, malgré le fait que ceux-ci peuvent contenir des sucres ainsi que des polysaccharides. Cette confusion persiste car aujourd’hui certains nutritionnistes utilisent le terme glucides complexes pour désigner toute sorte de saccharide digestible présent dans un aliment entier, où l’on trouve également des fibres, des vitamines et des minéraux (par opposition aux glucides transformés, qui fournissent de l’énergie mais peu d’autres nutriments) . L’usage standard est cependant de classer chimiquement les glucides : simple s’il s’agit de sucres ( monosaccharides et disaccharides ) et complexe s’il s’agit de polysaccharides (ou oligosaccharides ). [26]
Dans tous les cas, la distinction chimique simple vs complexe A peu de valeur pour déterminer la qualité nutritionnelle des glucides. [26] Certains glucides simples (par exemple , le fructose ) augmentent rapidement la glycémie, tandis que certains glucides complexes (amidons) augmentent lentement la glycémie. La vitesse de digestion est déterminée par divers facteurs, notamment les autres nutriments consommés avec les glucides, la façon dont les aliments sont préparés, les différences individuelles de métabolisme et la chimie des glucides. [27] Les glucides sont parfois divisés en “glucides disponibles”, qui sont absorbés dans l’ intestin grêle et en “glucides non disponibles”, qui passent dans le gros intestin, où ils sont soumis à fermentation par le microbiote gastro – intestinal . [28]
Les directives diététiques pour les Américains 2010 de l’USDA appellent à une consommation modérée à élevée de glucides dans le cadre d’une alimentation équilibrée comprenant six portions d’une once d’aliments céréaliers chaque jour, au moins la moitié provenant de sources de grains entiers et le reste d’ aliments enrichis . [29]
Les concepts d’ index glycémique (IG) et de charge glycémique ont été développés pour caractériser le comportement alimentaire au cours de la digestion humaine. Ils classent les aliments riches en glucides en fonction de la rapidité et de l’ampleur de leur effet sur la glycémie . L’indice glycémique est une mesure de la rapidité avec laquelle le glucose alimentaire est absorbé, tandis que la charge glycémique est une mesure du glucose total absorbable dans les aliments. L’ indice d’insuline est une méthode de classification similaire et plus récente qui classe les aliments en fonction de leurs effets sur les niveaux d’ insuline dans le sang , qui sont causés par le glucose (ou l’amidon) et certains acides aminés contenus dans les aliments.
Effets sur la santé de la restriction alimentaire en glucides
Les régimes à faible teneur en glucides peuvent passer à côté des avantages pour la santé – tels qu’un apport accru en fibres alimentaires – offerts par les glucides de haute qualité présents dans les légumineuses et les légumineuses , les grains entiers , les fruits et les légumes. [30] [31] Les inconvénients du régime alimentaire peuvent inclure l’ halitose , les maux de tête et la constipation , et en général, les effets indésirables potentiels des régimes à restriction glucidique sont sous-étudiés, en particulier pour les risques possibles d’ ostéoporose et d’incidence du cancer . [32]
Les régimes pauvres en glucides peuvent être aussi efficaces que les régimes faibles en gras pour aider à perdre du poids à court terme lorsque l’apport calorique global est réduit. [33] Une déclaration scientifique de l’ Endocrine Society A déclaré que “lorsque l’apport calorique est maintenu constant […] l’accumulation de graisse corporelle ne semble pas être affectée par des changements même très prononcés dans la quantité de graisse par rapport aux glucides dans l’alimentation”. [33] À long terme, une perte ou un maintien de poids efficace dépend de la restriction calorique , [33] et non du ratio de macronutriments dans un régime. [34] Le raisonnement de l’alimentation préconise que les glucides provoquent une accumulation excessive de graisse en augmentant l’ insuline sanguineet que les régimes à faible teneur en glucides ont un « avantage métabolique », n’est pas étayée par des preuves cliniques . [33] [35] De plus, il n’est pas clair comment un régime pauvre en glucides affecte la santé cardiovasculaire , bien que deux revues aient montré que la restriction en glucides peut améliorer les marqueurs lipidiques du risque de maladie cardiovasculaire . [36] [37]
Les régimes pauvres en glucides ne sont pas plus efficaces qu’un régime alimentaire sain conventionnel pour prévenir l’apparition du diabète de type 2 , mais pour les personnes atteintes de diabète de type 2, ils constituent une option viable pour perdre du poids ou aider au contrôle de la glycémie . [38] [39] [40] Il existe des preuves limitées pour soutenir l’utilisation systématique d’un régime pauvre en glucides dans la gestion du diabète de type 1 . [41] L’ American Diabetes Association recommande aux personnes atteintes de diabète d’adopter une alimentation généralement saine, plutôt qu’une alimentation axée sur les glucides ou d’autres macronutriments. [40]
Une forme extrême de régime pauvre en glucides – le régime cétogène – est établie comme régime médical pour traiter l’ épilepsie . [42] Grâce à l’ approbation des célébrités au début du 21e siècle, il est devenu un régime à la mode comme moyen de perte de poids, mais avec des risques d’effets secondaires indésirables , tels qu’un faible niveau d’énergie et une augmentation de la faim, de l’insomnie , des nausées et des malaises gastro -intestinaux . [42] La British Dietetic Association l’A nommé l’un des “5 pires régimes de célébrités à éviter en 2018”. [42]
La source

 Comprimés de glucose
Comprimés de glucose
La plupart des glucides alimentaires contiennent du glucose, soit comme élément constitutif unique (comme dans les polysaccharides amidon et glycogène), soit avec un autre monosaccharide (comme dans les hétéropolysaccharides saccharose et lactose). [43] Le glucose non lié est l’un des principaux ingrédients du miel. Le glucose est extrêmement abondant et A été isolé à partir de diverses sources naturelles à travers le monde, y compris les cônes mâles du conifère Wollemia nobilis à Rome, [44] les racines des plantes Ilex asprella en Chine, [45] et les pailles de riz en Californie. [46]
| Produit alimentaire | Glucides, totaux, A dont fibres alimentaires |
Sucres totaux | Fructose libre | Glucose libre | Saccharose | Rapport fructose/ glucose |
Saccharose en proportion des sucres totaux (%) |
|---|---|---|---|---|---|---|---|
| Des fruits | |||||||
| Pomme | 13.8 | 10.4 | 5.9 | 2.4 | 2.1 | 2.0 | 19.9 |
| Abricot | 11.1 | 9.2 | 0,9 | 2.4 | 5.9 | 0,7 | 63,5 |
| Banane | 22,8 | 12.2 | 4.9 | 5.0 | 2.4 | 1.0 | 20,0 |
| Figue , séchée | 63,9 | 47,9 | 22,9 | 24,8 | 0,9 | 0,93 | 0,15 |
| Raisins | 18.1 | 15.5 | 8.1 | 7.2 | 0,2 | 1.1 | 1 |
| Orange nombril | 12.5 | 8.5 | 2.25 | 2.0 | 4.3 | 1.1 | 50,4 |
| La pêche | 9.5 | 8.4 | 1.5 | 2.0 | 4.8 | 0,9 | 56,7 |
| Poire | 15.5 | 9.8 | 6.2 | 2.8 | 0,8 | 2.1 | 8.0 |
| Ananas | 13.1 | 9.9 | 2.1 | 1.7 | 6.0 | 1.1 | 60,8 |
| Prune | 11.4 | 9.9 | 3.1 | 5.1 | 1.6 | 0,66 | 16.2 |
| Légumes | |||||||
| Betterave rouge | 9.6 | 6.8 | 0,1 | 0,1 | 6.5 | 1.0 | 96,2 |
| Carotte | 9.6 | 4.7 | 0,6 | 0,6 | 3.6 | 1.0 | 77 |
| Poivron rouge , doux | 6.0 | 4.2 | 2.3 | 1.9 | 0.0 | 1.2 | 0.0 |
| Oignon , doux | 7.6 | 5.0 | 2.0 | 2.3 | 0,7 | 0,9 | 14.3 |
| Patate douce | 20.1 | 4.2 | 0,7 | 1.0 | 2.5 | 0,9 | 60.3 |
| patate douce | 27,9 | 0,5 | Traces | Traces | Traces | N / A | Traces |
| Canne à sucre | 13–18 | 0,2–1,0 | 0,2–1,0 | 11–16 | 1.0 | haute | |
| Betterave à sucre | 17–18 | 0,1–0,5 | 0,1–0,5 | 16–17 | 1.0 | haute | |
| Céréales | |||||||
| Maïs , doux | 19.0 | 6.2 | 1.9 | 3.4 | 0,9 | 0,61 | 15,0 |
^A La valeur des glucides est calculée dans la base de données USDA et ne correspond pas toujours à la somme des sucres, de l’amidon et des “fibres alimentaires”.
Métabolisme
Le métabolisme des glucides est l’ensemble des processus biochimiques responsables de la formation , de la décomposition et de l’interconversion des glucides dans les organismes vivants .
Le glucide le plus important est le glucose , un sucre simple ( monosaccharide ) qui est métabolisé par presque tous les organismes connus. Le glucose et d’autres glucides font partie d’une grande variété de voies métaboliques à travers les espèces : les plantes synthétisent des glucides à partir de dioxyde de carbone et d’eau par photosynthèse en stockant l’énergie absorbée en interne, souvent sous forme d’ amidon ou de lipides . Les composants végétaux sont consommés par les animaux et les champignons , et utilisés comme carburant pour la respiration cellulaire . L’oxydation d’un gramme de glucides donne environ 16 kJ (4 kcal) d’ énergie, tandis que l’oxydation d’un gramme de lipides donne environ 38 kJ (9 kcal). Le corps humain stocke entre 300 et 500 g de glucides selon le poids corporel, le muscle squelettique contribuant à une grande partie du stockage. [48] L’énergie obtenue du métabolisme (par exemple, l’oxydation du glucose) est généralement stockée temporairement dans les cellules sous forme d’ ATP . [49] Les organismes capables de respiration anaérobie et Aérobie métabolisent le glucose et l’oxygène (Aérobie) pour libérer de l’énergie, avec du dioxyde de carbone et de l’eau comme sous-produits.
Catabolisme
Le catabolisme est la réaction métabolique que subissent les cellules pour décomposer des molécules plus grosses, en extrayant de l’énergie. Il existe deux principales voies métaboliques du catabolisme des monosaccharides : la glycolyse et le cycle de l’acide citrique .
Dans la glycolyse, les oligo- et polysaccharides sont d’abord clivés en monosaccharides plus petits par des enzymes appelées glycoside hydrolases . Les unités monosaccharidiques peuvent alors entrer dans le catabolisme monosaccharidique. Un investissement de 2 ATP est nécessaire dans les premières étapes de la glycolyse pour phosphoryler le glucose en glucose 6-phosphate ( G6P ) et le fructose 6-phosphate ( F6P ) en fructose 1,6-biphosphate ( FBP ), poussant ainsi la réaction de manière irréversible. [48] Dans certains cas, comme chez les humains, tous les types de glucides ne sont pas utilisables car les enzymes digestives et métaboliques nécessaires ne sont pas présentes.
Chimie des glucides
La chimie des glucides est une branche importante et économiquement importante de la chimie organique. Certaines des principales réactions organiques impliquant des glucides sont :
- Réarrangement d’Amadori
- Acétalisation des glucides
- Digestion des glucides
- Réaction de la cyanhydrine
- Réaction de Koenigs-Knorr
- Transformation Lobry de Bruyn-Van Ekenstein
- Réaction de Nef
- Dégradation de Wohl
Voir également
- Bioplastique
- RMN des glucides
- Gluconéogenèse – Un processus où le glucose peut être synthétisé par des sources non glucidiques.
- Glycobiologie
- Glycogène
- Glycoinformatique
- Glycolipide
- Glycome
- Glycomique
- Glycosyle
- Macromolécule
- Acide saccharique
Références
- ^ Flitsch SL, Ulijn RV (janvier 2003). “Les sucres liés à la tache”. Nature . 421 (6920): 219-20. Bibcode : 2003Natur.421..219F . doi : 10.1038/421219a . PMID 12529622 . S2CID 4421938 .
- ^ un b Avenas P (2012). “Étymologie des principaux noms de polysaccharides” (PDF) . Dans Navard P (éd.). Le Réseau d’Excellence Européen des Polysaccharides (EPNOE) . Vienne : Springer-Verlag . Archivé de l’original (PDF) le 9 février 2018 . Consulté le 28 janvier 2018 .
- ^ Maton A, Hopkins J, McLaughlin CW, Johnson S, Warner MQ, LaHart D, Wright JD (1993). Biologie humaine et santé . Falaises d’Englewood, New Jersey : Prentice Hall. p. 52–59 . ISBN 978-0-13-981176-0.
- ^ Base de données nationale sur les nutriments de l’USDA, 2015, p. 14
- ^ Cummings, John H. (2001). L’effet des fibres alimentaires sur le poids et la composition des matières fécales (3e éd.). Boca Raton, Floride : CRC Press. p. 184. ISBN 978-0-8493-2387-4. Archivé de l’original le 2 avril 2019 . Consulté le 24 avril 2022 .
- ^ Byrne CS, Chambers ES, Morrison DJ, Frost G (septembre 2015). “Le rôle des Acides gras à chaîne courte dans la régulation de l’appétit et l’homéostasie énergétique” . Journal international de l’obésité . 39 (9) : 1331–8. doi : 10.1038/ijo.2015.84 . PMC 4564526 . PMID 25971927 .
- ^ Fearon WF (1949). Introduction à la biochimie (2e éd.). Londres : Heinemann. ISBN 9781483225395. Archivé de l’original le 27 juillet 2020 . Consulté le 30 novembre 2017 .
- ^ Base de données nationale sur les nutriments de l’USDA, 2015, p. 13
- ^ Coulter JM, Barnes CR, Cowles HC (1930). Un manuel de botanique pour les collèges et universités . ISBN 9781113909954. Archivé de l’original le 17 avril 2022 . Consulté le 24 avril 2022 .
- ^ Burtis CA, Ashwood ER, Tietz NW (2000). Tietz fondements de la chimie clinique . ISBN 9780721686349. Archivé de l’original le 24 juin 2016 . Consulté le 8 janvier 2016 .
- ^ Matthews CE, Van Holde KE, Ahern KG (1999). Biochimie (3e éd.). Benjamin Cummings. ISBN 978-0-8053-3066-3.[ page nécessaire ]
- ^ “Chapitre 1 – Le rôle des glucides dans la nutrition” . Les glucides dans l’alimentation humaine . Document de la FAO sur l’alimentation et la nutrition – 66. Organisation des Nations Unies pour l’alimentation et l’agriculture. Archivé de l’original le 22 décembre 2015 . Consulté le 21 décembre 2015 .
- ^ Bertozzi CR, Rabuka D (2017). “Base structurelle de la diversité des glycanes” . Essentials of Glycobiology (3e éd.). Cold Spring Harbor (État de New York) : Cold Spring Harbor Laboratory Press. ISBN 978-1-621821-32-8. Archivé de l’original le 19 mai 2020 . Consulté le 30 août 2017 .
- ^ Campbell NA, Williamson B, Heyden RJ (2006). Biologie : Explorer la vie . Boston, Massachusetts : Pearson Prentice Hall. ISBN 978-0-13-250882-7. Archivé de l’original le 2 novembre 2014 . Consulté le 2 décembre 2008 .
- ^ Pigman W, Horton D (1972). “Chapitre 1: Stéréochimie des Monosaccharides”. Dans Pigman et Horton (éd.). Les glucides: chimie et biochimie Vol 1A (2e éd.). San Diego : Presse académique. p. 1–67. ISBN 9780323138338.
- ^ Pigman W, Anet E (1972). “Chapitre 4: Mutarotations et Actions des Acides et des Bases”. Dans Pigman et Horton (éd.). Les glucides: chimie et biochimie Vol 1A (2e éd.). San Diego : Presse académique. pp. 165–94. ISBN 9780323138338.
- ^ “lyxoflavine” . Merriam-Webster . Archivé de l’original le 31 octobre 2014 . Consulté le 26 février 2014 .
- ^ “Afficher les aliments” . usda.gov . Archivé de l’original le 3 octobre 2017 . Consulté le 4 juin 2014 .
- ^ “Calcul de la teneur énergétique des aliments – Facteurs de conversion énergétique” . fao.org . Archivé de l’original le 24 mai 2010 . Consulté le 2 août 2013 .
- ^ “Liste de référence des glucides” (PDF) . www.diabetes.org.uk . Archivé de l’original (PDF) le 14 mars 2016 . Consulté le 30 octobre 2016 .
- ↑ Pichon L, Huneau JF, Fromentin G, Tomé D (mai 2006). “Un régime riche en protéines, riche en graisses et sans glucides réduit l’apport énergétique, la lipogenèse hépatique et l’adiposité chez les rats” . Le Journal de l’alimentation . 136 (5) : 1256–1260. doi : 10.1093/jn/136.5.1256 . PMID 16614413 .
- ^ Conseil de l’alimentation et de la nutrition (2002/2005). Apports nutritionnels de référence pour l’énergie, les glucides, les fibres, les lipides, les acides gras, le cholestérol, les protéines et les acides aminés Archivé le 10 février 2007 sur archive.today . Washington, DC : La presse des académies nationales . Page 769 Archivé le 12 septembre 2006 à la Wayback Machine . ISBN 0-309-08537-3 .
- ^ Consultation conjointe d’experts OMS / FAO (2003). [1] ( PDF ). Genève : Organisation mondiale de la santé . p. 55–56. ISBN 92-4-120916-X .
- ^ Kelly SA, Hartley L, Loveman E, Colquitt JL, Jones HM, Al-Khudairy L, Clar C, Germanò R, Lunn HR, Frost G, Rees K (2017). “Céréales complètes pour la prévention primaire ou secondaire des maladies cardiovasculaires” (PDF) . La base de données Cochrane des revues systématiques . 8 : CD005051. doi : 10.1002/14651858.CD005051.pub3 . PMC 6484378 . PMID 28836672 . Archivé de l’original (PDF) le 28 septembre 2018 . Consulté le 27 septembre 2018 .
- ^ Consultation conjointe d’experts OMS / FAO (1998), Glucides dans la nutrition humaine , chapitre 1 Archivé le 15 janvier 2007 à la Wayback Machine . ISBN 92-5-104114-8 .
- ^ un b “Glucides” . La source nutritionnelle . École de santé publique de Harvard. 18 septembre 2012. Archivé de l’original le 7 mai 2013 . Consulté le 3 avril 2013 .
- ^ Jenkins DJ, Jenkins AL, Wolever TM, Thompson LH, Rao AV (février 1986). “Glucides simples et complexes”. Revues nutritionnelles . 44 (2): 44–9. doi : 10.1111/j.1753-4887.1986.tb07585.x . PMID 3703387 .
- ^ Hedley, CL (2001). Glucides dans les graines de légumineuses à grains : améliorer la qualité nutritionnelle et les caractéristiques agronomiques . CABI. p. 79. ISBN 978-0-85199-944-9. Archivé de l’original le 24 avril 2022 . Consulté le 24 avril 2022 .
- ^ DHHS et USDA , Dietary Guidelines for Americans 2010 Archivé le 20 août 2014 à la Wayback Machine .
- ^ Seidelmann, Sara B; Claggett, Brian; Cheng, Suzanne ; Henglin, Mir; Shah, Amil ; Steffen, Lyn M; Folsom, Aaron R; Rimm, Eric B; Willett, Walter C; Salomon, Scott D (2018). « Apport alimentaire en glucides et mortalité : une étude de cohorte prospective et une méta-analyse » . Le Lancet. Santé publique (méta-analyse). 3 (9) : e419–e428. doi : 10.1016/s2468-2667(18)30135-x . ISSN 2468-2667 . PMC 6339822 . PMID 30122560 .
- ^ Reynolds A, Mann J , Cummings J, Winter N, Mete E, Te Morenga L (10 janvier 2019). “Qualité des glucides et santé humaine: une série de revues systématiques et de méta-analyses” (PDF) . Lancet (Revue). 393 (10170): 434–445. doi : 10.1016/S0140-6736(18)31809-9 . PMID 30638909 . S2CID 58632705 . Archivé (PDF) de l’original le 11 août 2021 . Consulté le 24 avril 2022 .
- ^ Churuangsuk C, Kherouf M, Combet E, Lean M (2018). “Régimes faibles en glucides pour le surpoids et l’obésité: une revue systématique des revues systématiques” (PDF) . Examens de l’obésité (examen systématique). 19 (12): 1700–1718. doi : 10.1111/obr.12744 . PMID 30194696 . S2CID 52174104 . Archivé (PDF) de l’original le 23 septembre 2019 . Consulté le 24 avril 2022 .
- ^ un bcd Schwartz MW, Seeley RJ, Zeltser LM, Drewnowski A, Ravussin E, Redman LM, et al. (2017). « Pathogenèse de l’obésité : une déclaration scientifique de la société endocrinienne » . Examens endocriniens . 38 (4): 267–296. doi : 10.1210/er.2017-00111 . PMC 5546881 . PMID 28898979 .
- ^ Butryn ML, Clark VL, Coletta MC (2012). Akabas SR, et al. (éd.). Approches comportementales du traitement de l’obésité . Manuel d’obésité . John Wiley et fils. p. 259. ISBN 978-0-470-65588-7. Pris ensemble, ces résultats indiquent que l’apport calorique, et non la composition en macronutriments, détermine le maintien de la perte de poids à long terme.
- ^ Salle KD (2017). “Un examen du modèle d’hydrate de carbone-insuline de l’obésité”. Journal européen de nutrition clinique (Revue). 71 (3): 323–326. doi : 10.1038/ejcn.2016.260 . PMID 28074888 . S2CID 54484172 .
- ^ Mansoor N, Vinknes KJ, Veierød MB, Retterstøl K (février 2016). “Effets des régimes à faible teneur en glucides par rapport aux régimes à faible teneur en matières grasses sur le poids corporel et les facteurs de risque cardiovasculaires : une méta-analyse d’essais contrôlés randomisés”. Le Journal britannique de la nutrition . 115 (3): 466–79. doi : 10.1017/S0007114515004699 . PMID 26768850 . S2CID 21670516 .
- ^ Gjuladin-Hellon T, Davies IG, Penson P, Amiri Baghbadorani R (2019). “Effets des régimes alimentaires restreints en glucides sur les taux de cholestérol des lipoprotéines de basse densité chez les adultes en surpoids et obèses : une revue systématique et une méta-analyse” (PDF) . Examens nutritionnels (examen systématique). 77 (3): 161–180. doi : 10.1093/nutrit/nuy049 . PMID 30544168 . S2CID 56488132 . Archivé (PDF) de l’original le 6 mai 2020 . Consulté le 24 avril 2022 .
- ^ Brouns F (2018). “Prévention du surpoids et du diabète : un régime pauvre en glucides et riche en graisses est-il recommandé ?” . Eur J Nutr (Revue). 57 (4): 1301-1312. doi : 10.1007/s00394-018-1636-y . PMC 5959976 . PMID 29541907 .
- ^ Meng Y, Bai H, Wang S, Li Z, Wang Q, Chen L (2017). “Efficacité d’un régime pauvre en glucides pour la gestion du diabète sucré de type 2 : une revue systématique et une méta-analyse d’essais contrôlés randomisés”. Recherche sur le diabète et pratique clinique . 131 : 124–131. doi : 10.1016/j.diabres.2017.07.006 . PMID 28750216 .
- ^ un b Comité de pratique professionnelle de l’Association américaine du diabète (2019). “Comité de pratique professionnelle : Normes de soins médicaux pour le diabète – 2019” . Soins du diabète . 42 (Supplément 1) : s46–s60. doi : 10.2337/dc19-S005 . PMID 30559231 . Archivé de l’original le 18 décembre 2018 . Consulté le 24 avril 2022 .
- ^ Seckold R, Fisher E, de Bock M, King BR, Smart CE (2019). “Les hauts et les bas des régimes à faible teneur en glucides dans la gestion du diabète de type 1 : un examen des résultats cliniques”. Diabète. Méd. (La revue). 36 (3): 326–334. doi : 10.1111/dme.13845 . PMID 30362180 . S2CID 53102654 .
- ^ A b c “Top 5 des pires régimes de célébrités à éviter en 2018” . Association diététique britannique. 7 décembre 2017. Archivé de l’original le 31 juillet 2020 . Consulté le 1er décembre 2020 . La British Dietetic Association (BDA) A dévoilé aujourd’hui sa liste annuelle très attendue des régimes de célébrités à éviter en 2018. La gamme de cette année comprend les régimes crus végétaliens, alcalins, Pioppi et cétogènes ainsi que les suppléments nutritionnels de Katie Price.
- ^ “Les glucides et la glycémie” . La source nutritionnelle . 5 août 2013. Archivé de l’original le 30 janvier 2017 . Consulté le 30 janvier 2017 – via la Harvard TH Chan School of Public Health.
- ^ Venditti, Alessandro; Frezza, Claudio; Vincenti, Flaminia ; Brodella, Antonia; Sciubba, Fabio; Montesano, Camille ; Franceschin, Marco; Sergi, Manuel; Foddai, Sebastiano; Di Cocco, Maria Enrica; Curini, Roberta (2019). “Un dérivé syn-ent-labdadiene avec une fonction spiro-β-lactone rare des cônes mâles de Wollemia nobilis” . Phytochimie . 158 : 91–95. doi : 10.1016/j.phytochem.2018.11.012 . ISSN 0031-9422 . PMID 30481664 . S2CID 53757166 .
- ^ Lei, Yu; Shi, She-Po ; Chanson, Yue-Lin; Bi, Dan ; Tu, Peng-Fei (2014). “Saponines triterpéniques des racines d’Ilex asprella” . Chimie & Biodiversité . 11 (5): 767–775. doi : 10.1002/cbdv.201300155 . ISSN 1612-1872 . PMID 24827686 . S2CID 40353516 .
- ^ Balan, Venkatesh; Bals, Bryan ; Chundawat, Shishir PS ; Marshall, Derek ; Dale, Bruce E. (2009), Prétraitement de la biomasse lignocellulosique à l’aide d’AFEX , Methods in Molecular Biology, vol. 581, Totowa, NJ : Humana Press, pp. 61–77, Bibcode : 2009biof.book…61B , doi : 10.1007/978-1-60761-214-8_5 , ISBN 978-1-60761-213-1, PMID 19768616 , récupéré le 11 novembre 2021
- ^ “Centre de données alimentaires” . fdc.nal.usda.gov .
- ^ un b Maughan, Ron (juin 2013). « Chirurgie d’Oxford » . www.onesearch.cuny.edu . [ lien mort permanent ]
- ^ Mehta S (9 octobre 2013). “Énergétique de la Respiration Cellulaire (Métabolisme du Glucose)” . Notes de biochimie, Notes . Archivé de l’original le 25 janvier 2018 . Consulté le 15 octobre 2015 .
Lectures complémentaires
- « Composition d’aliments crus, transformés, préparés » (PDF) . Département de l’agriculture des États-Unis . Septembre 2015 . Consulté le 30 octobre 2016 .
Liens externes
| Wikimedia Commons A des médias liés aux glucides . |
| Wikiquote A des citations liées aux glucides . |
- Glucides, y compris des modèles interactifs et des animations (nécessite MDL Chime )
- Commission mixte IUPAC-IUBMB sur la nomenclature biochimique (JCBN): Nomenclature des glucides
- Glucides détaillés
- Glucides et glycosylation – La bibliothèque virtuelle de biochimie, de biologie moléculaire et de biologie cellulaire
- Functional Glycomics Gateway , une collaboration entre le Consortium for Functional Glycomics et Nature Publishing Group