La thermodynamique est une branche de la physique qui traite de la chaleur , du travail et de la température , ainsi que de leur relation avec l’énergie , l’ entropie et les propriétés physiques de la matière et du rayonnement . Le comportement de ces grandeurs est régi par les quatre lois de la thermodynamique qui véhiculent une description quantitative à l’aide de grandeurs physiques macroscopiques mesurables , mais peuvent être expliquées en termes de constituants microscopiques par la mécanique statistique . La thermodynamique s’applique à une grande variété de sujets scientifiques etl’ ingénierie , en particulier la chimie physique , la biochimie , le génie chimique et le génie mécanique , mais aussi dans d’ autres domaines complexes comme la météorologie .
Historiquement, la thermodynamique s’est développée à partir d’un désir d’augmenter l’ efficacité des premières machines à vapeur , notamment grâce aux travaux du physicien français Sadi Carnot (1824) qui croyait que l’efficacité des moteurs était la clé qui pourrait aider la France à gagner les guerres napoléoniennes . [1] Le physicien écossais-irlandais Lord Kelvin fut le premier à formuler une définition concise de la thermodynamique en 1854 [2] qui déclarait : « La thermodynamique est le sujet de la relation de la chaleur aux forces agissant entre les parties contiguës des corps, et la relation de la chaleur à l’agence électrique.”
L’application initiale de la thermodynamique aux moteurs thermiques mécaniques s’est rapidement étendue à l’étude des composés chimiques et des Réactions chimiques. La thermodynamique chimique étudie la nature du rôle de l’ entropie dans le processus des Réactions chimiques et a fourni l’essentiel de l’expansion et de la connaissance du domaine. [3] [4] [5] [6] [7] [8] [9] [10] [11] D’autres formulations de la thermodynamique ont émergé. La Thermodynamique statistique , ou mécanique statistique, s’intéresse à la statistique .prédictions du mouvement collectif des particules à partir de leur comportement Microscopique. En 1909, Constantin Carathéodory a présenté une approche purement mathématique dans une formulation Axiomatique , une description souvent appelée thermodynamique géométrique .
Introduction
Une description de tout système thermodynamique utilise les quatre lois de la thermodynamique qui forment une base Axiomatique. La première loi précise que l’énergie peut être transférée entre des systèmes physiques sous forme de chaleur , de travail et avec transfert de matière. [12] La deuxième loi définit l’existence d’une quantité appelée entropie , qui décrit la direction, thermodynamiquement, dans laquelle un système peut évoluer et quantifie l’état d’ordre d’un système et qui peut être utilisée pour quantifier le travail utile qui peut être extrait du système. [13]
En thermodynamique, les interactions entre de grands ensembles d’objets sont étudiées et catégorisées. Au centre de cela se trouvent les concepts du système thermodynamique et de son environnement . Un système est composé de particules, dont les mouvements moyens définissent ses propriétés, et ces propriétés sont à leur tour liées les unes aux autres par des équations d’état . Les propriétés peuvent être combinées pour exprimer l’énergie interne et les potentiels thermodynamiques , qui sont utiles pour déterminer les conditions d’ équilibre et les processus spontanés .
Avec ces outils, la thermodynamique peut être utilisée pour décrire comment les systèmes réagissent aux changements de leur environnement. Cela peut s’appliquer à une grande variété de sujets en sciences et en ingénierie , tels que les moteurs , les transitions de phase , les Réactions chimiques , les phénomènes de transport et même les trous noirs . Les résultats de la thermodynamique sont essentiels pour d’ autres domaines de la physique et pour la chimie , le génie chimique , le génie de la corrosion , le génie aérospatial , le génie mécanique , la biologie cellulaire ,génie biomédical , science des matériaux et économie , pour n’en nommer que quelques-uns. [14] [15]
Cet article porte principalement sur la thermodynamique classique qui étudie principalement les systèmes en équilibre thermodynamique . La thermodynamique hors équilibre est souvent traitée comme une extension du traitement classique, mais la mécanique statistique a apporté de nombreuses avancées dans ce domaine.
Histoire

 Les thermodynamiciens représentant les huit écoles fondatrices de la thermodynamique. Les écoles qui ont eu l’effet le plus durable dans la fondation des versions modernes de la thermodynamique sont l’école de Berlin, en particulier telle qu’établie dans le manuel de Rudolf Clausius de 1865 La théorie mécanique de la chaleur , l’école de Vienne, avec la mécanique statistique de Ludwig Boltzmann , et la École gibbsienne de l’Université de Yale, ingénieur américain Willard Gibbs ‘ 1876 Sur l’équilibre des substances hétérogènes lançant la thermodynamique chimique. [16]
Les thermodynamiciens représentant les huit écoles fondatrices de la thermodynamique. Les écoles qui ont eu l’effet le plus durable dans la fondation des versions modernes de la thermodynamique sont l’école de Berlin, en particulier telle qu’établie dans le manuel de Rudolf Clausius de 1865 La théorie mécanique de la chaleur , l’école de Vienne, avec la mécanique statistique de Ludwig Boltzmann , et la École gibbsienne de l’Université de Yale, ingénieur américain Willard Gibbs ‘ 1876 Sur l’équilibre des substances hétérogènes lançant la thermodynamique chimique. [16]
L’ histoire de la thermodynamique en tant que discipline scientifique commence généralement avec Otto von Guericke qui, en 1650, a construit et conçu la première pompe à vide au monde et a démontré un vide à l’aide de ses hémisphères de Magdebourg . Guericke a été poussé à faire le vide afin de réfuter la supposition de longue date d’ Aristote selon laquelle “la nature a horreur du vide”. Peu de temps après Guericke, le physicien et chimiste anglo-irlandais Robert Boyle avait pris connaissance des conceptions de Guericke et, en 1656, en coordination avec le scientifique anglais Robert Hooke , avait construit une pompe à air. [17] En utilisant cette pompe, Boyle et Hooke ont remarqué une corrélation entrepression , température et volume . Avec le temps, La loi de Boyle a été formulée, qui stipule que la pression et le volume sont inversement proportionnels . Puis, en 1679, sur la base de ces concepts, un associé de Boyle nommé Denis Papin a construit un digesteur à vapeur , qui était un récipient fermé avec un couvercle bien ajusté qui confinait la vapeur jusqu’à ce qu’une haute pression soit générée.
Les conceptions ultérieures ont mis en œuvre une soupape de dégagement de vapeur qui a empêché la machine d’exploser. En regardant la soupape monter et descendre en rythme, Papin a conçu l’idée d’un moteur à piston et à cylindre. Cependant, il n’a pas donné suite à sa conception. Néanmoins, en 1697, sur la base des conceptions de Papin, l’ingénieur Thomas Savery construisit le premier moteur, suivi de Thomas Newcomen en 1712. Bien que ces premiers moteurs soient rudimentaires et inefficaces, ils attirèrent l’attention des plus grands scientifiques de l’époque.
Les concepts fondamentaux de capacité calorifique et de chaleur latente , nécessaires au développement de la thermodynamique, ont été développés par le professeur Joseph Black de l’Université de Glasgow, où James Watt était employé comme luthier. Black et Watt ont réalisé des expériences ensemble, mais c’est Watt qui a conçu l’idée du condenseur externe qui a entraîné une forte augmentation de l’ efficacité de la machine à vapeur . [18] S’appuyant sur tous les travaux antérieurs, Sadi Carnot , le “père de la thermodynamique”, a publié Réflexions sur la puissance motrice du feu(1824), un discours sur la chaleur, la puissance, l’énergie et l’efficacité des moteurs. Le livre décrit les relations énergétiques de base entre le moteur de Carnot , le cycle de Carnot et la puissance motrice . Elle a marqué le début de la thermodynamique en tant que science moderne. [dix]
Le premier manuel de thermodynamique a été écrit en 1859 par William Rankine , initialement formé comme physicien et professeur de génie civil et mécanique à l’ Université de Glasgow . [19] Les première et deuxième lois de la thermodynamique ont émergé simultanément dans les années 1850, principalement à partir des travaux de William Rankine , Rudolf Clausius et William Thomson (Lord Kelvin). Les fondements de la Thermodynamique statistique ont été posés par des physiciens tels que James Clerk Maxwell , Ludwig Boltzmann , Max Planck , Rudolf Clausius et J. Willard Gibbs .
Au cours des années 1873-1876, le physicien mathématicien américain Josiah Willard Gibbs a publié une série de trois articles, le plus célèbre étant On the Equilibrium of Heterogeneous Substances , [3] dans lequel il a montré comment les Processus thermodynamiques , y compris les Réactions chimiques , pouvaient être analysés graphiquement. , en étudiant l’ énergie , l’ entropie , le volume , la température et la pression du système thermodynamique de telle manière, on peut déterminer si un processus se produirait spontanément. [20] Aussi Pierre Duhemau 19ème siècle a écrit sur la thermodynamique chimique. [4] Au début du XXe siècle, des chimistes tels que Gilbert N. Lewis , Merle Randall , [5] et EA Guggenheim [6] [7] ont appliqué les méthodes mathématiques de Gibbs à l’analyse des processus chimiques.
Étymologie
L’étymologie de la thermodynamique a une histoire complexe. [21] Il a d’abord été orthographié sous une forme avec un trait d’union comme un adjectif ( thermo-dynamique ) et de 1854 à 1868 comme le nom thermo-dynamique pour représenter la science des moteurs thermiques généralisés. [21]
Le biophysicien américain Donald Haynie affirme que la thermodynamique a été inventée en 1840 à partir de la racine grecque θέρμη therme, signifiant « chaleur », et δύναμις dynamis, signifiant « puissance ». [22]
Pierre Perrot prétend que le terme thermodynamique a été inventé par James Joule en 1858 pour désigner la science des relations entre la chaleur et la puissance, [10] cependant, Joule n’a jamais utilisé ce terme, mais a utilisé à la place le terme moteur thermodynamique parfait en référence au moteur thermodynamique parfait de Thomson. 1849 [23] phraséologie. [21]
En 1858, la thermodynamique , en tant que terme fonctionnel, était utilisée dans l’article de William Thomson “An Account of Carnot’s Theory of the Motive Power of Heat”. [23]
Branches de la thermodynamique
L’étude des systèmes thermodynamiques s’est développée en plusieurs branches connexes, chacune utilisant un modèle fondamental différent comme base théorique ou expérimentale, ou appliquant les principes à différents types de systèmes.
Thermodynamique classique
La thermodynamique classique est la description des états des systèmes thermodynamiques au quasi-équilibre, qui utilise des propriétés macroscopiques mesurables. Il permet de modéliser les échanges d’énergie, de travail et de chaleur selon les lois de la thermodynamique . Le qualificatif classique reflète le fait qu’il représente le premier niveau de compréhension du sujet tel qu’il s’est développé au XIXe siècle et décrit les changements d’un système en termes de paramètres empiriques macroscopiques (à grande échelle et mesurables). Une interprétation Microscopique de ces concepts a ensuite été fournie par le développement de la mécanique statistique .
Mécanique statistique
La mécanique statistique , également connue sous le nom de Thermodynamique statistique, a émergé avec le développement des théories atomiques et moléculaires à la fin du XIXe siècle et au début du XXe siècle, et a complété la thermodynamique classique par une interprétation des interactions microscopiques entre les particules individuelles ou les états de la mécanique quantique. Ce domaine relie les propriétés microscopiques des atomes et molécules individuels aux propriétés macroscopiques et globales des matériaux qui peuvent être observés à l’échelle humaine, expliquant ainsi la thermodynamique classique comme un résultat naturel des statistiques, de la mécanique classique et de la théorie quantique au niveau Microscopique.
Thermodynamique chimique
La thermodynamique chimique est l’étude de l’interrelation de l’énergie avec des Réactions chimiques ou avec un changement d’ état physique dans les limites des lois de la thermodynamique . L’objectif principal de la thermodynamique chimique est de déterminer la spontanéité d’une transformation donnée. [24]
Thermodynamique d’équilibre
Thermodynamique d’équilibreest l’étude des transferts de matière et d’énergie dans des systèmes ou des corps qui, par des agents de leur environnement, peuvent être entraînés d’un état d’équilibre thermodynamique à un autre. Le terme « équilibre thermodynamique » indique un état d’équilibre dans lequel tous les flux macroscopiques sont nuls ; dans le cas des systèmes ou des corps les plus simples, leurs propriétés intensives sont homogènes, et leurs pressions sont perpendiculaires à leurs frontières. Dans un état d’équilibre, il n’y a pas de potentiels déséquilibrés, ou de forces motrices, entre des parties macroscopiquement distinctes du système. Un objectif central de la thermodynamique à l’équilibre est : étant donné un système dans un état d’équilibre initial bien défini, et étant donné son environnement, et étant donné ses parois constitutives,
Thermodynamique hors équilibre
La thermodynamique hors équilibre est une branche de la thermodynamique qui traite des systèmes qui ne sont pas en équilibre thermodynamique . La plupart des systèmes trouvés dans la nature ne sont pas en équilibre thermodynamique car ils ne sont pas dans des états stationnaires et sont soumis de manière continue et discontinue à des flux de matière et d’énergie vers et depuis d’autres systèmes. L’étude thermodynamique des systèmes hors équilibre nécessite des concepts plus généraux que ceux traités par la thermodynamique à l’équilibre. [25] De nombreux systèmes naturels restent encore aujourd’hui au-delà de la portée des méthodes thermodynamiques macroscopiques actuellement connues.
Lois de la thermodynamique
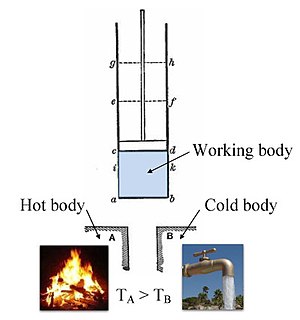
 Version couleur annotée du moteur thermique Carnot original de 1824 montrant le corps chaud (chaudière), le corps de travail (système, vapeur) et le corps froid (eau), les lettres étiquetées selon les points d’arrêt du cycle Carnot .
Version couleur annotée du moteur thermique Carnot original de 1824 montrant le corps chaud (chaudière), le corps de travail (système, vapeur) et le corps froid (eau), les lettres étiquetées selon les points d’arrêt du cycle Carnot .
La thermodynamique est principalement basée sur un ensemble de quatre lois qui sont universellement valables lorsqu’elles sont appliquées à des systèmes qui relèvent des contraintes impliquées par chacune. Dans les diverses descriptions théoriques de la thermodynamique, ces lois peuvent être exprimées sous des formes apparemment différentes, mais les formulations les plus importantes sont les suivantes.
Loi zéro
La loi zéro de la thermodynamique stipule : Si deux systèmes sont chacun en équilibre thermique avec un troisième, ils sont également en équilibre thermique l’un avec l’autre.
Cette affirmation implique que l’équilibre thermique est une relation d’équivalence sur l’ensemble des systèmes thermodynamiques considérés. Les systèmes sont dits en équilibre si les petits échanges aléatoires entre eux (par exemple le mouvement brownien ) ne conduisent pas à un changement net d’énergie. Cette loi est implicitement admise dans toute mesure de température. Ainsi, si l’on cherche à décider si deux corps sont à la même température , il n’est pas nécessaire de les mettre en contact et de mesurer les changements de leurs propriétés observables dans le temps. [26] La loi fournit une définition empirique de la température et une justification pour la construction de thermomètres pratiques.
La loi zéro n’a pas été initialement reconnue comme une loi distincte de la thermodynamique, car sa base dans l’équilibre thermodynamique était impliquée dans les autres lois. Les première, deuxième et troisième lois avaient déjà été explicitement énoncées et avaient trouvé une acceptation commune dans la communauté des physiciens avant que l’importance de la loi zéro pour la définition de la température ne soit réalisée. Comme il n’était pas pratique de renuméroter les autres lois, elle a été nommée la loi zéro .
Première loi
La première loi de la thermodynamique stipule : Dans un processus sans transfert de matière, la variation de l’énergie interne , Δ tu {displaystyle Delta U} 
, d’un système thermodynamique est égal à l’énergie acquise sous forme de chaleur, Q {displaystyle Q}

, moins le travail thermodynamique, O {displaystyle W}

, effectué par le système sur son environnement. [27] [n° 1]
Δ tu = Q − O {displaystyle Delta U=QW} 
.
où Δ tu {displaystyle Delta U} 
désigne la variation de l’énergie interne d’un système fermé (pour lequel la chaleur ou le travail à travers la frontière du système sont possibles, mais le transfert de matière n’est pas possible), Q {displaystyle Q}

désigne la quantité d’énergie fournie au système sous forme de chaleur, et O {displaystyle W}

désigne la quantité de travail thermodynamique effectué par le système sur son environnement. Une affirmation équivalente est que les Machines à mouvement perpétuel du premier type sont impossibles ; travail O {displaystyle W}

fait par un système sur son environnement nécessite que l’énergie interne du système tu {displaystyle U}

diminuer ou être consommée, de sorte que la quantité d’énergie interne perdue par ce travail doit être réapprovisionnée sous forme de chaleur Q {displaystyle Q}

par une source d’énergie externe ou comme travail par une machine externe agissant sur le système (de sorte que tu {displaystyle U}

est récupéré) pour faire fonctionner le système en continu.
Pour les processus qui incluent le transfert de matière, une déclaration supplémentaire est nécessaire : en tenant dûment compte des états de référence respectifs des systèmes, lorsque deux systèmes, qui peuvent être de compositions chimiques différentes, initialement séparés uniquement par une paroi imperméable, et autrement isolés , sont combinés en un nouveau système par l’opération thermodynamique d’enlèvement de la paroi, puis
tu 0 = tu 1 + tu 2 {displaystyle U_{0}=U_{1}+U_{2}} 
,
où U 0 désigne l’énergie interne du système combiné, et U 1 et U 2 désignent les énergies internes des systèmes séparés respectifs.
Adaptée à la thermodynamique, cette loi est une expression du principe de conservation de l’énergie , qui stipule que l’énergie peut être transformée (passée d’une forme à une autre), mais ne peut être ni créée ni détruite. [28]
L’énergie interne est une propriété principale de l’ état thermodynamique , tandis que la chaleur et le travail sont des modes de transfert d’énergie par lesquels un processus peut modifier cet état. Un changement d’énergie interne d’un système peut être obtenu par toute combinaison de chaleur ajoutée ou retirée et de travail effectué sur ou par le système. En fonction de l’état , l’énergie interne ne dépend pas de la manière, ou du cheminement par étapes intermédiaires, par lequel le système est arrivé à son état.
Deuxième loi
Une version traditionnelle de la deuxième loi de la thermodynamique stipule : La chaleur ne circule pas spontanément d’un corps plus froid vers un corps plus chaud.
La deuxième loi fait référence à un système de matière et de rayonnement, initialement avec des inhomogénéités de température, de pression, de potentiel chimique et d’autres propriétés intensives , qui sont dues à des «contraintes» internes, ou à des parois rigides imperméables, à l’intérieur, ou à des forces imposées de l’extérieur. . La loi observe que, lorsque le système est isolé du monde extérieur et de ces forces, il existe une grandeur thermodynamique définie, son entropie, qui augmente à mesure que les contraintes sont supprimées, atteignant finalement une valeur maximale à l’équilibre thermodynamique, lorsque les inhomogénéités disparaissent pratiquement. Pour les systèmes initialement éloignés de l’équilibre thermodynamique, bien que plusieurs aient été proposés, on ne connaît aucun principe physique général qui détermine les vitesses d’approche de l’équilibre thermodynamique, et la thermodynamique ne traite pas de ces vitesses. Les nombreuses versions de la deuxième loi expriment toutes l’ Irréversibilité d’une telle approche de l’équilibre thermodynamique.
En thermodynamique macroscopique , la deuxième loi est une observation de base applicable à tout processus thermodynamique réel; en Thermodynamique statistique, la deuxième loi est postulée comme étant une conséquence du chaos moléculaire.
Troisième loi
La troisième loi de la thermodynamique stipule : Lorsque la température d’un système se rapproche du zéro absolu, tous les processus cessent et l’entropie du système se rapproche d’une valeur minimale.
Cette loi de la thermodynamique est une loi statistique de la nature concernant l’entropie et l’impossibilité d’atteindre le zéro absolu de température. Cette loi fournit un point de référence absolu pour la détermination de l’entropie. L’entropie déterminée par rapport à ce point est l’entropie absolue. D’autres définitions incluent “l’entropie de tous les systèmes et de tous les états d’un système est la plus petite au zéro absolu”, ou de manière équivalente “il est impossible d’atteindre le zéro absolu de la température par un nombre fini de processus”.
Le zéro absolu, auquel toute activité s’arrêterait s’il était possible d’y parvenir, est de −273,15 °C (degrés Celsius), ou −459,67 °F (degrés Fahrenheit), ou 0 K (kelvin), ou 0° R (degrés Rankine ).
Modèles de système
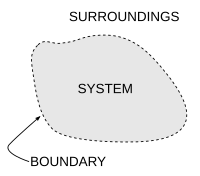
 Un schéma d’un système thermodynamique générique
Un schéma d’un système thermodynamique générique
Un concept important en thermodynamique est le système thermodynamique , qui est une région précisément définie de l’univers à l’étude. Tout dans l’univers, sauf le système, s’appelle l’ environnement . Un système est séparé du reste de l’univers par une frontière qui peut être physique ou notionnelle, mais sert à confiner le système à un volume fini. Des segments de la frontière sont souvent décrits comme des murs ; ils ont des ‘perméabilités’ respectives définies. Transferts d’énergie sous forme de travail , ou sous forme de chaleur , ou de matière, entre le système et l’environnement, s’effectuent à travers les murs, selon leurs perméabilités respectives.
La matière ou l’énergie qui traverse la frontière de manière à effectuer un changement dans l’énergie interne du système doit être prise en compte dans l’équation du bilan énergétique. Le volume contenu par les murs peut être la région entourant un seul atome d’énergie de résonance, comme Max Planck défini en 1900 ; il peut s’agir d’un corps de vapeur ou d’air dans une machine à vapeur , tel que Sadi Carnot l’ a défini en 1824. Le système pourrait également n’être qu’un seul nucléide (c’est-à-dire un système de quarks ) comme le suppose la thermodynamique quantique . Lorsqu’un point de vue plus lâche est adopté et que l’exigence d’équilibre thermodynamique est abandonnée, le système peut être le corps d’un cyclone tropical , tel queKerry Emanuel a théorisé en 1986 dans le domaine de la thermodynamique atmosphérique , ou l’ horizon des événements d’un trou noir .
Les frontières sont de quatre types : fixes, mobiles, réelles et imaginaires. Par exemple, dans un moteur, une limite fixe signifie que le piston est verrouillé à sa position, à l’intérieur de laquelle un processus à volume constant peut se produire. Si le piston est autorisé à se déplacer, cette limite est mobile tandis que les limites du cylindre et de la culasse sont fixes. Pour les systèmes fermés, les frontières sont réelles alors que pour les systèmes ouverts, les frontières sont souvent imaginaires. Dans le cas d’un moteur à réaction, une limite imaginaire fixe peut être supposée à l’admission du moteur, des limites fixes le long de la surface du carter et une seconde limite imaginaire fixe à travers la tuyère d’échappement.
Généralement, la thermodynamique distingue trois classes de systèmes, définies en fonction de ce qui est autorisé à franchir leurs frontières :
| Type de système | Débit massique | Travail | Chaleur |
|---|---|---|---|
| Ouvrir | |
|
|
| Fermé | |
|
|
| Isolation thermique | |
|
|
| Isolé mécaniquement | |
|
|
| Isolée | |
|
|
Au fil du temps dans un système isolé, les différences internes de pressions, de densités et de températures ont tendance à s’atténuer. Un système dans lequel tous les processus d’égalisation sont terminés est dit être dans un état d’ équilibre thermodynamique .
Une fois en équilibre thermodynamique, les propriétés d’un système sont, par définition, immuables dans le temps. Les systèmes en équilibre sont beaucoup plus simples et faciles à comprendre que les systèmes qui ne sont pas en équilibre. Souvent, lors de l’analyse d’un processus thermodynamique dynamique, l’hypothèse simplificatrice est faite que chaque état intermédiaire du processus est à l’équilibre, produisant des Processus thermodynamiques qui se développent si lentement qu’ils permettent à chaque étape intermédiaire d’être un état d’équilibre et sont dits processus réversibles. .
États et processus
Lorsqu’un système est à l’équilibre dans un ensemble donné de conditions, on dit qu’il est dans un état thermodynamique défini . L’état du système peut être décrit par un certain nombre de grandeurs d’état qui ne dépendent pas du processus par lequel le système est arrivé à son état. On les appelle variables intensives ou variables extensives selon la façon dont elles changent lorsque la taille du système change. Les propriétés du système peuvent être décrites par une équation d’état qui précise la relation entre ces variables. L’état peut être considéré comme la description quantitative instantanée d’un système avec un nombre défini de variables maintenues constantes.
Un processus thermodynamique peut être défini comme l’évolution énergétique d’un système thermodynamique passant d’un état initial à un état final. Il peut être décrit par des quantités de processus . Typiquement, chaque processus thermodynamique se distingue des autres processus à caractère énergétique en fonction des paramètres, tels que la température, la pression ou le volume, etc., qui sont maintenus fixes ; De plus, il est utile de regrouper ces processus en paires, dans lesquelles chaque variable maintenue constante est un membre d’une paire conjuguée .
Plusieurs Processus thermodynamiques couramment étudiés sont :
- Processus adiabatique : se produit sans perte ni gain d’énergie par la chaleur
- Processus isenthalpique : se produit à enthalpie constante
- Processus isentropique : un processus adiabatique réversible, se produit à entropie constante
- Processus isobare : se produit à pression constante
- Processus isochore : se produit à volume constant (également appelé isométrique/isovolumétrique)
- Processus isotherme : se produit à température constante
- Processus en régime permanent : se produit sans modification de l’ énergie interne
Instrumentation
Il existe deux types d’ instruments thermodynamiques , le compteur et le réservoir . Un compteur thermodynamique est un appareil qui mesure n’importe quel paramètre d’un système thermodynamique . Dans certains cas, le paramètre thermodynamique est en fait défini en termes d’instrument de mesure idéalisé. Par exemple, la loi zéro stipule que si deux corps sont en équilibre thermique avec un troisième corps, ils sont également en équilibre thermique l’un avec l’autre. Ce principe, comme l’a noté James Maxwell en 1872, affirme qu’il est possible de mesurer la température. Un thermomètre idéalisé est un échantillon d’un gaz parfait à pression constante. De la loi des gaz parfaits pV=nRT , le volume d’un tel échantillon peut être utilisé comme indicateur de température ; de cette manière, il définit la température. Bien que la pression soit définie mécaniquement, un appareil de mesure de la pression, appelé baromètre , peut également être construit à partir d’un échantillon d’un gaz parfait maintenu à une température constante. Un calorimètre est un appareil utilisé pour mesurer et définir l’énergie interne d’un système.
Un réservoir thermodynamique est un système dont la taille est telle que ses paramètres d’état ne sont pas sensiblement modifiés lorsqu’il est mis en contact avec le système d’intérêt. Lorsque le réservoir est mis en contact avec le système, le système est mis en équilibre avec le réservoir. Par exemple, un réservoir sous pression est un système à une pression particulière, qui impose cette pression au système auquel il est mécaniquement relié. L’atmosphère terrestre est souvent utilisée comme réservoir de pression. L’océan peut servir de réservoir de température lorsqu’il est utilisé pour refroidir les centrales électriques.
Variables conjuguées
Le concept central de la thermodynamique est celui d’ énergie , la capacité de faire un travail . Selon la première loi , l’énergie totale d’un système et de son environnement est conservée. L’énergie peut être transférée dans un système par chauffage, compression ou addition de matière, et extraite d’un système par refroidissement, expansion ou extraction de matière. En mécanique , par exemple, le transfert d’énergie est égal au produit de la force appliquée à un corps et du déplacement qui en résulte.
Les variables conjuguées sont des paires de concepts thermodynamiques, la première s’apparentant à une “force” appliquée à un système thermodynamique , la seconde s’apparentant au “déplacement” résultant et le produit des deux égalant la quantité d’énergie transférée. Les variables conjuguées courantes sont :
- Pression – volume (les paramètres mécaniques );
- Température – entropie (paramètres thermiques);
- Potentiel chimique – nombre de particules (paramètres du matériau).
Potentiels
Les potentiels thermodynamiques sont différentes mesures quantitatives de l’énergie stockée dans un système. Les potentiels sont utilisés pour mesurer les changements d’énergie dans les systèmes lorsqu’ils évoluent d’un état initial à un état final. Le potentiel utilisé dépend des contraintes du système, comme une température ou une pression constante. Par exemple, les énergies de Helmholtz et de Gibbs sont les énergies disponibles dans un système pour effectuer un travail utile lorsque la température et le volume ou la pression et la température sont fixes, respectivement.
Les cinq potentiels les plus connus sont :
| Nom | Symbole | Formule | Variables naturelles |
|---|---|---|---|
| Énergie interne | tu {displaystyle U}  |
∫ ( T d S − p d V + ∑ i μ i d N i ) {displaystyle int left(T,dS-p,dV+sum _{i}mu _{i}dN_{i}right)}  |
S , V , { N i } {displaystyle S,V,{N_{i}}}  |
| Énergie libre de Helmholtz | F {displaystyle F}  |
U − T S {displaystyle U-TS}  |
T , V , { N i } {displaystyle T,V,{N_{i}}}  |
| Enthalpie | H {displaystyle H}  |
U + p V {displaystyle U+pV}  |
S , p , { N i } {displaystyle S,p,{N_{i}}}  |
| Énergie libre de Gibbs | G {displaystyle G}  |
U + p V − T S {displaystyle U+pV-TS}  |
T , p , { N i } {displaystyle T,p,{N_{i}}}  |
| Potentiel Landau, ou grand potentiel |
Ω {displaystyle Oméga}   |
U − T S − {displaystyle U-TS-}    |
T , V , { μ i } {displaystyle T,V,{mu _{i}}}  |
où T {displaystyle T} 
est la température , S {displaystyle S}

l’ entropie , p {displaystyle p}

la pression , V {displaystyle V}

le volume , μ {displaystylemu}

le potentiel chimique , N {displaystyle N}

le nombre de particules dans le système, et i {displaystyle i}

est le nombre de types de particules dans le système.
Les potentiels thermodynamiques peuvent être dérivés de l’équation du bilan énergétique appliquée à un système thermodynamique. D’autres potentiels thermodynamiques peuvent également être obtenus par transformation de Legendre .
Champs appliqués
- Thermodynamique atmosphérique
- Thermodynamique biologique
- Thermodynamique des trous noirs
- Thermodynamique chimique
- Thermodynamique classique
- Thermodynamique d’équilibre
- Écologie industrielle (re: Exergy )
- Thermodynamique à entropie maximale
- Thermodynamique hors équilibre
- Philosophie de la physique thermique et statistique
- Psychrométrie
- Thermodynamique quantique
- Thermodynamique statistique , c’est-à-dire Mécanique statistique
- Thermoéconomie
- Chimie des polymères
- Thermodynamique des énergies renouvelables
Voir également
-

 Portail de physique
Portail de physique
- Chemin de processus thermodynamique
Listes et délais
- Liste des publications importantes en thermodynamique
- Liste des manuels de thermodynamique et de mécanique statistique
- Liste des conductivités thermiques
- Liste des propriétés thermodynamiques
- Tableau des équations thermodynamiques
- Chronologie de la thermodynamique
Remarques
- ↑ La convention de signe (Q est la chaleur fournie au système, W est le travail effectué par le système) est celle de Rudolf Clausius . La convention de signe opposé est habituelle en thermodynamique chimique.
Références
- ^ Clausius, Rodolphe (1850). Sur la puissance motrice de la chaleur, et sur les lois qu’on peut en déduire pour la théorie de la chaleur . Annalen der Physik de Poggendorff, LXXIX (réimpression de Douvres). ISBN 978-0-486-59065-3.
- ^ William Thomson, LL.DDCL, FRS (1882). Epreuves Mathématiques et Physiques . Vol. 1. Londres, Cambridge : CJ Clay, MA et fils, Cambridge University Press. p. 232. Archivé de l’original le 18 avril 2021 . Récupéré le 2 novembre 2020 . {{cite book}}: CS1 maint: multiple names: authors list (link)
- ^ un b Gibbs, Willard, J. (1874–1878). Transactions de l’Académie des arts et des sciences du Connecticut . Vol. III. Nouveau Havre. p. 108–248 , 343–524. {{cite book}}: CS1 maint: multiple names: authors list (link)
- ^ un b Duhem, PMM (1886). Le Potentiel Thermodynamique et ses Applications , Hermann, Paris.
- ^ un b Lewis, Gilbert N.; Randall, Merle (1923). Thermodynamique et énergie libre des substances chimiques . McGraw-Hill Book Co. Inc.
- ^ un b Guggenheim, EA (1933). Thermodynamique moderne par les méthodes de JW Gibbs , Methuen, Londres.
- ^ un b Guggenheim, EA (1949/1967). Thermodynamique. An Advanced Treatment for Chemists and Physicists , 1ère édition 1949, 5ème édition 1967, North-Holland, Amsterdam.
- ^ Ilya Prigogine, I. & Defay, R., traduit par DH Everett (1954). Thermodynamique chimique . Longmans, Green & Co., Londres. Comprend la thermodynamique hors équilibre classique. {{cite book}}: CS1 maint: multiple names: authors list (link)
- ^ Enrico Fermi (1956). Thermodynamique . Courrier Douvres Publications. p. ix. ISBN 978-0486603612. OCLC 230763036 . Archivé de l’original le 18 avril 2021 . Récupéré le 2 novembre 2020 .
- ^ un bc Perrot , Pierre (1998). A à Z de la thermodynamique . Presse universitaire d’Oxford. ISBN 978-0-19-856552-9. OCLC 123283342 .
- ^ Clark, John, OE (2004). Le dictionnaire essentiel de la science . Livres Barnes & Nobles. ISBN 978-0-7607-4616-5. OCLC 58732844 .{{cite book}}: CS1 maint: multiple names: authors list (link)
- ^ Van Ness, HC (1983) [1969]. Comprendre la thermodynamique . Dover Publications, Inc. ISBN 9780486632773. OCLC 8846081 .
- ^ Dugdale, JS (1998). L’entropie et sa signification physique . Taylor et François. ISBN 978-0-7484-0569-5. OCLC 36457809 .
- ^ Smith, JM; Van Ness, HC ; Abbott, MM (2005). Introduction à la thermodynamique du génie chimique (7e éd.). p. 584. Bibcode : 1950JChEd..27..584S . ISBN 978-0-07-310445-4. OCLC 56491111 .
- ^ Haynie, Donald, T. (2001). Thermodynamique biologique . La presse de l’Universite de Cambridge. ISBN 978-0-521-79549-4. OCLC 43993556 .{{cite book}}: CS1 maint: multiple names: authors list (link)
- ^ Écoles de thermodynamique Archivé le 7 décembre 2017 à la Wayback Machine – EoHT.info.
- ^ Partington, JR (1989). Une brève histoire de la chimie . Douvres. OCLC 19353301 .
- ^ Le moteur Newcomen a été amélioré de 1711 jusqu’aux travaux de Watt, rendant la comparaison d’efficacité sujette à qualification, mais l’augmentation par rapport à la version 1865 était de l’ordre de 100%.
- ^ Cengel, Yunus A.; Boles, Michael A. (2005). Thermodynamique – une approche d’ingénierie . McGraw-Hill. ISBN 978-0-07-310768-4.
- ^ Gibbs, Willard (1993). Les articles scientifiques de J. Willard Gibbs, volume un : thermodynamique . Presse à arc de bœuf. ISBN 978-0-918024-77-0. OCLC 27974820 .
- ^ un bc “la Thermodynamique (l’étymologie)” . EoHT.info. Archivé de l’original le 25 mai 2010 . Récupéré le 24 juillet 2010 .
- ^ Donald T. Haynie (2008). Thermodynamique biologique (2 éd.). La presse de l’Universite de Cambridge. p. 26 .
- ^ un b Kelvin, William T. (1849) “Un compte rendu de la théorie de Carnot sur la puissance motrice de la chaleur – avec des résultats numériques déduits des expériences de Regnault sur la vapeur.” Transactions de la Société royale d’Édimbourg, XVI. 2 janvier. Copie numérisée archivée le 24 juillet 2017 sur la Wayback Machine
- ^ Klotz, Irving (2008). Thermodynamique chimique : théorie et méthodes de base . Hoboken, New Jersey : John Wiley & Sons, Inc. p. 4. ISBN 978-0-471-78015-1.
- ^ Pokrovski, Vladimir (2020). Thermodynamique des systèmes complexes : principes et applications . IOP Publishing, Bristol, Royaume-Uni.
- ^ Moran, Michael J. et Howard N. Shapiro, 2008. Principes fondamentaux de l’ingénierie thermodynamique . 6e éd. Wiley et fils : 16.
- ^ Bailyn, M. (1994). A Survey of Thermodynamics , American Institute of Physics, AIP Press, Woodbury NY, ISBN 0883187973 , p. 79.
- ^ Callen, HB (1960/1985). Thermodynamics and an Introduction to Thermostatistics , deuxième édition, John Wiley & Sons, Hoboken NY, ISBN 9780471862567 , pp. 11–13.
Lectures complémentaires
- Goldstein, Martin & Inge F. (1993). Le réfrigérateur et l’univers . Presse universitaire de Harvard. ISBN 978-0-674-75325-9. OCLC 32826343 .Une introduction non technique, bonne sur les questions historiques et interprétatives.
- Kazakov, Andrei; Muzny, Chris D.; Chirico, Robert D.; Diky, Vladimir V.; Frenkel, Michael (2008). “Web Thermo Tables – une version en ligne des tables thermodynamiques TRC” . Journal de recherche de l’Institut national des normes et de la technologie . 113 (4): 209-220. doi : 10.6028/jres.113.016 . ISSN 1044-677X . PMC 4651616 . PMID 27096122 .
- Gibbs JW (1928). Les œuvres complètes de J. Willard Gibbs Thermodynamique . New York : Longmans, Green and Co.Vol. 1, p. 55–349.
- Guggenheim EA (1933). Thermodynamique moderne par les méthodes de Willard Gibbs . Londres : Methuen & co. ltd.
- En ligneDenbigh K. (1981). Les principes de l’équilibre chimique : avec des applications en chimie et en génie chimique . Londres : Cambridge University Press.
- Stull, DR, Westrum Jr., EF et Sinke, GC (1969). La thermodynamique chimique des composés organiques . Londres : John Wiley and Sons, Inc.{{cite book}}: CS1 maint: multiple names: authors list (link)
- Bazarov IP (2010). Thermodynamique: Manuel . Saint-Pétersbourg : maison d’édition Lan. p. 384.ISBN _ 978-5-8114-1003-3.5e éd. (en russe)
- Bawendi Moungi G., Alberty Robert A. et Silbey Robert J. (2004). Chimie Physique . J. Wiley & Sons, Incorporé.
- Alberty Robert A. (2003). Thermodynamique des réactions biochimiques . Wiley-Interscience.
- Alberty Robert A. (2006). Thermodynamique biochimique : applications de Mathematica . Méthodes d’analyse biochimique . Vol. 48. John Wiley & Sons, Inc. p. 1–458. ISBN 978-0-471-75798-6. PMID 16878778 .
- Aneth Ken A., Bromberg Sarina (2011). Forces motrices moléculaires : Thermodynamique statistique en biologie, chimie, physique et nanosciences . Science des guirlandes. ISBN 978-0-8153-4430-8.
- M. Scott Shell (2015). Thermodynamique et mécanique statistique : une approche intégrée . La presse de l’Universite de Cambridge. ISBN 978-1107656789.
- Douglas E. Barrick (2018). Thermodynamique biomoléculaire : de la théorie aux applications . Presse CRC. ISBN 978-1-4398-0019-5.
Les titres suivants sont plus techniques :
- Béjan, Adrien (2016). Advanced Engineering Thermodynamics (4 éd.). Wiley. ISBN 978-1-119-05209-8.
- Cengel, Yunus A., & Boles, Michael A. (2002). Thermodynamique – une approche d’ingénierie . Mcgraw Hill. ISBN 978-0-07-238332-4. OCLC 45791449 .{{cite book}}: CS1 maint: multiple names: authors list (link)
- Dunning-Davies, Jeremy (1997). Thermodynamique concise : principes et applications . Éditions Horwood. ISBN 978-1-8985-6315-0. OCLC 36025958 .
- Kroemer, Herbert & Kittel, Charles (1980). Physique Thermique . Société WH Freeman. ISBN 978-0-7167-1088-2. OCLC 32932988 .
Liens externes
-

 Médias liés à la thermodynamique sur Wikimedia Commons
Médias liés à la thermodynamique sur Wikimedia Commons
| Wikibooks a un livre sur le thème : Ingénierie de la thermodynamique |
| Wikiquote a des citations liées à la thermodynamique . |
- Callendar, Hugh Longbourne (1911). “Thermodynamique” . Encyclopædia Britannica . Vol. 26 (11e éd.). pages 808–814.
- Sites Web de données thermodynamiques et de calcul de propriétés
- Sites Web éducatifs sur la thermodynamique
- Biochimie Thermodynamique
- Thermodynamique et mécanique statistique
- Ingénierie thermodynamique – Une approche graphique
- Thermodynamique et mécanique statistique par Richard Fitzpatrick