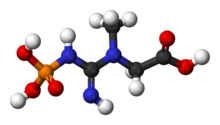
La phosphocréatine , également connue sous le nom de créatine phosphate ( CP ) ou PCr ( Pcr ), est une molécule de créatine phosphorylée qui sert de réserve rapidement mobilisable de phosphates à haute énergie dans Le muscle squelettique , le Myocarde et le cerveau pour recycler l’ adénosine triphosphate , la monnaie énergétique de la cellule.
 |
|
 |
|
| Des noms | |
|---|---|
| Nom IUPAC N -Méthyl- N -(phosphonocarbamimidoyl)glycine | |
| Autres noms Phosphate de créatine; phosphorylcréatine; créatine-P; phosphagène; fosfocréatine | |
| Identifiants | |
| Numero CAS |
|
| Modèle 3D ( JSmol ) |
|
| Abréviations | PCR |
| Référence Beilstein | 1797096 |
| ChEBI |
|
| ChEMBL |
|
| ChemSpider |
|
| DrugBank |
|
| Carte d’information de l’ECHA | 100.000.585 |
| Numéro CE |
|
| KEGG |
|
| CID PubChem |
|
| UNII |
|
| Tableau de bord CompTox ( EPA ) |
|
InChI
|
|
SOURIRES
|
|
| Propriétés | |
| Formule chimique | C4H10N3O5P _ _ _ _ _ _ _ _ |
| Masse molaire | 211,114 g · mol -1 |
| Pharmacologie | |
| Code ATC | C01EB06 ( OMS ) |
| Dangers | |
| Étiquetage SGH : | |
| Pictogrammes |  |
| Mention d’avertissement | Avertissement |
| Mentions de danger | H315 , H319 , H335 |
| Conseils de prudence | P261 , P264 , P271 , P280 , P302+P352 , P304+P340 , P305+P351+P338 , P312 , P321 , P332+P313 , P337+P313 , P362 , P403+P233 , P405 , P501 |
| Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
Chimie
Dans les reins, l’enzyme AGAT catalyse la conversion de deux acides aminés – l’arginine et la glycine – en Guanidinoacétate (également appelé glycocyamine ou GAA), qui est ensuite transporté dans le sang vers le foie. Un groupe méthyle est ajouté au GAA à partir de l’acide aminé méthionine par l’enzyme GAMT , formant de la créatine non phosphorylée. Celle-ci est ensuite libérée dans le sang par le foie où elle se déplace principalement vers les cellules musculaires (95 % de la créatine corporelle se trouve dans les muscles) et, dans une moindre mesure, vers le cerveau, le cœur et le pancréas. Une fois à l’intérieur des cellules, il est transformé en phosphocréatine par le complexe enzymatique créatine kinase .
La phosphocréatine est capable de donner son groupe phosphate pour convertir l’ adénosine diphosphate (ADP) en adénosine triphosphate (ATP). Ce processus est une composante importante des systèmes bioénergétiques de tous les vertébrés. Par exemple, alors que le corps humain ne produit que 250 g d’ATP par jour, il recycle chaque jour tout son poids corporel en ATP grâce à la créatine phosphate.
La phosphocréatine peut être décomposée en créatinine , qui est ensuite excrétée dans l’urine. Un homme de 70 kg contient environ 120 g de créatine, dont 40 % sous forme non phosphorylée et 60 % sous forme de phosphate de créatine. De cette quantité, 1 à 2 % sont décomposés et excrétés chaque jour sous forme de créatinine.
La phosphocréatine est utilisée par voie intraveineuse dans les hôpitaux de certaines parties du monde pour des problèmes cardiovasculaires sous le nom de Neoton, et également utilisée par certains athlètes professionnels, car ce n’est pas une substance contrôlée.
Une fonction
La phosphocréatine peut donner de manière anaérobie un groupe phosphate à l’ ADP pour former de l’ ATP pendant les cinq à huit premières secondes d’un effort musculaire maximal. [ citation nécessaire ] Inversement, un excès d’ ATP peut être utilisé pendant une période de faible effort pour reconvertir la créatine en phosphocréatine.
La phosphorylation réversible de la créatine (c’est-à-dire la réaction avant et arrière) est catalysée par plusieurs créatine kinases . La présence de créatine kinase ( CK-MB , bande myocardique de créatine kinase) dans le plasma sanguin indique une lésion tissulaire et est utilisée dans le diagnostic de l’infarctus du Myocarde. [1]
La capacité de la cellule à générer de la phosphocréatine à partir d’un excès d’ ATP pendant le repos, ainsi que son utilisation de la phosphocréatine pour une régénération rapide de l’ATP pendant une activité intense, fournit un tampon spatial et temporel de la concentration d’ ATP . En d’autres termes, la phosphocréatine agit comme réserve de haute énergie dans une réaction couplée ; l’énergie dégagée par le don du groupe phosphate est utilisée pour régénérer l’autre composé – dans ce cas, l’ATP . La phosphocréatine joue un rôle particulièrement important dans les tissus qui ont des besoins énergétiques élevés et fluctuants, tels que les muscles et le cerveau.
Histoire
La découverte de la phosphocréatine [2] [3] a été rapportée par Grace et Philip Eggleton de l’ Université de Cambridge [4] et séparément par Cyrus Fiske et Yellapragada Subbarow de la Harvard Medical School [5] en 1927. Quelques années plus tard, David Nachmansohn , travaillant sous Meyerhof à l’ Institut Kaiser Wilhelm à Dahlem, Berlin, a contribué à la compréhension du rôle de la phosphocréatine dans la cellule. [3]
Références
- ^ Schlattner U, Tokarska-Schlattner M, Wallimann T (2006). “Créatine kinase mitochondriale dans la santé et la maladie humaines” . Biochimica et Biophysica Acta (BBA) – Base moléculaire de la maladie . 1762 (2): 164-180. doi : 10.1016/j.bbadis.2005.09.004 . PMID 16236486 .
- ^ Saks, Valdur (2007). Bioénergétique des systèmes moléculaires : énergie pour la vie . Weinheim : Wiley-VCH. p. 2 . ISBN 978-3-527-31787-5.
- ^ un b Ochoa, Severo (1989). Sherman, EJ; Académie nationale des sciences (éd.). David Nachmansohn . Mémoires biographiques. Vol. 58. Presse des académies nationales. pp. 357–404. ISBN 978-0-309-03938-3.
- ^ Eggleton, Philippe; Eggleton, Grace Palmer (1927). “Le phosphate inorganique et une forme labile de phosphate organique dans le gastrocnémien de la grenouille” . Journal biochimique . 21 (1): 190–195. doi : 10.1042/bj0210190 . PMC 1251888 . PMID 16743804 .
- ^ Fiske, Cyrus H.; Subbarao, Yellapragada (1927). “La nature du” phosphate inorganique “dans Le muscle volontaire”. Sciences . 65 (1686): 401–403. Bibcode : 1927Sci….65..401F . doi : 10.1126/science.65.1686.401 . PMID 17807679 .
Liens externes
- Base de données sur le métabolome humain de l’ Université de l’Alberta