Éther
Les éthers sont une classe de composés organiques qui contiennent un groupe éther – un atome d’ oxygène relié à deux groupes alkyle ou aryle . Ils répondent à la formule générale R–O–R′, où R et R′ représentent les groupes alkyle ou aryle. Les éthers peuvent à nouveau être classés en deux variétés : si les groupes alkyle ou aryle sont les mêmes des deux côtés de l’ atome d’ oxygène , alors c’est un éther simple ou symétrique, alors que s’ils sont différents, les éthers sont appelés éthers mixtes ou dissymétriques. [1] Un exemple typique du premier groupe est le solvant et l’éther diéthylique Anesthésique , communément appelé simplement « éther » ( CH 3 –CH 2 –O–CH 2 –CH 3 ). Les éthers sont courants en chimie organique et encore plus répandus en biochimie, car ce sont des liaisons courantes dans les glucides et la lignine . [2]
 La structure générale d’un éther. R et R’ représentent n’importe quel substituant alkyle ou aryle .
La structure générale d’un éther. R et R’ représentent n’importe quel substituant alkyle ou aryle .
Structure et collage
Les éthers présentent des liaisons C – O – C courbées. Dans l’éther diméthylique , l’ angle de liaison est de 111° et les distances C–O sont de 141 pm . [3] La barrière à la rotation autour des liaisons C–O est faible. La liaison de l’oxygène dans les éthers, les alcools et l’eau est similaire. Dans le langage de la théorie des liaisons de valence , l’hybridation à l’oxygène est sp 3 .
L’oxygène est plus électronégatif que le carbone, ainsi les hydrogènes alpha des éthers sont plus acides que ceux des hydrocarbures simples. Cependant, ils sont beaucoup moins acides que les hydrogènes alpha des groupes carbonyle (comme dans les Cétones ou les Aldéhydes ).
Les éthers peuvent être symétriques de type ROR ou dissymétriques de type ROR’. Des exemples du premier sont l’éther diéthylique , l’éther diméthylique, l’Éther dipropylique , etc. Des éthers asymétriques illustratifs sont l’anisole (méthoxybenzène) et le diméthoxyéthane .
Éthers vinyliques et acétyléniques
Les éthers vinyliques et acétyléniques sont beaucoup moins courants que les éthers alkyliques ou aryliques. Les éthers vinyliques, souvent appelés éthers d’énol , sont des intermédiaires importants dans la synthèse organique . Les éthers acétyléniques sont particulièrement rares. Le di-tert-butoxyacétylène est l’exemple le plus courant de cette classe rare de composés.
Nomenclature
Dans le système de Nomenclature IUPAC , les éthers sont nommés en utilisant la formule générale « alcoxyalcane » , par exemple CH 3 –CH 2 –O–CH 3 est le Méthoxyéthane . Si l’éther fait partie d’une molécule plus complexe, il est décrit comme un substituant alcoxy, donc –OCH 3 serait considéré comme un groupe « Méthoxy – » . Le radical alkyle le plus simple est écrit devant, donc CH 3 –O–CH 2 CH 3 serait donné comme Méthoxy (CH 3 O) éthane (CH 2 CH 3).
Nom trivial
Les règles IUPAC ne sont souvent pas suivies pour les éthers simples. Les noms triviaux des éthers simples (c’est-à-dire ceux qui n’ont pas ou peu d’autres groupes fonctionnels) sont un composé des deux substituants suivis de « éther ». Par exemple, éthyl méthyl éther (CH 3 OC 2 H 5 ), diphényléther (C 6 H 5 OC 6 H 5 ). Comme pour les autres composés organiques, des éthers très courants ont acquis des noms avant que les règles de nomenclature ne soient formalisées. L’éther diéthylique est simplement appelé éther, mais était autrefois appelé huile douce de vitriol . L’éther méthylphénylique est de l’ anisole , car on le trouvait à l’origine dans l’ Anis . L’ aromatiqueles éthers comprennent les furanes . Les acétals (éthers α-alcoxy R–CH(–OR)–O–R) sont une autre classe d’éthers aux propriétés caractéristiques.
Polyéthers
Les polyéthers sont généralement des polymères contenant des liaisons éther dans leur chaîne principale. Le terme polyol fait généralement référence à des polyols de polyéther avec un ou plusieurs groupes terminaux fonctionnels tels qu’un groupe Hydroxyle . Le terme “oxyde” ou d’autres termes sont utilisés pour un polymère de masse molaire élevée lorsque les groupes terminaux n’affectent plus les propriétés du polymère.
Les éthers couronnes sont des polyéthers cycliques. Certaines toxines produites par les dinoflagellés telles que la brévétoxine et la ciguatoxine sont extrêmement volumineuses et sont connues sous le nom de polyéthers cycliques ou en échelle .
| Nom des polymères de masse molaire faible à moyenne | Nom des polymères à haute masse molaire | Préparation | Unité répétitive | Exemples de noms commerciaux |
|---|---|---|---|---|
| Paraformaldéhyde | Polyoxyméthylène (POM) ou polyacétal ou polyformaldéhyde | Polymérisation par étapes du formaldéhyde | –CH 2 O– | Delrin de DuPont |
| Polyéthylène glycol (PEG) | Oxyde de polyéthylène (PEO) ou polyoxyéthylène (POE) | Polymérisation par ouverture de cycle de l’oxyde d’ éthylène | –CH 2 CH 2 O– | Carbowax de Dow |
| Polypropylène glycol (PPG) | Oxyde de polypropylène (PPOX) ou polyoxypropylène (POP) | polymérisation anionique par ouverture de cycle de l’oxyde de propylène | –CH 2 CH(CH 3 )O– | Arcol de Covestro |
| Polytétraméthylène glycol (PTMG) ou Polytétraméthylène éther glycol (PTMEG) | Polytétrahydrofuranne (PTHF) | Polymérisation par ouverture de cycle catalysée par un acide du tétrahydrofurane | –CH2CH2CH2CH2O– | Térathane d’ Invista et PolyTHF de BASF |
Les polymères phényléthers sont une classe de polyéthers aromatiques contenant des cycles aromatiques dans leur chaîne principale : polyphényléther (PPE) et poly( p -phénylène oxyde) (PPO).
Composés apparentés
De nombreuses classes de composés avec des liaisons C–O–C ne sont pas considérées comme des éthers : Esters (R–C(=O)–O–R′), hémiacétals (R–CH(–OH)–O–R′), acide carboxylique anhydrides (RC(=O)–O–C(=O)R′).
Propriétés physiques
Les éthers ont des points d’ébullition similaires à ceux des Alcanes analogues . Les éthers simples sont généralement incolores.
| Données sélectionnées sur certains éthers alkyliques | |||||
|---|---|---|---|---|---|
| Éther | Structure | mp (°C) | pb (°C) | Solubilité dans 1 litre de H 2 O | Moment dipolaire ( D ) |
| Éther diméthylique | CH 3 –O–CH 3 | −138,5 | −23,0 | 70 g | 1h30 |
| L’éther diéthylique | CH 3 CH 2 –O–CH 2 CH 3 | −116,3 | 34.4 | 69 grammes | 1.14 |
| Tétrahydrofurane | O(CH 2 ) 4 | −108,4 | 66,0 | Miscible | 1,74 |
| Dioxane | O(C 2 H 4 ) 2 O | 11.8 | 101.3 | Miscible | 0,45 |
Réactions

 Structure du peroxyde d’éther diéthylique polymère
Structure du peroxyde d’éther diéthylique polymère
Les liaisons CO qui composent les éthers simples sont fortes. Ils ne réagissent qu’aux bases les plus fortes. Bien que généralement de faible réactivité chimique , ils sont plus réactifs que les Alcanes .
Les éthers spécialisés tels que les époxydes , les cétals et les acétals sont des classes non représentatives d’éthers et sont discutés dans des articles séparés. Les réactions importantes sont énumérées ci-dessous. [4]
Clivage
Bien que les éthers résistent à l’hydrolyse, ils sont clivés par l’acide bromhydrique et l’acide iodhydrique . Le chlorure d’hydrogène ne clive les éthers que lentement. Les éthers méthyliques donnent généralement des halogénures de méthyle :
ROCH 3 + HBr → CH 3 Br + ROH
Ces réactions se déroulent via des intermédiaires onium , c’est-à-dire [RO(H)CH 3 ] + Br − .
Certains éthers subissent un clivage rapide avec du tribromure de bore (même du chlorure d’aluminium est utilisé dans certains cas) pour donner le bromure d’alkyle. [5] Selon les substituants, certains éthers peuvent être clivés avec une variété de réactifs, par exemple une base forte.
Formation de peroxyde
Lorsqu’ils sont stockés en présence d’air ou d’oxygène, les éthers ont tendance à former des peroxydes explosifs , tels que l’Hydroperoxyde d’éther diéthylique . La réaction est accélérée par la lumière, les catalyseurs métalliques et les Aldéhydes. En plus d’éviter les conditions de stockage susceptibles de former des peroxydes, il est recommandé, lorsqu’un éther est utilisé comme solvant, de ne pas le distiller à sec, car les peroxydes éventuellement formés, étant moins volatils que l’éther d’origine, se concentreront dans les dernières gouttes de liquide. La présence de peroxyde dans d’anciens échantillons d’éthers peut être détectée en les secouant avec une solution fraîchement préparée d’un sulfate ferreux suivi de l’ajout de KSCN. L’apparition d’une couleur rouge sang indique la présence de peroxydes. Les propriétés dangereuses des peroxydes d’éther sont la raison pour laquelle l’éther diéthylique et d’autres éthers formant des peroxydes comme le tétrahydrofurane (THF) ou l’éther diméthylique d’éthylène glycol (1,2-diméthoxyéthane) sont évités dans les procédés industriels.
Bases de Lewis

 Structure de VCl 3 (thf) 3 . [6]
Structure de VCl 3 (thf) 3 . [6]
Les éthers servent de bases de Lewis . Par exemple, l’éther diéthylique forme un complexe avec le trifluorure de bore , c’est-à-dire l’éthérate diéthylique (BF 3 ·OEt 2 ). Les éthers se coordonnent également au centre Mg des réactifs de Grignard . Le tétrahydrofuranne est plus basique que les éthers acycliques. Il forme des complexes avec de nombreux halogénures métalliques.
Alpha-halogénation
Cette réactivité est similaire à la tendance des éthers avec des atomes d’hydrogène alpha à former des peroxydes. La réaction avec le chlore produit des alpha-chloroéthers.
Synthèse
Les éthers peuvent être préparés par de nombreuses voies. En général, les éthers alkyliques se forment plus facilement que les éthers aryliques, les dernières espèces nécessitant souvent des catalyseurs métalliques. [7]
La synthèse de l’éther diéthylique par réaction entre l’ éthanol et l’acide sulfurique est connue depuis le XIIIe siècle. [8]
Déshydratation des alcools
La déshydratation des alcools donne des éthers : [9]
2 R–OH → R–O–R + H 2 O à haute température 

Cette réaction de substitution nucléophile directe nécessite des températures élevées (environ 125 °C). La réaction est catalysée par des acides, généralement de l’acide sulfurique. La méthode est efficace pour générer des éthers symétriques, mais pas des éthers asymétriques, puisque l’un ou l’autre OH peut être protoné, ce qui donnerait un mélange de produits. L’éther diéthylique est produit à partir d’éthanol par cette méthode. Les éthers cycliques sont facilement générés par cette approche. Les réactions d’élimination concurrencent la déshydratation de l’alcool :
R–CH 2 –CH 2 (OH) → R–CH=CH 2 + H 2 O
La voie de déshydratation nécessite souvent des conditions incompatibles avec des molécules délicates. Plusieurs méthodes plus douces existent pour produire des éthers.
Synthèse d’éther de Williamson
Déplacement nucléophile des halogénures d’ alkyle par des alcoxydes
R–ONa + R′–X → R–O–R′ + Na X
Cette réaction s’appelle la synthèse de l’éther de Williamson . Cela implique le traitement d’un alcool parent avec une base forte pour former l’alcoolate, suivi de l’ajout d’un composé aliphatique approprié portant un groupe partant approprié (R – X). Les groupes partants (X) appropriés comprennent l’iodure , le bromure ou les sulfonates . Cette méthode ne fonctionne généralement pas bien pour les halogénures d’aryle (par exemple le bromobenzène, voir condensation d’Ullmann ci-dessous). De même, cette méthode ne donne les meilleurs rendements que pour les halogénures primaires. Les halogénures secondaires et tertiaires sont susceptibles de subir une élimination E2 lors de l’exposition à l’anion alcoxyde basique utilisé dans la réaction en raison de l’encombrement stérique des grands groupes alkyle.
Dans une réaction apparentée, les halogénures d’alkyle subissent un déplacement nucléophile par les phénoxydes . Le R–X ne peut pas être utilisé pour réagir avec l’alcool. Cependant , les phénols peuvent être utilisés pour remplacer l’alcool tout en conservant l’halogénure d’alkyle. Comme les phénols sont acides, ils réagissent facilement avec une base forte comme l’hydroxyde de sodium pour former des ions phénoxyde. L’ion phénoxyde remplacera alors le groupe -X dans l’halogénure d’alkyle, formant un éther avec un groupe aryle qui lui est attaché dans une réaction avec un mécanisme S N 2 .
C 6 H 5 OH + OH − → C 6 H 5 –O − + H 2 O C 6 H 5 –O − + R–X → C 6 H 5 OU
Condensation d’Ullmann
La condensation d’Ullmann est similaire à la méthode de Williamson sauf que le substrat est un halogénure d’aryle. De telles réactions nécessitent généralement un catalyseur, tel que le cuivre.
Addition électrophile d’alcools à des alcènes
Les alcools s’ajoutent aux alcènes activés électrophiliquement .
R 2 C=CR 2 + R–OH → R 2 CH–C(–O–R)–R 2
Une catalyse acide est nécessaire pour cette réaction. Souvent, le trifluoroacétate de mercure (Hg(OCOCF 3 ) 2 ) est utilisé comme catalyseur pour la réaction générant un éther avec la régiochimie de Markovnikov . En utilisant des réactions similaires, les éthers tétrahydropyranyliques sont utilisés comme groupes protecteurs pour les alcools.
Préparation des époxydes
Les époxydes sont généralement préparés par oxydation d’alcènes. L’époxyde le plus important en termes d’échelle industrielle est l’oxyde d’éthylène, qui est produit par oxydation de l’éthylène avec de l’oxygène. D’autres époxydes sont produits par l’une des deux voies suivantes :
- Par l’oxydation d’alcènes avec un peroxyacide tel que m -CPBA .
- Par substitution nucléophile intramoléculaire de base d’une halohydrine .
Éthers importants
  |
Oxyde d’éthylène | Un éther cyclique. Aussi l’ époxyde le plus simple . |
| |
Éther diméthylique | Gaz incolore utilisé comme propulseur d’aérosol . Un carburant alternatif renouvelable potentiel pour les moteurs diesel avec un indice de cétane aussi élevé que 56-57. |
| |
L’éther diéthylique | Liquide incolore à odeur sucrée. Un solvant courant à faible point d’ébullition (point d’ébullition 34,6 °C) et un Anesthésique précoce . Utilisé comme liquide de démarrage pour les moteurs diesel. Également utilisé comme réfrigérant et dans la fabrication de poudre à canon sans fumée , ainsi qu’en parfumerie . |
| |
Diméthoxyéthane (DME) | Solvant miscible à l’eau souvent présent dans les batteries au lithium (Eb 85 °C) : |
  |
Dioxane | Un éther cyclique et un solvant à point d’ébullition élevé (Eb 101,1 °C). |
  |
Tétrahydrofuranne (THF) | Un éther cyclique, l’un des éthers simples les plus polaires qui est utilisé comme solvant. |
  |
Anisole (méthoxybenzène) | Un éther d’aryle et un constituant majeur de l’ huile essentielle de graine d’ Anis . |
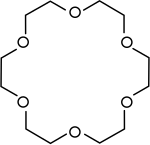  |
Éthers couronnes | Polyéthers cycliques utilisés comme catalyseurs de transfert de phase . |
  |
Polyéthylène glycol (PEG) | Un polyéther linéaire, par exemple utilisé dans les cosmétiques et les produits pharmaceutiques . |
| Polypropylène glycol | Un polyéther linéaire, par exemple utilisé dans les polyuréthanes . | |
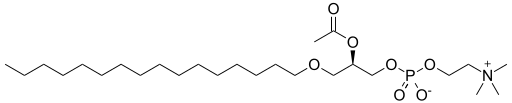  |
Facteur d’activation plaquettaire | Un éther lipide , un exemple avec un éther sur sn-1, un ester sur sn-2 et un éther inorganique sur sn-3 de l’échafaudage glycéryle. |
Voir également
- Ester
- Éther lipide
- Dépendance à l’éther
- Éther (chanson)
- Histoire de l’anesthésie générale
- Inhalant
Références
- ^ IUPAC , Compendium de terminologie chimique , 2e éd. (le “Livre d’or”) (1997). Version corrigée en ligne : (2006–) ” ethers “. doi : 10.1351/goldbook.E02221
- ^ Saul Patai, éd. (1967). La liaison éther . Chimie des groupes fonctionnels de PATAI. John Wiley et fils. doi : 10.1002/9780470771075 . ISBN 9780470771075.
- ^ Vojinović, Krunoslav; Losehand, Udo ; Mitzel, Norbert W. (2004). “Agrégation de dichlorosilane-éther diméthylique: un nouveau motif dans la formation d’adduits d’halosilane”. Dalton Trans. (16): 2578-2581. doi : 10.1039/b405684a . PMID 15303175 .
- ^ Wilhelm Heitmann, Günther Strehlke, Dieter Mayer “Ethers, Aliphatic” dans Ullmann’s Encyclopedia of Industrial Chemistry Wiley-VCH, Weinheim, 2002. doi : 10.1002/14356007.a10_023
- ^ JFW McOmie et DE West (1973). “3,3′-Dihydroxylbiphényle” . Synthèses organiques . ; Volume collectif , vol. 5, p. 412
- ^ FACotton, SADuraj, GLPowell, WJRoth (1986). “Études structurelles comparatives des solvates de tétrahydrofurane de chlorure de métal de transition précoce (III) de première rangée”. Inorg. Chim. Acta . 113 : 81. doi : 10.1016/S0020-1693(00)86863-2 . {{cite journal}}: Maint CS1 : utilise le paramètre auteurs ( lien )
- ^ Frlan, Rok; Kikelj, Danijel (29 juin 2006). “Progrès récents dans la synthèse d’éther diarylique”. Synthèse . 2006 (14): 2271-2285. doi : 10.1055/s-2006-942440 .
- ^ Chisholm, Hugh, éd. (1911). “Ether” . Encyclopædia Britannica . Vol. 9 (11e éd.). La presse de l’Universite de Cambridge. p. 806.
- ^ Claydon; Greeves ; Warren (2001). Chimie organique . Presse universitaire d’Oxford. p. 129 . ISBN 978-0-19-850346-0.
