Le butanol peut être utilisé comme carburant dans un moteur à combustion interne . Il ressemble plus à l’ essence qu’à l’ éthanol . Un hydrocarbure C4, le butanol est un carburant d’appoint et fonctionne donc dans les véhicules conçus pour être utilisés avec de l’essence sans modification. [1] Le n – butanol et l’ isobutanol ont été étudiés comme carburants possibles. Les deux peuvent être produits à partir de la biomasse (comme “biobutanol” [2] [3] [4] ) ainsi qu’à partir de combustibles fossiles (comme “pétrobutanol” [5] ). Les propriétés chimiques dépendent de laisomère ( n -butanol ou isobutanol), pas sur la méthode de production.
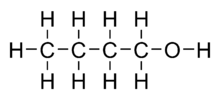 Le butanol, un hydrocarbure C-4, est un biocarburant prometteur, qui partage de nombreuses propriétés avec l’essence.
Le butanol, un hydrocarbure C-4, est un biocarburant prometteur, qui partage de nombreuses propriétés avec l’essence.
Bien qu’intrigant à bien des égards, le carburant butanol est rarement économiquement compétitif.
Bactéries génétiquement modifiées
L’obtention de rendements plus élevés en butanol implique une manipulation des réseaux métaboliques par génie métabolique et génie génétique . [6] [7] Bien que des progrès significatifs aient été réalisés , les voies de fermentation pour la production de butanol restent inefficaces. Le titre et les rendements sont faibles et la séparation est très coûteuse. En tant que telle, la production microbienne de butanol n’est pas compétitive en termes de coûts par rapport au butanol dérivé du pétrole. [8]
Bien qu’elle n’ait pas fait ses preuves sur le plan commercial, la combinaison de méthodes de production électrochimiques et microbiennes peut offrir un moyen de produire du butanol à partir de sources durables . [9]
Escherichia coli
Escherichia coli , ou E. coli , est une bactérie à Gram négatif en forme de bâtonnet . E. coli est le micro-organisme le plus susceptible de passer à la production commerciale d’isobutanol. [10] Dans sa forme machinée E. coli produit les rendements les plus élevés d’isobutanol de n’importe quel micro-organisme. [ citation nécessaire ] Des méthodes telles que l’analyse en mode élémentaire ont été utilisées pour améliorer l’ efficacité métabolique d’ E. coli afin que de plus grandes quantités d’isobutanol puissent être produites. [11] Escherichia coliest un bio-synthétiseur d’isobutanol idéal pour plusieurs raisons :
- E. coli est un organisme pour lequel plusieurs outils de manipulation génétique existent, et c’est un organisme pour lequel il existe une abondante littérature scientifique. [10] Cette richesse de connaissances permet à E. coli d’être facilement modifié par les scientifiques.
- E. coli a la capacité d’utiliser la Lignocellulose (déchets végétaux issus de l’agriculture) dans la synthèse de l’isobutanol. L’utilisation de la Lignocellulose empêche E. coli d’utiliser des matières végétales destinées à la consommation humaine, et empêche toute relation prix aliment-carburant qui résulterait de la biosynthèse de l’isobutanol par E. coli . [dix]
- La modification génétique a été utilisée pour élargir la portée de la Lignocellulose qui peut être utilisée par E. coli . Cela a fait d’ E. coli un biosynthétiseur d’isobutanol utile et diversifié. [12]
Le principal inconvénient d’ E. coli est qu’il est sensible aux bactériophages lorsqu’il est cultivé. Cette susceptibilité pourrait potentiellement arrêter des Bioréacteurs entiers. [10] En outre, la voie de réaction native pour l’isobutanol dans E. coli fonctionne de manière optimale à une concentration limitée d’isobutanol dans la cellule. Pour minimiser la sensibilité d’ E. coli à des concentrations élevées, des mutants des enzymes impliquées dans la synthèse peuvent être générés par mutagenèse aléatoire . Par chance, certains mutants peuvent s’avérer plus tolérants à l’isobutanol ce qui va améliorer le rendement global de la synthèse. [13]
Clostridies
Le n -butanol peut être produit par fermentation de la biomasse par le procédé ABE en utilisant Clostridium acetobutylicum , Clostridium beijerinckii . C. acetobutylicum était autrefois utilisé pour la production d’ acétone à partir d’ amidon . Le butanol était un sous-produit de la fermentation (deux fois plus de butanol était produit). Les matières premières du biobutanol sont les mêmes que celles de l’éthanol : cultures énergétiques comme la betterave à sucre , la canne à sucre , le maïs grain , le blé et le manioc , futures cultures énergétiques non alimentaires comme lele panic raide et même le guayule en Amérique du Nord, ainsi que des sous-produits agricoles tels que la bagasse , la paille et les tiges de maïs . [14] Selon DuPont , les usines de bioéthanol existantes peuvent être adaptées de manière rentable à la production de biobutanol. [15] De plus, la production de butanol à partir de la biomasse et de sous-produits agricoles pourrait être plus efficace (c’est-à-dire la puissance motrice du moteur délivrée par unité d’énergie solaire consommée) que la production d’ éthanol ou de méthanol . [16]
Une souche de Clostridium peut convertir presque toutes les formes de cellulose en butanol même en présence d’oxygène. [17]
Une souche de Clostridium cellulolyticum , un microbe natif dégradant la cellulose, fournit de l’isobutanol directement à partir de la cellulose. [18]
Une combinaison de Succinate et d’éthanol peut être fermentée pour produire du Butyrate (un précurseur du carburant butanol) en utilisant les voies métaboliques présentes dans Clostridium kluyveri . Le Succinate est un intermédiaire du cycle du TCA , qui métabolise le glucose. Les bactéries anaérobies telles que Clostridium acetobutylicum et Clostridium saccharobutylicum contiennent également ces voies. Le Succinate est d’abord activé puis réduit par une réaction en deux étapes pour donner du 4-hydroxybutyrate , qui est ensuite métabolisé en crotonyl-coenzyme A(CoA) . Le crotonyl-CoA est ensuite converti en Butyrate. Les gènes correspondant à ces voies de production de butanol à partir de Clostridium ont été clonés chez E. coli . [19]
Cyanobactéries
Les cyanobactéries sont un phylum de bactéries photosynthétiques . [20] Les cyanobactéries conviennent à la biosynthèse de l’isobutanol lorsqu’elles sont génétiquement modifiées pour produire de l’isobutanol et ses Aldéhydes correspondants . [21] Les espèces de cyanobactéries productrices d’isobutanol offrent plusieurs avantages en tant que synthétiseurs de biocarburants :
- Les cyanobactéries se développent plus rapidement que les plantes [22] et absorbent également la lumière du soleil plus efficacement que les plantes. [23] Cela signifie qu’ils peuvent être reconstitués à un rythme plus rapide que la matière végétale utilisée pour d’autres biosynthétiseurs de biocarburants.
- Les cyanobactéries peuvent être cultivées sur des terres non arables (terres non utilisées pour l’agriculture). [22] Cela empêche la concurrence entre les sources de nourriture et les sources de carburant . [22]
- Les suppléments nécessaires à la croissance des cyanobactéries sont le CO 2 , le H 2 O et la lumière du soleil. [23] Cela présente deux avantages :
- Parce que le CO 2 est dérivé de l’atmosphère, les cyanobactéries n’ont pas besoin de matière végétale pour synthétiser l’isobutanol (dans d’autres organismes qui synthétisent l’isobutanol, la matière végétale est la source du carbone nécessaire pour assembler synthétiquement l’isobutanol). [23] Étant donné que la matière végétale n’est pas utilisée par cette méthode de production d’isobutanol, la nécessité de s’approvisionner en matière végétale à partir de sources alimentaires et de créer une relation prix des aliments et du carburant est évitée. [22]
- Étant donné que le CO 2 est absorbé de l’atmosphère par les cyanobactéries, la possibilité d’une bioremédiation (sous la forme de cyanobactéries éliminant l’excès de CO 2 de l’atmosphère) existe. [23]
Les principaux inconvénients des cyanobactéries sont :
- Les cyanobactéries sont sensibles aux conditions environnementales lorsqu’elles sont cultivées. Les cyanobactéries souffrent beaucoup de la lumière du soleil de longueur d’ onde et d’intensité inappropriées, de CO 2 de concentration inappropriée ou de H 2 O de salinité inappropriée bien qu’une multitude de cyanobactéries soient capables de se développer dans les eaux saumâtres et marines. Ces facteurs sont généralement difficiles à contrôler et constituent un obstacle majeur à la production d’isobutanol par les cyanobactéries. [24]
- Les Bioréacteurs à cyanobactéries nécessitent une énergie élevée pour fonctionner. Les cultures nécessitent un mélange constant et la récolte des produits biosynthétiques est énergivore. Cela réduit l’efficacité de la production d’isobutanol via les cyanobactéries. [24]
Les cyanobactéries peuvent être repensées pour augmenter leur production de butanol, montrant l’importance des forces motrices de l’ATP et du cofacteur en tant que principe de conception dans l’ingénierie des voies. De nombreux organismes ont la capacité de produire du butanol en utilisant une voie dépendante de l’ acétyl-CoA . Le principal problème avec cette voie est la première réaction impliquant la condensation de deux molécules d’acétyl-CoA en acétoacétyl-CoA . Cette réaction est thermodynamiquement défavorable en raison de l’ énergie libre de Gibbs positive qui lui est associée (dG = 6,8 kcal/mol). [25] [26]
Bacillus subtilis
Bacillus subtilis est une bactérie gram-positive en forme de bâtonnet. Bacillus subtilis offre bon nombre des mêmes avantages et inconvénients que E. coli , mais il est moins utilisé et ne produit pas d’isobutanol en quantités aussi importantes que E. coli . [10] Semblable à E. coli , Bacillus subtilis est capable de produire de l’isobutanol à partir de Lignocellulose et est facilement manipulé par des techniques génétiques courantes. [10] L’analyse en mode élémentaire a également été utilisée pour améliorer la voie métabolique de synthèse de l’isobutanol utilisée par Bacillus subtilis, conduisant à des rendements plus élevés d’isobutanol étant produits. [27]
Saccharomyces cerevisiae
Saccharomyces cerevisiae , ou S. cerevisiae , est une espèce de levure . S. cerevisiae produit naturellement de l’isobutanol en petites quantités via savoie de biosynthèse de la valine . [28] S. cerevisiae est un candidat idéal pour la production de biocarburant à base d’isobutanol pour plusieurs raisons :
- S. cerevisiae peut être cultivé à des niveaux de pH bas , aidant à prévenir la contamination pendant la croissance dans les Bioréacteurs industriels. [dix]
- S. cerevisiae ne peut pas être affecté par les bactériophages car c’est un eucaryote . [dix]
- Des connaissances scientifiques approfondies sur S. cerevisiae et sa biologie existent déjà. [dix]
La Surexpression des enzymes dans la voie de biosynthèse de la valine de S. cerevisiae a été utilisée pour améliorer les rendements en isobutanol. [28] [29] [30] S. cerevisiae , cependant, s’est avéré difficile à travailler en raison de sa biologie inhérente :
- En tant qu’eucaryote, S. cerevisiae est génétiquement plus complexe que E. coli ou B. subtilis et est donc plus difficile à manipuler génétiquement. [dix]
- S. cerevisiae a la capacité naturelle de produire de l’éthanol . Cette capacité naturelle peut « écraser » et par conséquent inhiber la production d’isobutanol par S. cerevisiae . [dix]
- S. cerevisiae ne peut pas utiliser cinq sucres carbonés pour produire de l’isobutanol. L’incapacité d’utiliser des sucres à cinq carbones empêche S. cerevisiae d’utiliser la Lignocellulose et signifie que S. cerevisiae doit utiliser des matières végétales destinées à la consommation humaine pour produire de l’isobutanol. Il en résulte une relation prix alimentaire/carburant défavorable lorsque l’isobutanol est produit par S. cerevisiae . [dix]
Ralstonia eutrophe
Ralstonia eutropha est une bactérie gram-négative du sol de la classe des bêta -protéobactéries . Ralstonia eutropha est capable de convertir l’énergie électrique en isobutanol. Cette conversion se fait en plusieurs étapes :
- Les anodes sont placées dans un mélange de H 2 O et CO 2 .
- Un courant électrique traverse les anodes et, par un processus électrochimique , H 2 O et CO 2 sont combinés pour synthétiser l’acide formique .
- Une culture de Ralstonia eutropha (constituée d’une souche tolérante à l’électricité) est maintenue au sein du mélange H 2 O et CO 2 .
- La culture de Ralstonia eutropha transforme ensuite l’acide formique du mélange en isobutanol.
- L’isobutanol biosynthétisé est ensuite séparé du mélange et peut être utilisé comme biocarburant.
Matières premières
Le coût élevé des matières premières est considéré comme l’un des principaux obstacles à la production commerciale de butanols. L’utilisation de matières premières peu coûteuses et abondantes, par exemple des tiges de maïs , peut améliorer la viabilité économique du procédé. [31]
L’ingénierie métabolique peut être utilisée pour permettre à un organisme d’utiliser un substrat moins cher tel que le glycérol au lieu du glucose . Étant donné que les processus de fermentation nécessitent du glucose dérivé des aliments, la production de butanol peut avoir un impact négatif sur l’approvisionnement alimentaire (voir le débat entre aliments et carburant ). Le glycérol est une bonne source alternative pour la production de butanol . Alors que les sources de glucose sont précieuses et limitées, le glycérol est abondant et a un faible prix sur le marché car il s’agit d’un déchet de la production de biodiesel . La production de butanol à partir de glycérol est économiquement viable en utilisant les voies métaboliques qui existent dansBactérie Clostridium pasteurianum . [32]
Améliorer l’efficacité
Un processus appelé séparation du point de trouble pourrait permettre la récupération du butanol avec une grande efficacité. [33]
Producteurs et distribution
DuPont et BP prévoient de faire du biobutanol le premier produit de leur effort commun pour développer, produire et commercialiser des biocarburants de nouvelle génération. [34] En Europe, la société suisse Butalco [35] développe des levures génétiquement modifiées pour la production de biobutanol à partir de matériaux cellulosiques. Gourmet Butanol, une entreprise basée aux États-Unis, développe un procédé qui utilise des champignons pour convertir les déchets organiques en biobutanol. [36] [37] Celtic Renewables fabrique du biobutanol à partir de déchets résultant de la production de whisky et de pommes de terre de qualité inférieure .
Propriétés des combustibles courants
Isobutanol
L’isobutanol est un biocarburant de deuxième génération avec plusieurs qualités qui résolvent les problèmes posés par l’éthanol. [dix]
Les propriétés de l’isobutanol en font un biocarburant attractif :
- densité énergétique relativement élevée , 98% de celle de l’essence. [38]
- n’absorbe pas facilement l’eau de l’air, empêchant la corrosion des moteurs et des pipelines. [dix]
- peut être mélangé à n’importe quelle proportion avec de l’essence [39] , ce qui signifie que le carburant peut « tomber dans » l’infrastructure pétrolière existante en tant que Carburant de remplacement ou additif majeur. [dix]
- peuvent être produits à partir de matières végétales non liées à l’approvisionnement alimentaire, ce qui empêche une relation prix du carburant/prix des denrées alimentaires. [10] [11] [12] [27]
- en supposant qu’il est produit à partir de matières premières lignocellulosiques résiduelles , le mélange d’isobutanol avec de l’essence peut réduire considérablement les émissions de GES . [40]
n-Butanol
Le butanol tolère mieux la contamination par l’eau et est moins corrosif que l’éthanol et plus adapté à la distribution par les pipelines existants pour l’essence. [15] Dans les mélanges avec du diesel ou de l’essence, le butanol est moins susceptible de se séparer de ce carburant que l’éthanol si le carburant est contaminé par de l’eau. [15] Il existe également une synergie de co-mélange de pression de vapeur avec du butanol et de l’essence contenant de l’éthanol, ce qui facilite le mélange d’éthanol. Cela facilite le stockage et la distribution des carburants mélangés. [15] [41] [42]
| Le carburant | Densité énergétique | Rapport air-carburant | Énergie spécifique | Chaleur de vaporisation |
RON | LUN | AKI |
|---|---|---|---|---|---|---|---|
| Essence et bioessence | 32 MJ/L | 14.7 | 2,9 MJ/kg d’air | 0,36 MJ/kg | 91–99 | 81–89 | 87-95 |
| Carburant au butanol | 29,2 MJ/L | 11.1 | 3,6 MJ/kg d’air | 0,43 MJ/kg | 96 | 78 | 87 |
| Carburant éthanol anhydre | 19,6 MJ/L | 9.0 | 3,0 MJ/kg d’air | 0,92 MJ/kg | 107 | 89 | |
| Carburant au méthanol | 16 MJ/L | 6.4 | 3,1 MJ/kg d’air | 1,2 MJ/kg | 106 | 92 |
L’ indice d’octane du n-butanol est similaire à celui de l’essence mais inférieur à celui de l’éthanol et du méthanol. Le n-butanol a un RON ( indice d’ octane de recherche ) de 96 et un MON ( indice d’ octane moteur ) de 78 (avec un résultat “(R+M)/2 indice d’octane de la pompe” de 87, tel qu’utilisé en Amérique du Nord) tandis que t -le butanol a des indices d’octane de 105 RON et 89 MON. [44] Le t-butanol est utilisé comme additif dans l’essence mais ne peut pas être utilisé comme carburant sous sa forme pure car son point de fusion relativement élevé de 25,5 ° C (79 ° F) le fait gélifier et se solidifier près de la température ambiante. En revanche, l’ isobutanola un point de fusion inférieur à celui du n-butanol et un RON favorable de 113 et un MON de 94, et est donc bien mieux adapté aux mélanges d’essence à fraction élevée, aux mélanges avec du n-butanol ou comme carburant autonome. [45]
Un carburant avec un indice d’octane plus élevé est moins sujet au cliquetis (combustion extrêmement rapide et spontanée par compression) et le système de contrôle de tout moteur de voiture moderne peut en tirer parti en ajustant le calage de l’allumage. Cela améliorera l’efficacité énergétique, conduisant à une meilleure économie de carburant que ne l’indiquent les comparaisons du contenu énergétique de différents carburants. En augmentant le taux de compression, des gains supplémentaires en termes d’économie de carburant, de puissance et de couple peuvent être obtenus. À l’inverse, un carburant avec un indice d’octane inférieur est plus susceptible de cogner et réduira l’efficacité. Le cognement peut également endommager le moteur. Les moteurs conçus pour fonctionner avec un indice d’octane de 87 n’auront aucune économie de puissance/carburant supplémentaire s’ils fonctionnent avec un carburant à indice d’octane plus élevé.
Caractéristiques du butanol : rapport air-carburant, énergie spécifique, viscosité, chaleur spécifique
Les carburants à base d’alcool, y compris le butanol et l’éthanol, sont partiellement oxydés et doivent donc fonctionner avec des mélanges plus riches que l’essence. Les moteurs à essence standard des voitures peuvent ajuster le rapport air-carburant pour s’adapter aux variations du carburant, mais seulement dans certaines limites selon le modèle. Si la limite est dépassée en faisant fonctionner le moteur avec de l’éthanol pur ou un mélange d’essence avec un pourcentage élevé d’éthanol, le moteur tournera pauvrement, ce qui peut endommager gravement les composants. Comparé à l’éthanol, le butanol peut être mélangé dans des proportions plus élevées avec de l’essence pour être utilisé dans les voitures existantes sans qu’il soit nécessaire de le moderniser, car le rapport air-carburant et la teneur en énergie sont plus proches de ceux de l’essence. [41] [42]
Les carburants à base d’alcool ont moins d’énergie par unité de poids et de volume que l’essence. Pour permettre de comparer l’énergie nette libérée par cycle, une mesure appelée énergie spécifique des carburants est parfois utilisée. Il est défini comme l’énergie libérée par rapport air-carburant. L’énergie nette libérée par cycle est plus élevée pour le butanol que pour l’éthanol ou le méthanol et environ 10 % plus élevée que pour l’essence. [46]
| Substance | Viscosité cinématique à 20 °C |
|---|---|
| Butanol | 3,64 cst |
| Diesel | >3cSt |
| Éthanol | 1,52 cst |
| Eau | 1,0 cSt |
| Méthanol | 0,64 cSt |
| De l’essence | 0,4–0,8 cSt |
La viscosité des alcools augmente avec des chaînes carbonées plus longues. Pour cette raison, le butanol est utilisé comme alternative aux alcools plus courts lorsqu’un solvant plus visqueux est souhaité. La viscosité cinématique du butanol est plusieurs fois supérieure à celle de l’essence et à peu près aussi visqueuse que le carburant diesel de haute qualité. [47]
Le carburant d’un moteur doit être vaporisé avant de brûler. La vaporisation insuffisante est un problème connu avec les carburants à base d’alcool lors des démarrages à froid par temps froid. Comme la chaleur de vaporisation du butanol est inférieure à la moitié de celle de l’éthanol, un moteur fonctionnant au butanol devrait être plus facile à démarrer par temps froid qu’un moteur fonctionnant à l’éthanol ou au méthanol. [41]
Mélanges butanol-carburant
Des normes pour le mélange d’éthanol et de méthanol dans l’essence existent dans de nombreux pays, dont l’UE, les États-Unis et le Brésil. Des mélanges de butanol équivalents approximatifs peuvent être calculés à partir des relations entre le rapport carburant-air stoechiométrique du butanol, de l’éthanol et de l’essence. Les mélanges de carburant à l’éthanol courants pour le carburant vendu comme essence varient actuellement de 5% à 10%. On estime qu’environ 9,5 gigalitres (Gl) d’essence peuvent être économisés et qu’environ 64,6 Gl de mélange butanol-essence à 16 % (Bu16) peuvent potentiellement être produits à partir de résidus de maïs aux États-Unis, ce qui équivaut à 11,8 % de l’essence domestique totale. consommation. [31]
L’acceptation par les consommateurs peut être limitée en raison de l’ odeur de banane potentiellement désagréable du n-butanol. [48] Des plans sont en cours pour commercialiser un carburant composé à 85 % d’éthanol et à 15 % de butanol (E85B), afin que les moteurs à combustion interne E85 existants puissent fonctionner avec un carburant 100 % renouvelable qui pourrait être fabriqué sans utiliser de combustibles fossiles. Parce que sa chaîne d’hydrocarbures plus longue le rend assez non polaire , il ressemble plus à l’essence qu’à l’éthanol. Il a été démontré que le butanol fonctionne dans les véhicules conçus pour être utilisés avec de l’essence sans modification.
Butanol dans les véhicules
Actuellement, aucun véhicule de production n’est connu pour être approuvé par le fabricant pour une utilisation avec du butanol à 100 %. Au début de 2009, seuls quelques véhicules sont approuvés même pour l’utilisation de carburant E85 (c’est-à-dire 85 % d’éthanol + 15 % d’essence) aux États-Unis. Cependant, au Brésil, tous les constructeurs automobiles (Fiat, Ford, VW, GM, Toyota, Honda, Peugeot, Citroën et autres) produisent des véhicules “flex-fuel” qui peuvent fonctionner à 100 % d’essence et/ou tout mélange d’éthanol et d’essence jusqu’à 85% d’éthanol (E85). Ces voitures flex fuel représentent 90 % des ventes de véhicules personnels au Brésil, en 2009. BP et Dupont, engagés dans une joint-venture pour produire et promouvoir le carburant butanol, affirment [49] que « le biobutanol peut être mélangé jusqu’à 10 %v /v dans l’essence européenne et 11,5 % v/v dans l’essence américaine”. [50] [51] Dans leLors de la course Petit Le Mans 2009 , la Lola B09/86 – Mazda MZR-R n°16 de Dyson Racing a couru avec un mélange de biobutanol et d’éthanol développé par le partenaire technologique de l’équipe BP .
Voir également
-

 Portail de l’énergie
Portail de l’énergie -

 Portail des énergies renouvelables
Portail des énergies renouvelables
- De l’alcool au carburéacteur
- Rapport air-carburant
- Bioalcool
- Biocarburant
- Biodiesel
- Biohydrogène
- Bioconversion de la biomasse en carburants à base d’alcool mixte
- Butanol
- Catalyseur
- Éther diméthylique
- Distillation
- Normes d’émission
- Culture énergétique
- Carburant éthanol
- Installation de fermentation
- Acide formique : peut être utilisé comme intermédiaire pour produire de l’isobutanol à partir de CO 2 à l’aide de microbes [52] [53] [54]
- Biocarburants Gevo
- Liste des huiles végétales utilisées pour le biocarburant
Références
- ^ “ButylFuel, LLC” . Récupéré le 29/01/2008 .
- ^ Sampa Maiti; et coll. (10 décembre 2015). “Quête d’une bio‐production durable et valorisation du butanol comme solution prometteuse aux énergies fossiles”. Recherche énergétique . 40 (4): 411–438. doi : 10.1002/er.3458 .
- ^ Centre de données sur les carburants alternatifs et les véhicules avancés: Biobutanol
- ^ “Copie archivée” . Archivé de l’original le 2008-10-25 . Récupéré le 27/10/2008 . {{cite web}}: CS1 maint: archived copy as title (link)
- ^ Atsumi, Shota; Hanai, Taizo ; Liao, James C. (2008), “Voies non fermentatives pour la synthèse d’alcools supérieurs à chaîne ramifiée comme biocarburants”, Nature , 451 (7174): 86–89, Bibcode : 2008Natur.451…86A , doi : 10.1038 /nature06450 , PMID 18172501 , S2CID 4413113
- ^ Berezina OV, Zakharova NV, Yarotsky SV, Zverlov VV Producteurs microbiens de butanol. Biochimie et microbiologie appliquées 48 , Numéro : 7 Pages : 625–638 Publié : DEC 2012
- ^ Le Korea Advanced Institute of Science and Technology (KAIST), via EurekAlert!, un service de l’AAAS. (23 octobre 2012). “Production hautement efficace de biocarburants avancés par des micro-organismes métaboliquement modifiés” . {{cite web}}: CS1 maint: uses authors parameter (link)
- ^ Veettil, SI, Kumar, L., Koukoulas, AA (2016). “Les biocarburants avancés d’origine microbienne peuvent-ils jamais rivaliser avec le bioéthanol conventionnel? Un examen critique”. Bioressources . 11 (4): 10711–10755. doi : 10.15376/biores.11.4.Veettil . {{cite journal}}: CS1 maint: multiple names: authors list (link)
- ^ Li, H.; Opgenorth, PH; Wernick, DG ; Rogers, S.; Wu, T.-Y. ; Higashide, W.; Malati, P.; Huo, Y.-X. ; Cho, KM ; Liao, JC (29 mars 2012). “Conversion électromicrobienne intégrée du CO2 en alcools supérieurs”. Sciences . 335 (6076): 1596. Bibcode : 2012Sci…335.1596L . doi : 10.1126/science.1217643 . PMID 22461604 . S2CID 24328552 .
- ^ un bcd e f g h i j k l m n o p Peralta -Yahya, Pamela P .; Zhang, Fuzhong; del Cardayre, Stephen B.; Keasling, Jay D.; Del Cardayre, Stephen B.; Keasling, Jay D. (15 août 2012). “Ingénierie microbienne pour la production de biocarburants avancés”. Nature . 488 (7411): 320–328. Bibcode : 2012Natur.488..320P . doi : 10.1038/nature11478 . PMID 22895337 . S2CID 4423203 . {{cite journal}}: CS1 maint: multiple names: authors list (link)
- ^ un b Trinh, Cong T. (9 juin 2012). “Élucider et reprogrammer les métabolismes d’ Escherichia coli pour la production anaérobie obligatoire de n-butanol et d’isobutanol”. Microbiologie appliquée et biotechnologie . 95 (4): 1083–1094. doi : 10.1007/s00253-012-4197-7 . PMID 22678028 . S2CID 10586770 .
- ^ un b Nakashima, Nobutaka; Tamura, Tomohiro (1er juillet 2012). “Une nouvelle mutation de répression des catabolites de carbone d’ Escherichia coli , mlc∗, et son utilisation pour produire de l’isobutanol”. Journal des biosciences et de la bioingénierie . 114 (1): 38–44. doi : 10.1016/j.jbiosc.2012.02.029 . PMID 22561880 .
- ^ Chong, Huiqing; Geng, Hefang ; Zhang, Hongfang ; Chanson, Hao ; Huang, Lei ; Jiang, Rongrong (2013-11-06). “Améliorer la tolérance à l’isobutanol d’ E. coli grâce à l’ingénierie de sa protéine réceptrice d’AMPc de facteur de transcription global (CRP)”. Biotechnologie et Bioingénierie . 111 (4): 700–708. doi : 10.1002/bit.25134 . ISSN 0006-3592 . PMID 24203355 . S2CID 28120139 .
- ^ Ars | Demande de publication : Production de butanol à partir de la biomasse agricole
- ^ un bcd Fiche d’ information BP DuPont Biobutanol (PDF) .
- ^ https://www.sciencedaily.com/releases/2008/01/080123153142.htm Le butanol une alternative énergétique ?
- ^ “Une nouvelle bactérie produit du butanol directement à partir de cellulose” . Greencarcongress.com. 28 août 2011 . Consulté le 17 novembre 2012 .
- ^ Higashide, Wendy; Li, Yong Chao ; Yang, Yunfeng; Liao, James C. (2011-04-15). “Ingénierie métabolique de Clostridium cellulolyticum pour la production d’isobutanol à partir de cellulose” . Microbiologie appliquée et environnementale . 77 (8): 2727–2733. doi : 10.1128/AEM.02454-10 . ISSN 0099-2240 . PMC 3126361 . PMID 21378054 .
- ^ Sohling, B., & Gottschalk G. (1996). “Analyse moléculaire de la voie de dégradation anaérobie du Succinate dans Clostridium kluyveri ” . Journal de bactériologie . 178 (3): 871–880. doi : 10.1128/jb.178.3.871-880.1996 . PMC 177737 . PMID 8550525 . {{cite journal}}: CS1 maint: uses authors parameter (link)
- ^ Cyanobactéries
- ^ Atsumi, Shota; Higashide, Wendy ; Liao, James C (décembre 2009). “Recyclage Photosynthétique direct du dioxyde de carbone en isobutyraldéhyde”. Biotechnologie naturelle . 27 (12): 1177-1180. doi : 10.1038/nbt.1586 . PMID 19915552 . S2CID 1492698 .
- ^ un bcd Machado , député Iara ; Atsumi, Shota (1er novembre 2012). “Production de biocarburants cyanobactériens”. Journal de biotechnologie . 162 (1): 50–56. doi : 10.1016/j.jbiotec.2012.03.005 . PMID 22446641 .
- ^ un bcd Varman , AM ; Xiao, Y.; Pakrasi, HB; Tang, YJ (26 novembre 2012). “Ingénierie métabolique de Synechocystis sp. Souche PCC 6803 pour la production d’isobutanol” . Microbiologie appliquée et environnementale . 79 (3): 908–914. doi : 10.1128/AEM.02827-12 . PMC 3568544 . PMID 23183979 .
- ^ un b Singh, Nirbhay Kumar; Dhar, Dolly Wattal (11 mars 2011). “Les microalgues comme biocarburant de deuxième génération. Une revue” (PDF) . Agronomie pour le développement durable . 31 (4): 605–629. doi : 10.1007/s13593-011-0018-0 . S2CID 38589348 .
- ^ Stern JR, Coon MJ, Delcampillo A (1953). “Acetoacetyl coenzyme-a comme intermédiaire dans la décomposition enzymatique et la synthèse de l’acétoacétate”. J Am Chem Soc . 75 (6): 1517-1518. doi : 10.1021/ja01102a540 .
- ^ Lan, EI; Liao, JC (2012). “L’ATP entraîne la production Photosynthétique directe de 1-butanol dans les cyanobactéries” . Actes de l’Académie nationale des sciences des États-Unis d’Amérique . 109 (16): 6018–6023. Bibcode : 2012PNAS..109.6018L . doi : 10.1073/pnas.1200074109 . PMC 3341080 . PMID 22474341 .
- ^ un b Li, Shanshan; Huang, Di; Li, Yong ; Wen, Jianping; Jia, Xiaoqiang (1er janvier 2012). “Amélioration rationnelle du Bacillus subtilis produisant de l’isobutanol d’ingénierie par analyse en mode élémentaire” . Usines de cellules microbiennes . 11 (1): 101. doi : 10.1186/1475-2859-11-101 . PMC 3475101 . PMID 22862776 .
- ^ un b Kondo, Takashi; Tezuka, Hironori ; Ishii, juin ; Matsuda, Fumio ; Ogino, Chiaki ; Kondo, Akihiko (1er mai 2012). “Génie génétique pour améliorer la voie d’Ehrlich et modifier le flux de carbone pour une production accrue d’isobutanol à partir de glucose par Saccharomyces cerevisiae”. Journal de biotechnologie . 159 (1–2) : 32–37. doi : 10.1016/j.jbiotec.2012.01.022 . PMID 22342368 .
- ^ MATSUDA, Fumio; KONDO, Takashi ; IDA, Kengo ; TEZUKA, Hironori ; ISHII, juin ; KONDO, Akihiko (1er janvier 2012). “Construction d’une voie artificielle pour la biosynthèse de l’isobutanol dans le cytosol de Saccharomyces cerevisiae”. Bioscience, biotechnologie et biochimie . 76 (11): 2139–2141. doi : 10.1271/bbb.120420 . PMID 23132567 . S2CID 21726896 .
- ^ Lee, Won Heong; Seo, Seung-Oh; Bae, Yi-Hyun ; Nan, Hong ; Jin, Yong-Su; Seo, Jin-Ho (28 avril 2012). “Production d’isobutanol dans Saccharomyces cerevisiae modifié par Surexpression de la 2-cétoisovalérate décarboxylase et des enzymes biosynthétiques de la valine”. Génie des bioprocédés et des biosystèmes . 35 (9): 1467-1475. doi : 10.1007/s00449-012-0736-y . PMID 22543927 . S2CID 25012774 .
- ^ un b Karimi Alavijeh, Masih; Karimi, Keikhosro (mars 2019). “Production de biobutanol à partir de tiges de maïs aux États-Unis”. Cultures et produits industriels . 129 : 641–653. doi : 10.1016/j.indcrop.2018.12.054 . ISSN 0926-6690 .
- ^ Malaviya, A.; Jang, Y.; & Lee, SY (2012). “Production continue de butanol avec formation réduite de sous-produits à partir de glycérol par un mutant hyper producteur de Clostridium pasteurianum “. Appl Microbiol Biotechnol . 93 (4): 1485–1494. doi : 10.1007/s00253-011-3629-0 . PMID 22052388 . S2CID 1597829 .
- ^ Collège des sciences de l’agriculture, de la consommation et de l’environnement de l’Université de l’Illinois (14 août 2012). “Le nouveau procédé double la production de carburant alternatif tout en réduisant les coûts” . {{cite web}}: CS1 maint: uses authors parameter (link)
- ^ DuPont et BP divulguent un partenariat avancé sur les biocarburants ciblant plusieurs molécules de butanol
- ^ Accueil
- ^ “Butanol gastronomique” . Archivé de l’original le 2019-09-02 . Récupéré le 09/07/2020 .
- ^ Un collège du Maine remporte une subvention de l’EPA pour la recherche sur les déchets alimentaires en carburant | Biomassmagazine.com
- ^ Lu, Jingnan; Brigham, Christopher J.; Gai, Claudia S.; Sinskey, Anthony J. (4 août 2012). « Études sur la production d’alcools à chaîne ramifiée dans l’ingénierie Ralstonia eutropha » (PDF) . Microbiologie appliquée et biotechnologie . 96 (1): 283–297. doi : 10.1007/s00253-012-4320-9 . hdl : 1721.1/75742 . PMID 22864971 . S2CID 62337 .
- ^ Ting, Cindy Ng Wei; Wu, Jinchuan; Takahashi, Katsuyuki; Endo, Ayako ; Zhao, Hua (8 septembre 2012). “Dépisté Butanol-Tolerant Enterococcus faecium Capable de Production de Butanol”. Biochimie appliquée et biotechnologie . 168 (6): 1672–1680. doi : 10.1007/s12010-012-9888-0 . PMID 22961352 . S2CID 9201136 .
- ^ Wojcieszyk, Michał; Knuutila, Lotta ; Kroyan, Yuri ; de Pinto Balsemão, Mario ; Tripathi, Rupali ; Keskivali, Juha ; Karvo, Anna; Santasalo-Aarnio, Annukka ; Blomstedt, Otto; Larmi, Martti (janvier 2021). “Performance de l’anisole et de l’isobutanol en tant que bio-mélanges d’essence pour les moteurs à allumage commandé” . Durabilité . 13 (16) : 8729. doi : 10.3390/su13168729 .
- ^ un bcJL Smith ; JP Workman (20 décembre 2007). “Alcool pour les carburants moteurs” . Université d’État du Colorado . Archivé de l’original le 2011-08-21 . Récupéré le 29/01/2008 .
- ^ un b Randall Chase (2006-06-23). “DuPont, BP s’associent pour fabriquer du butanol ; ils disent qu’il surpasse l’éthanol en tant qu’additif pour carburant” . Presse associée . Récupéré le 29/01/2008 .
- ^ Moteurs à combustion interne, Edward F. Obert, 1973
- ^ UNEP.org-Propriétés des composés oxygénés (PDF) .
- ^ iea-amf.org-Advanced Motor Fuels: Butanol Properties (HTML).
- ^ Carburant butanol – Biocarburants, Bio-énergie – Oilgae – Huile d’algues
- ^ Boîte à outils d’ingénierie
- ^ “Sécurité des produits – n-Butanol” . dow.com . Dow Chemical Company. Archivé de l’original le 2 avril 2015 . Consulté le 9 juillet 2013 .
- ^ “Copie archivée” (PDF) . Archivé de l’original (PDF) le 2009-01-21 . Récupéré le 13/05/2009 . {{cite web}}: CS1 maint: archived copy as title (link)
- ^ “Copie archivée” (PDF) . Archivé de l’original (PDF) le 2012-02-29 . Récupéré le 25/07/2013 . {{cite web}}: CS1 maint: archived copy as title (link)
- ^ “Améliorer la biomasse en … butanol?” . Congrès de la voiture verte. 20 juillet 2005 . Récupéré le 29/01/2008 .
- ^ Extraire l’énergie de l’air – est-ce l’avenir du carburant ?
- ^ Les chercheurs de l’UCLA utilisent l’électricité et le CO2 pour fabriquer du butanol
- ^ Conversion électromicrobienne intégrée du CO2 en alcools supérieurs
Liens externes
- Biobutanol ( EERE ).
- Actualités de la recherche sur le biobutanol du Green Car Congress
- Vue 3D du butanol et fichier pdb