Alliage
Un alliage est un mélange d’ éléments chimiques dont au moins un est un métal . Contrairement aux composés chimiques à base métallique, un alliage conservera toutes les propriétés d’un métal dans le matériau résultant, telles que la Conductivité électrique , la ductilité , l’ opacité et le lustre ., mais peuvent avoir des propriétés différentes de celles des métaux purs, telles qu’une résistance ou une dureté accrue. Dans certains cas, un alliage peut réduire le coût global du matériau tout en préservant des propriétés importantes. Dans d’autres cas, le mélange confère des propriétés synergiques aux éléments métalliques constitutifs telles que la résistance à la corrosion ou la résistance mécanique.
 De gauche à droite : trois alliages ( cuivre au béryllium , inconel , acier ) et trois métaux purs ( titane , aluminium , magnésium )
De gauche à droite : trois alliages ( cuivre au béryllium , inconel , acier ) et trois métaux purs ( titane , aluminium , magnésium )
Les alliages sont définis par un caractère de liaison métallique . [1] Les constituants de l’alliage sont généralement mesurés en pourcentage de masse pour les applications pratiques et en fraction atomique pour les études scientifiques fondamentales. Les alliages sont généralement classés comme alliages de substitution ou interstitiels , selon l’arrangement atomique qui forme l’alliage. Ils peuvent en outre être classés comme homogènes (constitués d’une seule phase), hétérogènes (constitués de deux phases ou plus) ou intermétalliques . Un alliage peut être une solution solide d’éléments métalliques (une seule phase, où tous les grains métalliques (cristaux) sont de la même composition) ou un mélangede phases métalliques (deux solutions ou plus, formant une microstructure de cristaux différents au sein du métal).
Des exemples d’alliages comprennent l’Or rouge ( or et cuivre ) , l’or blanc (or et argent ), l’argent sterling (argent et cuivre), l’acier ou l’ Acier au silicium ( fer avec carbone non métallique ou silicium respectivement), la soudure , le laiton , l’ étain , le duralumin , bronze et amalgames .
Les alliages sont utilisés dans une grande variété d’applications, des alliages d’acier, utilisés dans tout, des bâtiments aux automobiles en passant par les outils chirurgicaux, aux alliages de titane exotiques utilisés dans l’industrie aérospatiale, aux alliages béryllium-cuivre pour les outils anti-étincelles.
Les caractéristiques

 Bronze liquide , coulé dans des moules lors de la coulée
Bronze liquide , coulé dans des moules lors de la coulée
Un alliage est un mélange d’ éléments chimiques , qui forme une substance impure (mélange) qui conserve les caractéristiques d’un métal . Un alliage est distinct d’un métal impur en ce que, avec un alliage, les éléments ajoutés sont bien contrôlés pour produire des propriétés souhaitables, tandis que les métaux impurs tels que le fer forgé sont moins contrôlés, mais sont souvent considérés comme utiles. Les alliages sont fabriqués en mélangeant deux éléments ou plus, dont au moins un est un métal. Celui-ci est généralement appelé le métal primaire ou le métal de base, et le nom de ce métal peut également être le nom de l’alliage. Les autres constituants peuvent ou non être des métaux mais, lorsqu’ils sont mélangés à la base fondue, ils seront solubleset dissoudre dans le mélange. Les propriétés mécaniques des alliages seront souvent très différentes de celles de ses constituants individuels. Un métal normalement très mou ( malléable ), comme l’ aluminium , peut être altéré en l’alliant à un autre métal mou, comme le cuivre . Bien que les deux métaux soient très doux et ductiles , l’ alliage d’aluminium résultant aura une résistance beaucoup plus grande . L’ajout d’une petite quantité de carbone non métallique au fer échange sa grande ductilité contre la plus grande résistance d’un alliage appelé acier . En raison de sa très haute résistance, mais toujours d’une ténacité substantielle, et sa capacité à être fortement altérée par le Traitement thermique , l’acier est l’un des alliages les plus utiles et les plus courants d’utilisation moderne. En ajoutant du chrome à l’acier, sa résistance à la corrosion peut être améliorée, créant de l’acier inoxydable , tandis que l’ajout de silicium modifiera ses caractéristiques électriques, produisant de l’Acier au silicium .


Comme l’huile et l’eau, un métal en fusion ne se mélange pas toujours avec un autre élément. Par exemple, le fer pur est presque totalement Insoluble avec le cuivre. Même lorsque les constituants sont solubles, chacun aura généralement un point de saturation , au-delà duquel aucun autre constituant ne peut être ajouté. Le fer, par exemple, peut contenir un maximum de 6,67 % de carbone. Bien que les éléments d’un alliage doivent généralement être solubles à l’ état liquide , ils peuvent ne pas toujours être solubles à l’ état solide . Si les métaux restent solubles lorsqu’ils sont solides, l’alliage forme une solution solide , devenant une structure homogène constituée de cristaux identiques, appelée phase. Si, à mesure que le mélange refroidit, les constituants deviennent insolubles, ils peuvent se séparer pour former deux ou plusieurs types de cristaux différents, créant une microstructure hétérogène de différentes phases, certaines avec plus d’un constituant que l’autre. Cependant, dans d’autres alliages, les éléments insolubles peuvent ne se séparer qu’après la cristallisation. S’ils sont refroidis très rapidement, ils cristallisent d’abord en une phase homogène, mais ils sont sursaturés avec les constituants secondaires. Au fil du temps, les atomes de ces alliages sursaturés peuvent se séparer du réseau cristallin, devenir plus stables et former une seconde phase qui sert à renforcer les cristaux à l’intérieur.


Certains alliages, tels que l’ électrum – un alliage d’ argent et d’or – se produisent naturellement. Les météorites sont parfois constituées d’alliages naturels de fer et de nickel , mais ne sont pas originaires de la Terre. L’un des premiers alliages fabriqués par l’homme était le bronze , qui est un mélange d’ étain et de cuivre . Le bronze était un alliage extrêmement utile pour les anciens, car il est beaucoup plus solide et plus dur que l’un ou l’autre de ses composants. L’acier était un autre alliage commun. Cependant, dans les temps anciens, il ne pouvait être créé que comme sous-produit accidentel du chauffage du minerai de fer dans les incendies ( fusion ) lors de la fabrication du fer. D’autres alliages anciens comprennentétain , laiton et fonte . À l’ère moderne, l’acier peut être créé sous de nombreuses formes. L’acier au carbone peut être fabriqué en faisant varier uniquement la teneur en carbone, produisant des alliages doux comme l’Acier doux ou des alliages durs comme l’acier à ressort . Les aciers alliés peuvent être fabriqués en ajoutant d’autres éléments, tels que le chrome , le molybdène , le vanadium ou le nickel , ce qui donne des alliages tels que l’acier rapide ou l’acier à outils . Petites quantités de manganèsesont généralement alliés à la plupart des aciers modernes en raison de leur capacité à éliminer les impuretés indésirables, telles que le phosphore , le soufre et l’oxygène , qui peuvent avoir des effets néfastes sur l’alliage. Cependant, la plupart des alliages n’ont été créés que dans les années 1900, comme divers alliages d’aluminium, de titane , de nickel et de magnésium . Certains superalliages modernes , tels que l’ incoloy , l’ inconel et l’Hastelloy , peuvent être constitués d’une multitude d’éléments différents.
Un alliage est techniquement un métal impur, mais lorsqu’il s’agit d’alliages, le terme impuretés désigne généralement des éléments indésirables. De telles impuretés sont introduites à partir des métaux de base et des éléments d’alliage, mais sont éliminées pendant le traitement. Par exemple, le soufre est une impureté courante dans l’acier. Le soufre se combine facilement avec le fer pour former du sulfure de fer , qui est très cassant, créant des points faibles dans l’acier. [2] Le lithium , le sodium et le calcium sont des impuretés courantes dans les alliages d’aluminium, qui peuvent avoir des effets néfastes sur l’ intégrité structurellede moulages. Inversement, les métaux autrement purs qui contiennent simplement des impuretés indésirables sont souvent appelés “métaux impurs” et ne sont généralement pas appelés alliages. L’oxygène, présent dans l’air, se combine facilement avec la plupart des métaux pour former des oxydes métalliques ; en particulier à des températures plus élevées rencontrées lors de l’alliage. Un grand soin est souvent pris pendant le processus d’alliage pour éliminer les impuretés en excès, en utilisant des fondants , des additifs chimiques ou d’autres méthodes de métallurgie extractive . [3]
La théorie
L’alliage d’un métal se fait en le combinant avec un ou plusieurs autres éléments. Le processus d’alliage le plus courant et le plus ancien est réalisé en chauffant le métal de base au-delà de son point de fusion , puis en dissolvant les solutés dans le liquide fondu, ce qui peut être possible même si le point de fusion du soluté est bien supérieur à celui de la base. Par exemple, à l’état liquide, le titane est un solvant très puissant capable de dissoudre la plupart des métaux et éléments. De plus, il absorbe facilement des gaz comme l’oxygène et brûle en présence d’azote. Cela augmente le risque de contamination de toute surface de contact et doit donc être fondu dans un chauffage par induction sous vide et des creusets spéciaux en cuivre refroidis à l’eau . [4]Cependant, certains métaux et solutés, tels que le fer et le carbone, ont des points de fusion très élevés et étaient impossibles à fondre pour les peuples anciens. Ainsi, l’alliage (en particulier l’Alliage interstitiel) peut également être réalisé avec un ou plusieurs constituants à l’état gazeux, tel qu’on en trouve dans un haut-fourneau pour faire de la fonte brute (liquide-gaz), la nitruration , la carbonitruration ou d’autres formes de Cémentation . (solide-gaz), ou le processus de Cémentation utilisé pour fabriquer de l’ acier blister (solide-gaz). Il peut également être fait avec un, plusieurs ou tous les constituants à l’état solide, comme on en trouve dans les méthodes anciennes de soudage par motifs (solide-solide), l’Acier de cisaillement(solide-solide), ou production d’acier en creuset (solide-liquide), mélangeant les éléments par diffusion à l’état solide .
En ajoutant un autre élément à un métal, les différences de taille des atomes créent des contraintes internes dans le réseau des cristaux métalliques ; stress qui renforcent souvent ses propriétés. Par exemple, la combinaison du carbone avec le fer produit de l’ acier , qui est plus résistant que le fer , son élément principal. La Conductivité électrique et thermique des alliages est généralement inférieure à celle des métaux purs. Les propriétés physiques, telles que la densité , la réactivité , le module d’Young d’un alliage peuvent ne pas différer grandement de celles de son élément de base, mais les propriétés techniques telles que la Résistance à la traction , [5] la ductilité etla résistance au cisaillement peut être sensiblement différente de celles des matériaux constitutifs. Cela est parfois dû à la taille des atomes dans l’alliage, car les atomes plus gros exercent une force de compression sur les atomes voisins, et les atomes plus petits exercent une force de traction sur leurs voisins, aidant l’alliage à résister à la déformation. Parfois, les alliages peuvent présenter des différences de comportement marquées même lorsque de petites quantités d’un élément sont présentes. Par exemple, les impuretés dans les alliages ferromagnétiques semi-conducteurs conduisent à des propriétés différentes, comme l’ont d’abord prédit White, Hogan, Suhl, Tian Abrie et Nakamura. [6] [7]
Contrairement aux métaux purs, la plupart des alliages n’ont pas un point de fusion unique , mais une plage de fusion au cours de laquelle le matériau est un mélange de phases solide et liquide (une bouillie). La température à laquelle la fusion commence s’appelle le solidus , et la température à laquelle la fusion est juste terminée s’appelle le liquidus . Pour de nombreux alliages, il existe une proportion d’alliage particulière (dans certains cas plus d’un), appelée soit un mélange Eutectique , soit une composition péritectique, qui donne à l’alliage un point de fusion unique et bas, et aucune transition liquide/solide de neige fondue.
Traitement thermique
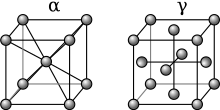
 Allotropes du fer , ( fer alpha et fer gamma ) montrant les différences d’arrangement atomique
Allotropes du fer , ( fer alpha et fer gamma ) montrant les différences d’arrangement atomique 
 Photomicrographies d’ acier . Photo du haut : l’acier recuit (refroidi lentement) forme une microstructure lamellaire hétérogène appelée perlite , composée des phases cémentite (claire) et ferrite (foncée). Photo du bas : l’ acier trempé (rapidement refroidi) forme une phase unique appelée martensite , dans laquelle le carbone reste piégé dans les cristaux, créant des contraintes internes
Photomicrographies d’ acier . Photo du haut : l’acier recuit (refroidi lentement) forme une microstructure lamellaire hétérogène appelée perlite , composée des phases cémentite (claire) et ferrite (foncée). Photo du bas : l’ acier trempé (rapidement refroidi) forme une phase unique appelée martensite , dans laquelle le carbone reste piégé dans les cristaux, créant des contraintes internes
Des éléments d’alliage sont ajoutés à un métal de base pour induire la dureté , la ténacité , la ductilité ou d’autres propriétés souhaitées. La plupart des métaux et alliages peuvent être écrouis en créant des défauts dans leur structure cristalline. Ces défauts sont créés lors de la déformation plastique par martelage, pliage, extrusion, etc., et sont permanents à moins que le métal ne soit recristallisé . Sinon, certains alliages peuvent également voir leurs propriétés altérées par un Traitement thermique . Presque tous les métaux peuvent être adoucis par recuit , ce qui recristallise l’alliage et répare les défauts, mais moins d’entre eux peuvent être durcis par un chauffage et un refroidissement contrôlés. De nombreux alliages del’aluminium , le cuivre , le magnésium , le titane et le nickel peuvent être renforcés dans une certaine mesure par une méthode de Traitement thermique, mais peu y répondent au même degré que l’ acier . [8]
Le fer, un métal de base de l’alliage fer-carbone connu sous le nom d’acier, subit une modification de l’arrangement ( allotropie ) des atomes de sa matrice cristalline à une certaine température (généralement entre 1 500 ° F (820 ° C) et 1 600 ° F ( 870 °C), selon la teneur en carbone). Cela permet aux plus petits atomes de carbone d’entrer dans les interstices du cristal de fer. Lorsque cette diffusion se produit, les atomes de carbone sont dits en solution dans le fer, formant une phase cristalline particulière, homogène et unique appelée austénite . Si l’acier est refroidi lentement, le carbone peut diffuser hors du fer et il reviendra progressivement à son allotrope à basse température. Lors d’un refroidissement lent, les atomes de carbone ne seront plus aussi solublesavec le fer, et sera forcé de précipiter hors de la solution, nucléant en une forme plus concentrée de carbure de fer (Fe 3 C) dans les espaces entre les cristaux de fer pur. L’acier devient alors hétérogène, car il est formé de deux phases, la phase fer-carbone appelée cémentite (ou carbure ), et la ferrite de fer pur . Un tel Traitement thermique produit un acier plutôt doux. Si l’acier est refroidi rapidement, cependant, les atomes de carbone n’auront pas le temps de se diffuser et de précipiter sous forme de carbure, mais seront piégés dans les cristaux de fer. Lors d’un refroidissement rapide, une transformation sans diffusion (martensite)se produit, dans lequel les atomes de carbone sont piégés en solution. Cela provoque la déformation des cristaux de fer lorsque la structure cristalline tente de passer à son état à basse température, laissant ces cristaux très durs mais beaucoup moins ductiles (plus cassants).
Alors que la haute résistance de l’acier résulte de l’empêchement de la diffusion et de la précipitation (formation de martensite), la plupart des alliages pouvant être traités thermiquement sont des alliages à durcissement par précipitation , qui dépendent de la diffusion des éléments d’alliage pour atteindre leur résistance. Lorsqu’ils sont chauffés pour former une solution puis refroidis rapidement, ces alliages deviennent beaucoup plus mous que la normale, lors de la transformation sans diffusion, mais durcissent ensuite en vieillissant. Les solutés de ces alliages précipiteront avec le temps, formant des composés intermétalliques .phases difficiles à discerner du métal de base. Contrairement à l’acier, dans lequel la solution solide se sépare en différentes phases cristallines (carbure et ferrite), les alliages à durcissement par précipitation forment différentes phases au sein d’un même cristal. Ces alliages intermétalliques semblent homogènes dans la structure cristalline, mais ont tendance à se comporter de manière hétérogène, devenant durs et quelque peu cassants. [8]
En 1906, des alliages à durcissement par précipitation ont été découverts par Alfred Wilm . Les alliages à durcissement par précipitation, tels que certains alliages d’ aluminium , de titane et de cuivre, sont des alliages pouvant être traités thermiquement qui se ramollissent lorsqu’ils sont trempés (refroidis rapidement), puis durcissent avec le temps. Wilm cherchait un moyen de durcir les alliages d’aluminium pour les utiliser dans les étuis de cartouches de mitrailleuses. Sachant que les alliages aluminium-cuivre pouvaient être traités thermiquement dans une certaine mesure, Wilm a essayé de tremper un alliage ternaire d’aluminium, de cuivre et d’ajouter du magnésium ., mais a d’abord été déçu des résultats. Cependant, lorsque Wilm l’a retesté le lendemain, il a découvert que la dureté de l’alliage augmentait lorsqu’il était laissé vieillir à température ambiante et dépassait de loin ses attentes. Bien qu’une explication du phénomène n’ait été fournie qu’en 1919, le duralumin a été l’un des premiers alliages “à durcissement par vieillissement” utilisés, devenant le principal matériau de construction des premiers Zeppelins , et a été bientôt suivi par de nombreux autres. [9] Parce qu’ils présentent souvent une combinaison de haute résistance et de faible poids, ces alliages sont devenus largement utilisés dans de nombreuses formes d’industrie, y compris la construction d’ avions modernes . [dix]
Mécanismes
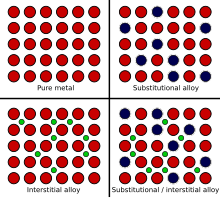
 Différents mécanismes atomiques de formation d’alliage, montrant le métal pur, substitutionnel, interstitiel et une combinaison des deux
Différents mécanismes atomiques de formation d’alliage, montrant le métal pur, substitutionnel, interstitiel et une combinaison des deux
Lorsqu’un métal en fusion est mélangé à une autre substance, deux mécanismes peuvent provoquer la formation d’un alliage, appelés échange d’atomes et mécanisme interstitiel . La taille relative de chaque élément dans le mélange joue un rôle primordial dans la détermination du mécanisme qui se produira. Lorsque les atomes sont de taille relativement similaire, la méthode d’échange d’atomes se produit généralement, où certains des atomes composant les cristaux métalliques sont remplacés par des atomes de l’autre constituant. C’est ce qu’on appelle un alliage de substitution . Des exemples d’alliages de substitution comprennent le bronze et le laiton , dans lesquels certains des atomes de cuivre sont respectivement remplacés par des atomes d’étain ou de zinc.
Dans le cas du mécanisme interstitiel, un atome est généralement beaucoup plus petit que l’autre et ne peut pas se substituer avec succès à l’autre type d’atome dans les cristaux du métal de base. Au lieu de cela, les atomes plus petits sont piégés dans les espaces entre les atomes de la matrice cristalline, appelés les interstices . C’est ce qu’on appelle un Alliage interstitiel . L’acier est un exemple d’Alliage interstitiel, car les très petits atomes de carbone s’insèrent dans les interstices de la matrice de fer.
L’acier inoxydable est un exemple d’une combinaison d’alliages interstitiels et de substitution, car les atomes de carbone s’insèrent dans les interstices, mais certains des atomes de fer sont remplacés par des atomes de nickel et de chrome. [8]
Histoire et exemples


Fer météorique
L’utilisation des alliages par l’homme a commencé avec l’utilisation du fer météorique , un alliage naturel de nickel et de fer . C’est le principal constituant des météorites ferreuses . Comme aucun procédé métallurgique n’a été utilisé pour séparer le fer du nickel, l’alliage a été utilisé tel quel. [11] Le fer météorique pouvait être forgé à partir d’une chaleur rouge pour fabriquer des objets tels que des outils, des armes et des clous. Dans de nombreuses cultures, il a été façonné par martelage à froid dans des couteaux et des pointes de flèches. Ils servaient souvent d’enclumes. Le fer météorique était très rare et précieux, et difficile à travailler pour les anciens . [12]
Bronze et laiton




Le fer se trouve généralement sous forme de minerai de fer sur Terre, à l’exception d’un gisement de fer natif au Groenland , qui était utilisé par les Inuits . [13] Le cuivre natif , cependant, a été trouvé dans le monde entier, ainsi que l’argent , l’or et le platine , qui ont également été utilisés pour fabriquer des outils, des bijoux et d’autres objets depuis le néolithique. Le cuivre était le plus dur de ces métaux et le plus répandu. Il est devenu l’un des métaux les plus importants pour les anciens. Il y a environ 10 000 ans, dans les hautes terres d’ Anatolie (Turquie), les humains ont appris à fondre des métaux tels que le cuivre etétain de minerai . Vers 2500 avant JC, les gens ont commencé à allier les deux métaux pour former du bronze , qui était beaucoup plus dur que ses ingrédients. L’étain était rare, cependant, se trouvant principalement en Grande-Bretagne. Au Moyen-Orient, les gens ont commencé à allier le cuivre au zinc pour former du laiton . [14] Les civilisations anciennes ont pris en compte le mélange et les diverses propriétés qu’il produisait, telles que la dureté , la ténacité et le point de fusion , dans diverses conditions de température et d’ écrouissage , développant une grande partie des informations contenues dans les diagrammes de phase des alliages modernes .[15] Par exemple, les pointes de flèches de la dynastie chinoise Qin (vers 200 av. J.-C.) étaient souvent construites avec une tête en bronze dur, mais une soie en bronze plus douce, combinant les alliages pour éviter à la fois de s’émousser et de se casser pendant l’utilisation. [16]
Amalgames
Le mercure a été fondu à partir de cinabre pendant des milliers d’années. Le mercure dissout de nombreux métaux, tels que l’or, l’argent et l’étain, pour former des amalgames (un alliage sous forme de pâte molle ou liquide à température ambiante). Les amalgames sont utilisés depuis 200 avant JC en Chine pour dorer des objets tels que des armures et des miroirs avec des métaux précieux. Les anciens Romains utilisaient souvent des amalgames mercure-étain pour dorer leurs armures. L’amalgame était appliqué sous forme de pâte puis chauffé jusqu’à ce que le mercure se vaporise, laissant derrière lui l’or, l’argent ou l’étain. [17] Le mercure était souvent utilisé dans les mines, pour extraire des métaux précieux comme l’or et l’argent de leurs minerais. [18]
Métaux précieux

 L’électrum , un alliage naturel d’argent et d’or, était souvent utilisé pour fabriquer des pièces de monnaie
L’électrum , un alliage naturel d’argent et d’or, était souvent utilisé pour fabriquer des pièces de monnaie
De nombreuses civilisations anciennes ont allié des métaux à des fins purement esthétiques. Dans l’ Egypte ancienne et à Mycènes , l’or était souvent allié avec du cuivre pour produire de l’Or rouge, ou du fer pour produire un or bordeaux brillant. L’or était souvent trouvé allié avec de l’argent ou d’autres métaux pour produire divers types d’ or coloré . Ces métaux étaient également utilisés pour se renforcer mutuellement, à des fins plus pratiques. Le cuivre était souvent ajouté à l’argent pour fabriquer de l’ argent sterling , augmentant sa résistance pour une utilisation dans la vaisselle, l’argenterie et d’autres articles pratiques. Très souvent, les métaux précieux étaient alliés à des substances moins précieuses afin de tromper les acheteurs. [19] Vers 250 av. J.-C., Archimède est mandaté par le roi deSyracuse pour trouver un moyen de vérifier la pureté de l’or d’une couronne, ce qui a conduit au célèbre cri des bains publics “Eureka!” à la découverte du principe d’Archimède . [20]
Étain
Le terme étain couvre une variété d’alliages constitués principalement d’étain. En tant que métal pur, l’étain est beaucoup trop mou pour être utilisé à des fins pratiques. Cependant, à l’ âge du bronze , l’étain était un métal rare dans de nombreuses régions d’Europe et de la Méditerranée, il était donc souvent plus valorisé que l’or. Pour fabriquer des bijoux, des couverts ou d’autres objets en étain, les ouvriers l’alliaient généralement avec d’autres métaux pour augmenter la résistance et la dureté. Ces métaux étaient généralement du plomb , de l’antimoine , du bismuthou cuivre. Ces solutés étaient parfois ajoutés individuellement en quantités variables, ou additionnés, créant une grande variété d’objets, allant d’objets pratiques tels que des plats, des outils chirurgicaux, des chandeliers ou des entonnoirs, à des objets décoratifs tels que des boucles d’oreilles et des pinces à cheveux.
Les premiers exemples d’étain proviennent de l’Égypte ancienne, vers 1450 av. L’utilisation de l’étain était répandue dans toute l’Europe, de la France à la Norvège et la Grande-Bretagne (où la plupart de l’étain ancien était extrait) au Proche-Orient. [21] L’alliage a également été utilisé en Chine et en Extrême-Orient, arrivant au Japon vers 800 après JC, où il a été utilisé pour fabriquer des objets tels que des récipients de cérémonie, des boîtes à thé ou des calices utilisés dans les sanctuaires shinto . [22]
Fer

 Formation de flaques en Chine, vers 1637. Contrairement à la plupart des processus d’alliage, la fonte brute liquide est versée d’un haut fourneau dans un récipient et agitée pour éliminer le carbone, qui se diffuse dans l’air en formant du dioxyde de carbone, laissant derrière lui un Acier doux au fer forgé .
Formation de flaques en Chine, vers 1637. Contrairement à la plupart des processus d’alliage, la fonte brute liquide est versée d’un haut fourneau dans un récipient et agitée pour éliminer le carbone, qui se diffuse dans l’air en formant du dioxyde de carbone, laissant derrière lui un Acier doux au fer forgé .
La première fonderie connue de fer a commencé en Anatolie , vers 1800 av. Appelé le procédé bloomery , il produisait du fer forgé très doux mais ductile . En 800 avant JC, la technologie de fabrication du fer s’était répandue en Europe, arrivant au Japon vers 700 après JC. La fonte brute , un alliage très dur mais cassant de fer et de carbone , était produite en Chine dès 1200 av. J.-C., mais n’arriva en Europe qu’au Moyen Âge. La fonte brute a un point de fusion inférieur à celui du fer et a été utilisée pour fabriquer de la fonte . Cependant, ces métaux ont trouvé peu d’utilisation pratique jusqu’à l’introduction de l’acier à creuset.vers 300 av. Ces aciers étaient de mauvaise qualité, et l’introduction du soudage par motifs , vers le 1er siècle après JC, a cherché à équilibrer les propriétés extrêmes des alliages en les laminant, pour créer un métal plus résistant. Vers 700 après JC, les Japonais ont commencé à plier l’acier de floraison et la fonte en couches alternées pour augmenter la résistance de leurs épées, en utilisant des fondants d’argile pour éliminer les scories et les impuretés. Cette méthode de fabrication d’ épées japonaises a produit l’un des alliages d’acier les plus purs du monde antique. [15]
Alors que l’utilisation du fer a commencé à se généraliser vers 1200 av. J.-C., principalement en raison des interruptions des routes commerciales de l’étain, le métal était beaucoup plus tendre que le bronze. Cependant, de très petites quantités d’ acier (un alliage de fer et environ 1% de carbone) ont toujours été un sous-produit du processus de bloomery. La capacité de modifier la dureté de l’acier par Traitement thermique était connue depuis 1100 avant JC, et le matériau rare était apprécié pour la fabrication d’outils et d’armes. Parce que les anciens ne pouvaient pas produire des températures suffisamment élevées pour fondre complètement le fer, la production d’acier en quantités décentes n’a pas eu lieu avant l’introduction de l’ acier blister.pendant le Moyen Age. Cette méthode a introduit du carbone en chauffant du fer forgé dans du charbon de bois pendant de longues périodes, mais l’absorption du carbone de cette manière est extrêmement lente, donc la pénétration n’était pas très profonde, donc l’alliage n’était pas homogène. En 1740, Benjamin Huntsman a commencé à faire fondre de l’acier blister dans un creuset pour égaliser la teneur en carbone, créant ainsi le premier procédé de production de masse d’ acier à outils . Le procédé de Huntsman a été utilisé pour fabriquer de l’acier à outils jusqu’au début des années 1900. [23]
L’introduction du haut fourneau en Europe au Moyen Âge signifiait que les gens pouvaient produire de la fonte brute en volumes beaucoup plus élevés que le fer forgé. Parce que la fonte brute pouvait être fondue, les gens ont commencé à développer des procédés pour réduire le carbone dans la fonte brute liquide pour créer de l’acier. La formation de flaques d’eau était utilisée en Chine depuis le premier siècle et a été introduite en Europe au cours des années 1700, où la fonte brute fondue était agitée lorsqu’elle était exposée à l’air, pour éliminer le carbone par oxydation . En 1858, Henry Bessemer a mis au point un procédé de fabrication de l’acier en soufflant de l’air chaud à travers de la fonte brute liquide pour réduire la teneur en carbone. Le procédé Bessemer a conduit à la première fabrication d’acier à grande échelle. [23]
L’acier est un alliage de fer et de carbone, mais le terme acier allié ne fait généralement référence qu’aux aciers contenant d’autres éléments, tels que le vanadium , le molybdène ou le cobalt , en quantités suffisantes pour modifier les propriétés de l’acier de base. Depuis les temps anciens, lorsque l’acier était principalement utilisé pour les outils et les armes, les méthodes de production et de travail du métal étaient souvent des secrets bien gardés. Même longtemps après l’ âge de raison , l’industrie sidérurgique était très compétitive et les fabricants se sont donné beaucoup de mal pour garder leurs procédés confidentiels, résistant à toute tentative d’analyse scientifique du matériau de peur qu’il ne révèle leurs méthodes. Par exemple, les habitants de Sheffield, un centre de production d’acier en Angleterre, était connu pour empêcher régulièrement les visiteurs et les touristes d’entrer dans la ville afin de dissuader l’espionnage industriel . Ainsi, presque aucune information métallurgique n’existait sur l’acier jusqu’en 1860. En raison de ce manque de compréhension, l’acier n’était généralement pas considéré comme un alliage jusqu’aux décennies entre 1930 et 1970 (principalement en raison des travaux de scientifiques comme William Chandler Roberts-Austen , Adolf Martens , et Edgar Bain ), ainsi “l’acier allié” est devenu le terme populaire pour les alliages d’acier ternaires et quaternaires. [24] [25]
Après que Benjamin Huntsman ait développé son acier pour creuset en 1740, il a commencé à expérimenter l’ajout d’éléments comme le manganèse (sous la forme d’une fonte à haute teneur en manganèse appelée spiegeleisen ), qui a aidé à éliminer les impuretés telles que le phosphore et l’oxygène ; un procédé adopté par Bessemer et toujours utilisé dans les aciers modernes (bien qu’à des concentrations suffisamment faibles pour être toujours considéré comme de l’acier au carbone). [26] Par la suite, de nombreuses personnes ont commencé à expérimenter divers alliages d’acier sans grand succès. Cependant, en 1882, Robert Hadfield , étant un pionnier de la métallurgie de l’acier, s’y intéresse et produit un alliage d’acier contenant environ 12 % de manganèse. Appelé mangalloy, il présentait une dureté et une ténacité extrêmes, devenant le premier alliage d’acier commercialement viable. [27] Par la suite, il crée l’ Acier au silicium , lançant la recherche d’autres alliages d’acier possibles. [28]
Robert Forester Mushet a découvert qu’en ajoutant du tungstène à l’acier, il pouvait produire un bord très dur qui résisterait à la perte de sa dureté à des températures élevées. “L’acier spécial de R. Mushet” (RMS) est devenu le premier acier rapide . [29] L’acier de Mushet a été rapidement remplacé par l’acier au carbure de tungstène , développé par Taylor et White en 1900, dans lequel ils ont doublé la teneur en tungstène et ajouté de petites quantités de chrome et de vanadium, produisant un acier supérieur à utiliser dans les tours et les outils d’usinage. En 1903, les frères Wright utilisent un acier au chrome-nickel pour fabriquer le vilebrequin de leur moteur d’avion, tandis qu’en 1908, Henry Forda commencé à utiliser des aciers au vanadium pour des pièces comme les vilebrequins et les soupapes de sa Ford modèle T , en raison de leur résistance plus élevée et de leur résistance aux températures élevées. [30] En 1912, Krupp Ironworks en Allemagne a développé un acier résistant à la rouille en ajoutant 21 % de chrome et 7 % de nickel , produisant le premier acier inoxydable . [31]
Autres
En raison de leur grande réactivité, la plupart des métaux n’ont été découverts qu’au XIXe siècle. Une méthode d’extraction de l’aluminium de la bauxite a été proposée par Humphry Davy en 1807, à l’aide d’un arc électrique . Bien que ses tentatives aient échoué, en 1855, les premières ventes d’aluminium pur atteignirent le marché. Cependant, comme la métallurgie extractive en était encore à ses balbutiements, la plupart des procédés d’extraction de l’aluminium produisaient des alliages involontaires contaminés par d’autres éléments trouvés dans le minerai; dont le plus abondant était le cuivre. Ces alliages aluminium-cuivre (à l’époque appelés «bronze d’aluminium») ont précédé l’aluminium pur, offrant une plus grande résistance et dureté par rapport au métal doux et pur, et se sont avérés, dans une légère mesure, traitables thermiquement. [32]Cependant, en raison de leur douceur et de leur trempabilité limitée, ces alliages ont trouvé peu d’utilisation pratique et étaient plutôt une nouveauté, jusqu’à ce que les frères Wright utilisent un alliage d’aluminium pour construire le premier moteur d’avion en 1903. [30] Entre 1865 et 1910 , des procédés d’extraction de nombreux autres métaux ont été découverts, tels que le chrome, le vanadium, le tungstène, l’ iridium , le cobalt et le molybdène , et divers alliages ont été développés. [33]
Avant 1910, la recherche consistait principalement en des particuliers qui bricolent dans leurs propres laboratoires. Cependant, alors que les industries aéronautique et automobile commençaient à se développer, la recherche sur les alliages est devenue un effort industriel dans les années qui ont suivi 1910, alors que de nouveaux alliages de magnésium ont été développés pour les pistons et les roues des voitures, et du métal en pot pour les leviers et les boutons, et des alliages d’aluminium développés pour des cellules et des revêtements d’avions ont été mis en service. [30]
Voir également
- Élargissement de l’alliage
- CALPHAD
- Mélange idéal
- Liste des alliages
Références
- ^ Callister, WD “Materials Science and Engineering: An Introduction” 2007, 7e édition, John Wiley and Sons, Inc. New York, Section 4.3 et Chapitre 9.
- ^ Verhoeven, John D. (2007). Métallurgie de l’acier pour le non-métallurgiste . ASM International. p. 56. ISBN 978-1-61503-056-9. Archivé de l’original le 2016-05-05.
- ^ Davis, Joseph R. (1993) Manuel de spécialité ASM : Aluminium et alliages d’aluminium . ASM International. p. 211. ISBN 978-0-87170-496-2 .
- ^ Manuel des métaux: Propriétés et sélection Par ASM International – ASM International 1978 Page 407
- ^ Mills, Adelbert Phillo (1922) Materials of Construction: Their Manufacture and Properties , John Wiley & sons, inc, initialement publié par l’Université du Wisconsin, Madison
- ^ Hogan, C. (1969). “Densité d’états d’un alliage Ferromagnétique isolant”. Examen physique . 188 (2): 870–874. Bibcode : 1969PhRv..188..870H . doi : 10.1103/PhysRev.188.870 .
- ^ Zhang, X.; En ligneSuhl, H. (1985). “Doublements de période liés aux ondes de spin et chaos sous pompage transversal”. Examen physique A . 32 (4): 2530-2533. Bibcode : 1985PhRvA..32.2530Z . doi : 10.1103/PhysRevA.32.2530 . PMID 9896377 .
- ^ un bc Dossett , Jon L. et Boyer, Howard E. (2006) Traitement thermique pratique . ASM International. p. 1–14. ISBN 1-61503-110-3 .
- ^ Métallurgie pour le non-métallurgiste par Harry Chandler – ASM International 1998 Page 1—3
- ^ Jacobs, MH Durcissement des précipitations Archivé le 02/12/2012 à la Wayback Machine . Université de Birmingham. Conférence TALAT 1204. slideshare.net
- ^ Rickard, TA (1941). “L’utilisation du fer météorique”. Journal de l’Institut royal d’anthropologie . 71 (1/2): 55–66. doi : 10.2307/2844401 . JSTOR 2844401 .
- ^ Buchwald , p. 13-22
- ^ Buchwald , pp. 35-37
- ^ Buchwald , pp. 39-41
- ^ un b Smith, Cyril (1960) Histoire de métallographie . Presse du MIT. p. 2–4. ISBN 0-262-69120-5 .
- ^ L’armée fantôme de l’empereur Archivé le 01/11/2017 à la Wayback Machine . pbs.org. novembre 2014
- ^ Rapp, George (2009) Archéominéralogie Archivé le 28/04/2016 à la Wayback Machine . Springer. p. 180. ISBN 3-540-78593-0
- ^ Miskimin, Harry A. (1977) L’économie de la fin de l’Europe de la Renaissance, 1460–1600 Archivé le 05/05/2016 à la Wayback Machine . La presse de l’Universite de Cambridge. p. 31. ISBN 0-521-29208-5 .
- ^ Nicholson, Paul T. et Shaw, Ian (2000) Matériaux et technologie de l’Égypte ancienne Archivé le 02/05/2016 à la Wayback Machine . La presse de l’Universite de Cambridge. pp. 164–167. ISBN 0-521-45257-0 .
- ^ Kay, Melvyn (2008) Hydraulique pratique Archivé le 03/06/2016 à la Wayback Machine . Taylor et François. p. 45. ISBN 0-415-35115-4 .
- ^ Hull, Charles (1992) Étain . Publications de la Comté. p. 3–4 ; ISBN 0-7478-0152-5
- ^ Brinkley, Frank (1904) Le Japon et la Chine : le Japon, son histoire, ses arts et sa littérature . L’université d’Oxford. p. 317
- ^ un b Roberts, George Adam; Krauss, George; Kennedy, Richard et Kennedy, Richard L. (1998) Aciers à outils Archivé le 24/04/2016 à la Wayback Machine . ASM International. p. 2–3. ISBN 0-87170-599-0 .
- ^ Sheffield Steel and America: Un siècle d’indépendance commerciale et technologique Par Geoffrey Tweedale – Cambridge University Press 1987 Page 57-62
- ^ Techniques expérimentales en matériaux et mécanique Par C. Suryanarayana – CRC Press 2011 p. 202
- ^ Aciers à outils, 5e édition Par George Adam Roberts, Richard Kennedy, G. Krauss – ASM International 1998 p. 4
- ^ Bramfitt, BL (2001). Guide du métallographe : pratiques et procédures pour les fers et les aciers . ASM International. p. 13–. ISBN 978-1-61503-146-7. Archivé de l’original le 2016-05-02.
- ^ Sheffield Steel and America: Un siècle d’indépendance commerciale et technologique Par Geoffrey Tweedale – Cambridge University Press 1987 pp. 57-62
- ^ Sheffield Steel and America: Un siècle d’indépendance commerciale et technologique Par Geoffrey Tweedale – Cambridge University Press 1987 pp. 66-68
- ^ a b c Métallurgie pour le non-métallurgiste par Harry Chandler – ASM International 1998 Page 3—5
- ^ Sheffield Steel and America: Un siècle d’indépendance commerciale et technologique Par Geoffrey Tweedale – Cambridge University Press 1987 p. 75
- ^ Aluminium: son histoire, son occurrence, ses propriétés, sa métallurgie et ses applications par Joseph William Richards – Henry Cairy Baird & Co 1887 Page 25—42
- ^ Métallurgie: 1863-1963 par WH Dennis – Routledge 2017
Bibliographie
- Buchwald, Vagn Fabritius (2005). Le fer et l’acier dans l’Antiquité . Det Kongelige Danske Videnskabernes Selskab. ISBN 978-87-7304-308-0.
Liens externes
| Recherchez alliage dans Wiktionary, le dictionnaire gratuit. |
| Wikimedia Commons a des médias liés aux alliages . |
- Roberts-Austen, William Chandler ; Neville, Francis Henry (1911). “Alliages” . Encyclopædia Britannica (11e éd.).
- “Alliage” . La Cyclopaedia américaine . 1879.
